DALGreen - Autophagy Detection

オートファジー(オートリソソーム)の検出試薬
-
製品コードD675 DALGreen - Autophagy Detection
| 容 量 | メーカー希望 小売価格 |
富士フイルム 和光純薬 |
|---|---|---|
| 20 nmol | ¥37,700 | 344-09191 |
 DALGreenの最適濃度の検討については、
DALGreenの最適濃度の検討については、
よくある質問の「DALGreenの最適濃度の検討方法を教えてください」
をご覧ください。
性質
DALGreenは、細胞内の不要なタンパク質・細胞小器官などの再利用や、代謝のための分解過程であるオートファジーを検出できる蛍光色素である。培養細胞に添加したDALGreenは生細胞膜を透過し、オートファジー誘導により形成されたオートファゴソーム内に取り込まる。その後、リソソームと融合し酸性環境となったオートリソソームにおいてDALGreenの蛍光が増大する。
技術情報
原理
 |
|
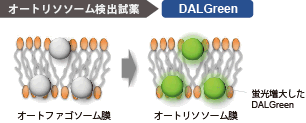 |
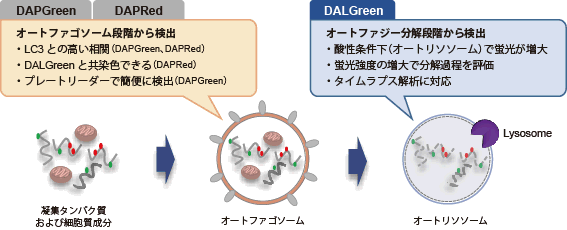
DAPGreen、DAPRedと同様にオートファゴソーム形成時に色素が膜に取り込まれます。その後、リソソームと融合し酸性環境になったときにDALGreenの蛍光が増大します。 |
操作は試薬添加だけ
遺伝子導入が不要。準備した細胞に試薬を添加するだけの簡単操作で蛍光イメージングを実現できます。
オートファジー検出試薬の比較表
蛍光顕微鏡だけでなくフローサイトメーターでも検出頂けます。またDAPGreenでは、プレートリーダーによる検出も実現しました。ご使用の装置で検出可能な蛍光特性をご確認の上、ご使用ください。
| 対応装置 | 蛍光特性 | 容量 / 使用回数 の目安 |
既存検出法 | |||
|---|---|---|---|---|---|---|
| 蛍光顕微鏡 | フローサイト メーター |
プレート リーダー |
||||
| DAPGreen | ○ | ○ | ○ | Ex. 425-475 Em. 500-560 ※ 共焦点顕微鏡では 488 nmにて励起可能 |
5 nmol x 1 / 35 mm dish: 25枚分 (0.1 μmol/lで使用時) |
LC3-GFP MDC Cyto-ID など |
| DAPRed (オートファゴソーム検出) |
○ | × | × | Ex. 500-560 nm Em. 690-750 nm |
5 nmol x 1 / 35 mm dish: 25枚分 (0.1 μmol/lで使用時) |
|
| DALGreen (オートリソソーム検出) |
○ | ○ | × | Ex. 350-450 Em. 500-560 ※ 共焦点顕微鏡では 488 nmにて励起可能 |
20 nmol x 1 / 35 mm dish: 10枚分 (1.0 μmol/lで使用時) |
LC3-GFP-RFP など |
※ DAPGreenとDALGreenの共染色イメージングはできません。
LC3との共染色
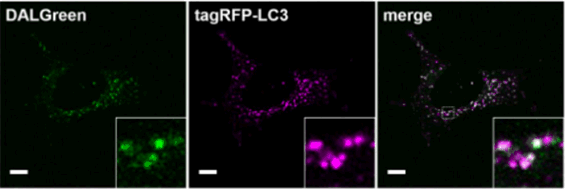
tagRFP-LC3発現MEF細胞へDALGreenとの共染色を行いました。結果、オートファゴソームおよびオートリソソームのマーカーであるLC3と殆ど共局在することが確認できました。(スケールバー:10 μm)
詳細は論文にて解説。
データ引用元: H. Iwashita, H. T. Sakurai, N. Nagahora, M. Ishiyama, K. Shioji, K. Sasamoto, K. Okuma, S. Shimizu, and Y. Ueno, "Small fluorescent molecules for monitoring autophagic flux", FEBS Letters., 2018, 592, (4), 559–567.
Lamp1との共染色
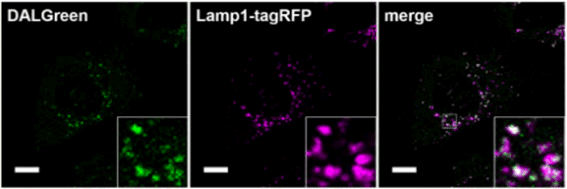
Lamp1-tagRFP発現MEF細胞へ、DALGreenとの共染色を行いました。結果、リソソーム膜タンパク質マーカーであるLamp1とDALGreenが共局在する結果が得られました。(スケールバー:10 μm)
詳細は論文にて解説。
データ引用元: H. Iwashita, H. T. Sakurai, N. Nagahora, M. Ishiyama, K. Shioji, K. Sasamoto, K. Okuma, S. Shimizu, and Y. Ueno, "Small fluorescent molecules for monitoring autophagic flux", FEBS Letters., 2018, 592, (4), 559–567.
ULK1/2ノックアウト細胞での評価
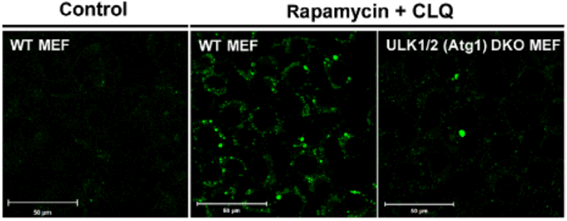
MEF細胞の野生株およびオートファゴソーム膜形成に関与しているULK1/2をノックアウトした株を用いてRapamycinとChloroquine刺激により比較。結果、野生株においてはDALGreenの蛍光強度の増大が確認されましたが、ULK1/2ノックアウトマウスにおいては、蛍光の増大は殆ど確認できませんでした。
詳細は論文にて解説。
データ引用元: H. Iwashita, H. T. Sakurai, N. Nagahora, M. Ishiyama, K. Shioji, K. Sasamoto, K. Okuma, S. Shimizu, and Y. Ueno, "Small fluorescent molecules for monitoring autophagic flux", FEBS Letters., 2018, 592, (4), 559–567.
LC3との比較
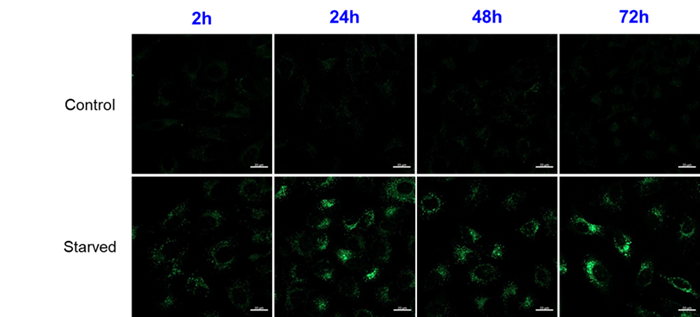
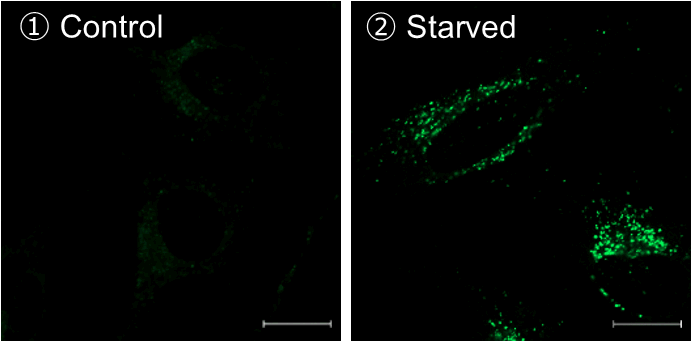
増殖培地にて培養したHeLa細胞(条件①)と飢餓培養にてオートファジーを誘導したHeLa細胞(条件②)を用いて、オートファジーマーカーであるLC3-IIの発現量とDALGreenによるイメージング像を比較した。
|
DALGreenによるイメージング |
LC3-II によるウエスタンブロット解析 |
結果
飢餓培養によりオートファジーを誘導したHeLa細胞においてDALGreenの蛍光強度の増大がみられた。また同様にLC3-II 発現量にも増加がみられ、双方の解析で相関する結果が得られた。
オートファジー誘導条件
① Control : 増殖培地で6時間培養
② 飢餓誘導 : アミノ酸不含培養培地で 6時間培養
DALGreenでのイメージング条件
細胞 :Hela細胞
検出波長 :Ex. 488 nm/ Em. 500-563 nm
スケールバー :20 μm
MDCとの比較
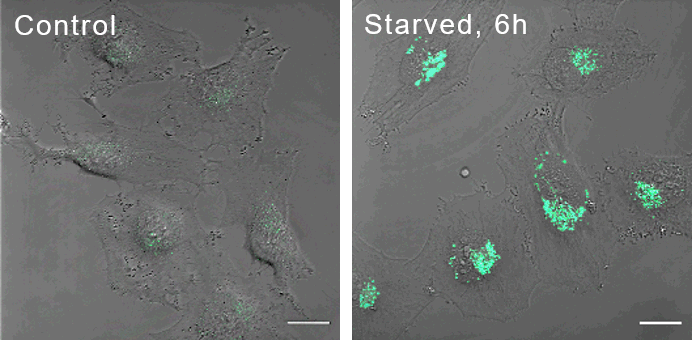
DALGreenと既存のオートファジー検出用蛍光色素MDC(Monodansylcadaverine)を用いて、飢餓条件下で培養したHeLa細胞におけるオートファジーを検出した。
DALGreenによるイメージング
濃度:1 μmol/l
インキュベート時間:30 min
検出波長:
Ex. 488 nm/ Em. 500-563 nm
スケールバー:40 μm
試薬添加後に飢餓誘導(6h)
MDCによるイメージング
濃度:10 μmol/l
インキュベート時間:30 min
検出波長:
Ex. 405 nm/ Em. 450-546 nm
スケールバー:40 μm
飢餓誘導(6h)後に試薬添加
結果
DALGreen 、MDCともに飢餓誘導された細胞で蛍光強度の増大がみられた。
波長
MDCの極大励起波長は紫外域にあるため488 nmでの励起は困難だが、DALGreenでは488 nmでの励起が可能である。
操作
DALGreen :試薬添加 ⇒ 飢餓誘導
MDC :飢餓誘導 ⇒ 試薬添加
DALGreenはオートファジー誘導前に試薬を添加するため、オートファジーをライブでモニターできる。
タイムラプス
再生できない方は、こちらからご覧いただけます。(別画面で開きます。)
HeLa細胞をDALGreenにて染色操作後、下記条件にて培養を開始し30分間隔で
6時間までの細胞の状態を観察した。
・Nutrient Condition :増殖培地
・Autophagic Condition :アミノ酸不含培養培地
<測定条件>
装置 :共焦点イメージングサイトメーター(横河電機株式会社:CQ1)
蛍光フィルター :Ex. 405 / Em. 525/50, 倍率:20X
DALGreenと既存方法の経時的な測定方法の比較
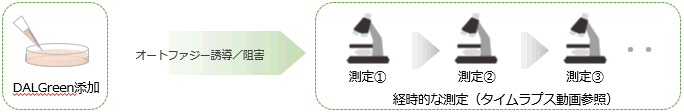
DALGreen
1つのサンプルで経時的な測定が可能
オートファジー誘導阻害前に試薬を添加するため、オートファジーをリアルタイムでモニターできる。
また、オートファジーの誘導阻害時間が不明な場合など、既存の試薬に比べて実験が楽になる。
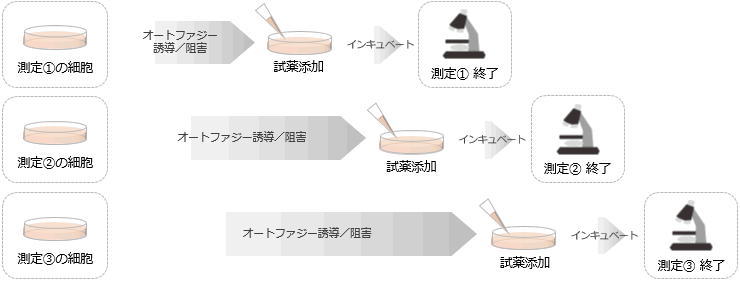
既存試薬
測定時間毎のサンプルが必要
MDC (Monodansylcadaverine)等の既存の試薬は、オートファジー誘導後に試薬を添加するため、
測定時間ごとに細胞の準備、オートファジーの誘導/阻害、試薬の添加が必要になる。
実験例:飢餓培養によるオートファジーとグルコース取込み変化
HeLa細胞をオートファゴソーム染色試薬DAPRedとオートリソソーム染色試薬DALGreenで染色した後、アミノ酸不含培地による飢餓培養を3時間行いオートファジーを誘導しました。DAPRedおよびDALGreenの蛍光強度が増大したことでオートファジーを確認し、また、Glucose Uptake Probe-Blueを用いて細胞のグルコース取り込み能力の上昇も観察されました。
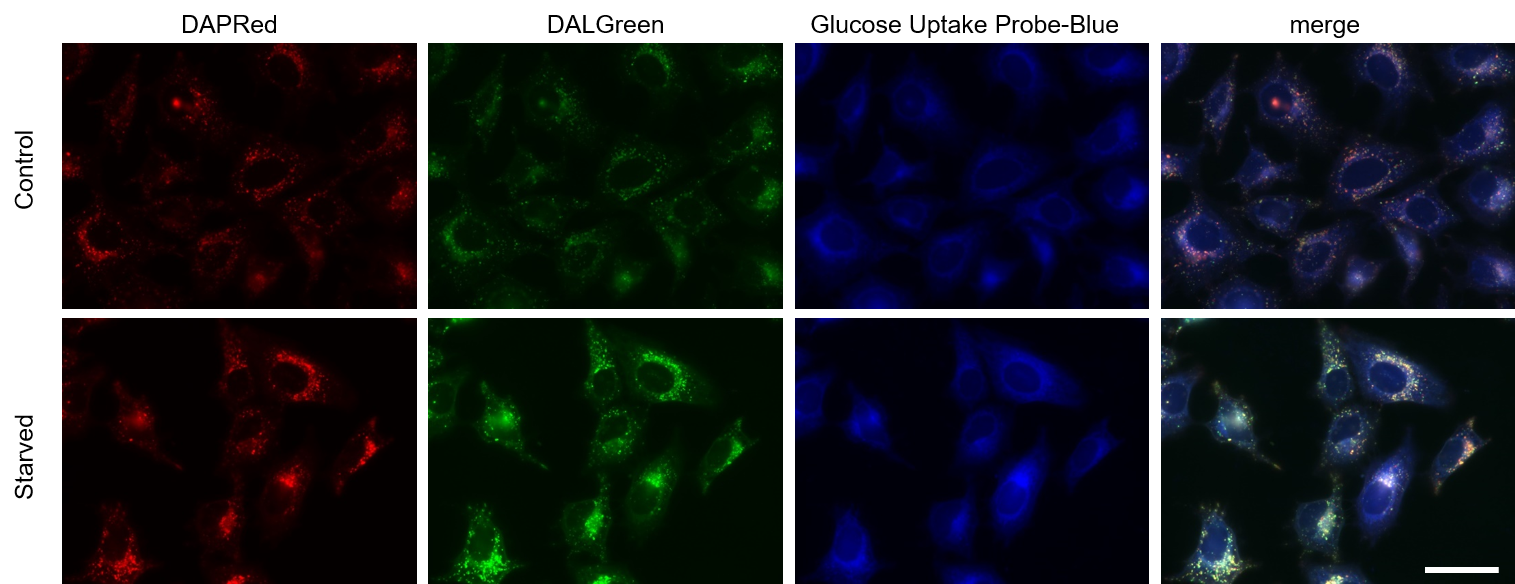
<検出条件>
落射型蛍光顕微鏡
Blue: Ex = 340-380 nm, Em = 435-485 nm
Green: Ex = 450-490 nm, Em = 500-550 nm
Red: Ex = 533-557 nm, Em = 570-640 nm
スケールバー: 50 μm
参考文献
| 文献No. | 対象サンプル | 装置 | 引用(リンク) |
|---|---|---|---|
| 1) | 細胞 (HeLa, MEF) |
蛍光顕微鏡 | H. Iwashita, H. T. Sakurai, N. Nagahora, M. Ishiyama, K. Shioji, K. Sasamoto, K. Okuma, S. Shimizu, and Y. Ueno, "Small fluorescent molecules for monitoring autophagic flux.", FEBS Letters., 2018, 592, (4), 559–567. |
| 2) | 細胞 (HeLa) |
蛍光顕微鏡 | T. Sakata, A. Saito and H. Sugimoto, "In situ measurement of autophagy under nutrient starvation based on interfacial pH sensing.", Scientific Reports., 2018, 8, 8282. |
| 3) | 細胞 (HS-MM) |
蛍光顕微鏡 | Y. Egawa, C. Saigo, Y. Kito, T. Moriki and T. Takeuchi, "Therapeutic potential of CPI-613 for targeting tumorous mitochondrial energy metabolism and inhibiting autophagy in clear cell sarcoma.", PLoS One., 2018, 13, (6), e0198940. |
| 4) | 細胞 (HaCaT) |
蛍光顕微鏡 | S. Abe, S. Hirose, M. Nishitani, I. Yoshida, M. Tsukayama, A. Tsuji and K. Yuasa, "Citrus peel polymethoxyflavones, sudachitin and nobiletin, induce distinct cellular responses in human keratinocyte HaCaT cells.", Biosci. Biotechnol. Biochem. ., 2018, 82, (12), 1347. |
| 5) | 細胞 (KGN) |
蛍光顕微鏡 | W. Yuping, M. Congshun, Z. Huihui, Z. Yuxia, C. Zhenguo and W. Liping, "Alleviation of endoplasmic reticulum stress protects against cisplatin-induced ovarian damage.", Reprod. Biol. Endocrinol., 2018,doi: 10.1186/s12958-018-0404-4. |
| 6) | 細胞 (BmN) |
蛍光顕微鏡 | S. Xue, F. Mao, D. Hu, H. Yan, J. Lei, E. Obeng, Y. Zhou, Y. Quan, and W. Yu, "Acetylation of BmAtg8 inhibits starvation-induced autophagy initiation.", Mol. Cell Biochem., 2019,doi: 10.1007/s11010-019-03513-y. |
| 7) | 細胞 (HeLa) |
蛍光顕微鏡 | F. Hongbao, Y. Shankun, C. Qixin, L. Chunyan, C. Yuqi, G. Shanshan, B. Yang, T. Zhiqi, L. Z. Amanda, T. Takanori, C.Yuncong, G. Zijian, H. Weijiang and D. Jiajie, "De Novo-Designed Near-Infrared Nanoaggregates for Super-Resolution Monitoring of Lysosomes in Cells, in Whole Organoids, and in Vivo.", ACS Nano, 2019, 13, (12), 1446. |
| 8) | 細胞 (RT-7) |
フローサイトメーター | E. Sasabe, A. Tomomura, N. Kitamura and T. Yamamoto, "Metal nanoparticles-induced activation of NLRP3 inflammasome in human oral keratinocytes is a possible mechanism of oral lichenoid lesions.", Toxicol In Vitro., 2020, 62, 104663. |
| 9) | 細胞 (骨髄腫) |
蛍光顕微鏡 | J. Xia, Y. He, B. Meng, S. Chen, J. Zhang, X. Wu, Y. Zhu, Y. Shen, X. Feng, Y. Guan, C. Kuang, J. Guo, Q. Lei, Y. Wu, G. An, G. Li, L. Qiu, F. Zhan and W. Zhou, "NEK2 induces autophagy-mediated bortezomib resistance by stabilizing Beclin-1 in multiple myeloma.", Mol Oncol, 2020, DOI: 10.1002/1878-0261.12641. |
| 10) | 細胞 (Human L2) |
蛍光顕微鏡 | Q. Xu, W. Shi, P. Lv, W. Meng, G. Mao, C. Gong, Y. Chen, Y. Wei, X. He, J. Zhao, H. Han, M. Sun and K. Xiao, "Critical role of caveolin-1 in aflatoxin B1-induced hepatotoxicity via the regulation of oxidation and autophagy.", Cell Death Dis., 2020, 11(1), 6. |
| 11) | 細胞 (心筋) |
蛍光顕微鏡 | L Cui, LP Zhao, JY Ye, L Yang, Y Huang, X.P. Jiang, Q. Zhang, JZ. Jia, DX. Zhang and Y. Huang, "The Lysosomal Membrane Protein Lamp2 Alleviates Lysosomal Cell Death by Promoting Autophagic Flux in Ischemic Cardiomyocytes.", Front Cell Dev Biol, 2020,DOI:10.3389/fcell.2020.00031. |
| 12) | 細胞 (IPEC-J2) |
蛍光顕微鏡 | Y Yang, J Huang, J Li, H Yang and Y. Yin, "The Effects of Butyric Acid on the Differentiation, Proliferation, Apoptosis, and Autophagy of IPEC-J2 Cells..", Curr. Mol. Med., 2020, 20(4), 307. |
| 13) | 細胞 (線維芽細胞、腎臓上皮細胞) | 蛍光顕微鏡 | M. M. Ivanova, J. Dao, N. Kasaci, B. Adewale, J. Fikry and O. G. Alpan, "Rapid Clathrin-Mediated Uptake of Recombinant α-Gal-A to Lysosome Activates Autophagy", Biomolecules, 2020, 10(6), 837. |
| 14) |
細胞 (NHEKs) |
蛍光顕微鏡 | S. Ikeoka and A. Kiso, "The Involvement of Mitophagy in the Prevention of UV-B-Induced Damage in Human Epidermal Keratinocytes ", J. Soc. Cosmet. Chem. Jpn., 2020, 54(3), 252. |
| 15) | 細胞 (HeLa) |
蛍光顕微鏡(超解像) | Q. Chen, M. Hao, L. Wang, L. Li, Y. Chen, X. Shao, Z. Tian, R. A. Pfuetzner, Q. Zhong, A. T. Brunger, J. Guan and J. Diao, "Prefused lysosomes cluster on autophagosomes regulated by VAMP8", Cell Death Dis., 2021, doi:10.1038/s41419-021-04243-0. |
| 16) | 細胞 (SH-SY5Y) |
蛍光顕微鏡 | Chang-ki Oh, Nima Dolatabadi, Piotr Cieplak, Maria T. Diaz-Meco, Jorge Moscat, John P. Nolan, Tomohiro Nakamura and Stuart A. Lipton, "S-Nitrosylation of p62 Inhibits Autophagic Flux to Promote α-Synuclein Secretion and Spread in Parkinson’s Disease and Lewy Body Dementia", J. Neurosci., 2022, doi:10.1523/JNEUROSCI.1508-21.2022. |
よくある質問
-
Q
DALGreen working solutionは、どのくらい安定ですか?
-
A
保存できません。用時調製してください。
-
Q
DMSO stock solutionは、どのくらい安定ですか?
-
A
調製後は、-20℃で保存してください。調製後1ヶ月間安定です。
また使用量に応じて小分けし保存することをお勧めします。
-
Q
オートファジーに関連するタンパク質をノックダウンし評価した実績はありますか?
-
A
オートファゴソーム膜形成に関与しているULK1及びULK2をノックダウンした細胞と野生株の細胞を飢餓誘導し、DALGreenにて評価した実績がございます。
評価では、ULK1/ULK2ノックダウン細胞に比べ、野生株ではDALGreenの蛍光が増大している結果が得られています。
本評価データは下記論文のSupporting Information(Fig. S5)をご参照ください。
なお、オートファジーのマーカーであるLC3-RFPとDALGreenを共染色し、殆どのPuncta(斑点)が共局在する結果も得られております。本実験データは、下記論文のFig..1をご参照ください。
H. Iwashita, H. T. Sakurai, N. Nagahora, M. Ishiyama, K. Shioji, K. Sasamoto, K. Okuma, S. Shimizu, and Y. Ueno, "Small fluorescent molecules for monitoring autophagic flux", FEBS Letters., 2018, 592, (4), 559–567.
論文へのリンクは製品HPにございます。
製品HP:DALGreen - Autophagy Detection
-
Q
リソソーム染色試薬との違いはありますか?
-
A
リソソーム染色試薬は、細胞内のリソソームに局在します。一方、DALGreenはオートファゴソームに
局在した後、オートファゴソームとリソソームが融合した際に蛍光が増大します。そのため、リソソーム染色試薬とDLGreenで共染色した場合、リソソーム染色試薬由来の蛍光のうち、オート
リソソームの部分がDALGreenの蛍光と重なります。
本評価データは下記論文のSupporting Information(Fig. S5)をご参照ください。
H. Iwashita, H. T. Sakurai, N. Nagahora, M. Ishiyama, K. Shioji, K. Sasamoto, K. Okuma, S. Shimizu, and Y. Ueno, "Small fluorescent molecules for monitoring autophagic flux", FEBS Letters., 2018, 592, (4), 559–567.
論文へのリンクは製品HPにございます。
製品HP:DALGreen - Autophagy Detection
-
Q
推奨フィルターを教えてください。
-
A
励起フィルター:350~450 nm
蛍光フィルター:500~560 nmなお、共焦点顕微鏡を用いて488 nm励起により蛍光観察した実績がございます。
弊社HP内の製品ページの実験例を参照ください。
-
Q
共染色時の注意点を教えてください。
-
A
本試薬はストークシフトが長い蛍光特性を持ちます。そのため、ご使用の前に本試薬と共染色試薬の蛍光波長を必ずご確認の上、適切な励起・検出波長に設定してください。
-
Q
DALGreenの最適濃度の検討方法を教えてください。
-
A
試薬の特性により、試薬の濃度が高すぎたり低すぎたりすると、オートファジー誘導時と誘導していないコントロールとの差が判りにくい場合があります。
下記の情報を参考に試薬濃度の検討することをお勧めします。細胞種によりDALGreenの最適濃度は異なります。
DALGreenを薄い濃度から(目安0.1 μmol/l)から数点段階的に振ってご検討ください。
(濃い濃度は4 μmol/L前後を目安としてください)(参考)
小社では、HeLa, HepG2、CHO細胞にて、細胞種毎のDALGreenの最適濃度の検討を行いました。
DALGreenを下記濃度で染色し、アミノ酸不含培地にて培養してオートファジーを誘導しました。
その結果、下記の赤字の濃度条件ではコントロールとの誘導時との差が見られました。細胞種 DALGreen 濃度 HeLa 4 µmol/l 2 µmol/l 1 µmol/l 0.5 µmol/l HepG2 4 µmol/l 2 µmol/l 1 µmol/l 0.5 µmol/l CHO 4 µmol/l 2 µmol/l 1 µmol/l 0.5 µmol/l 【HeLa細胞】
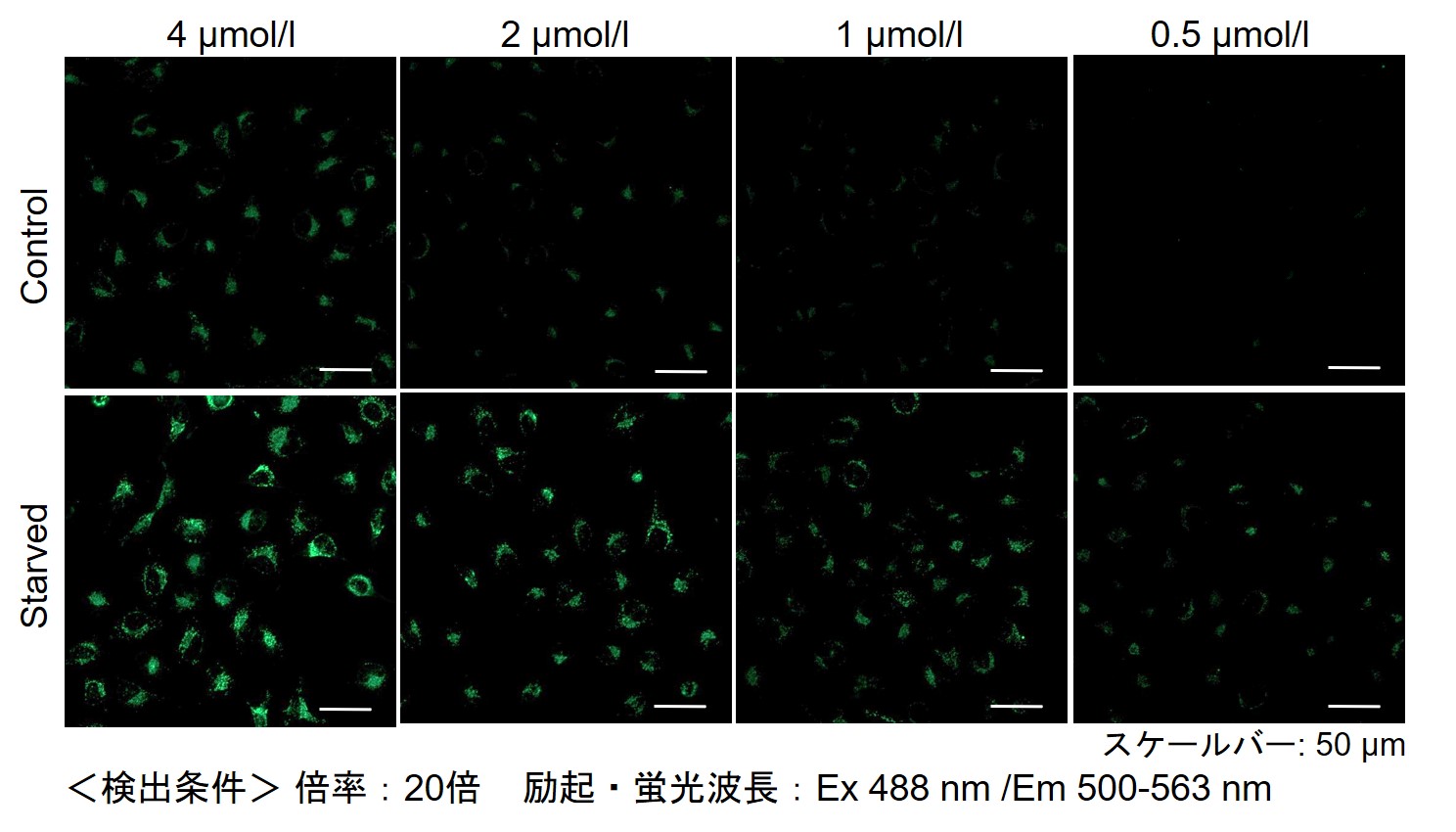
【HepG2細胞】
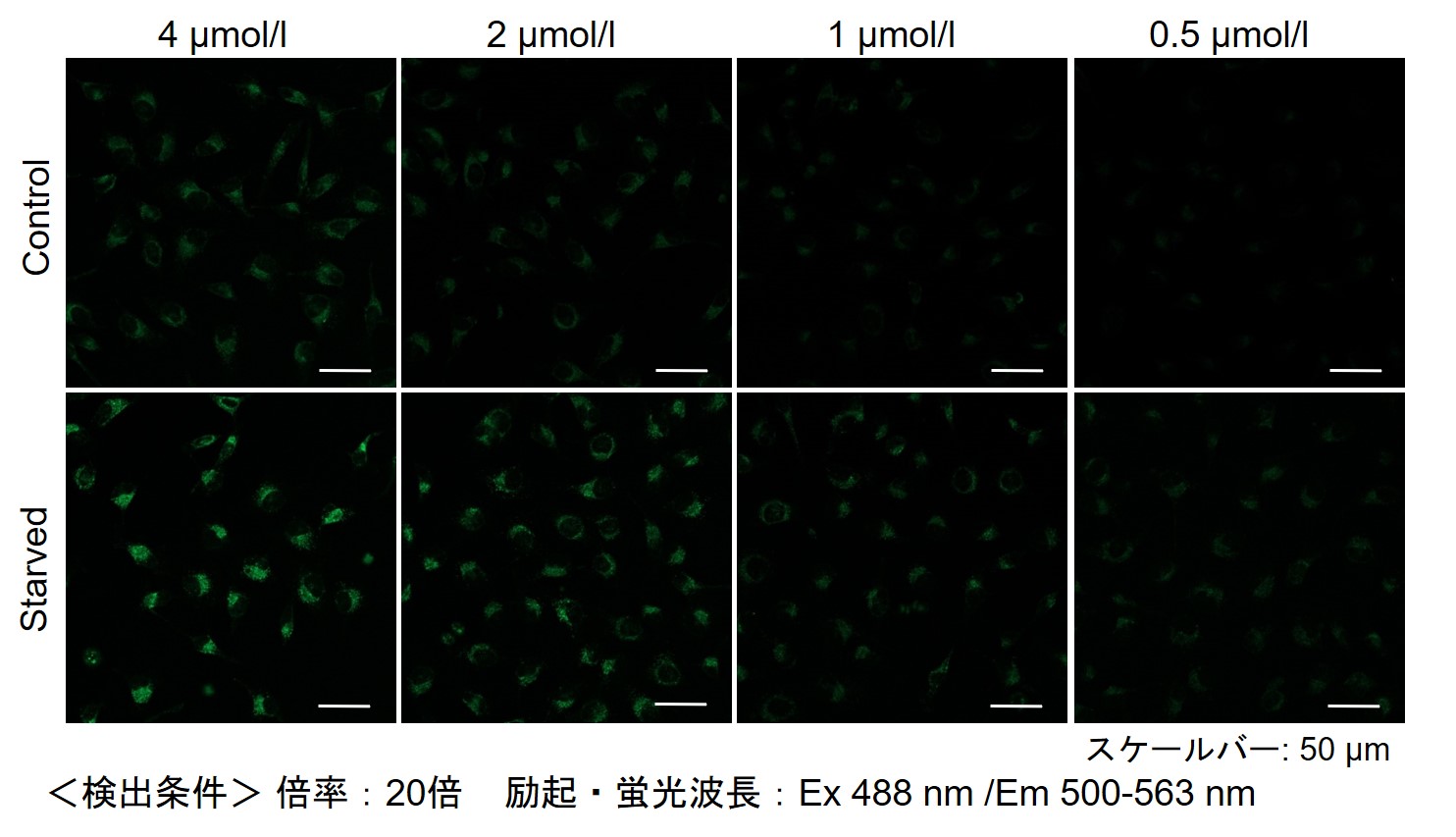
【CHO細胞】
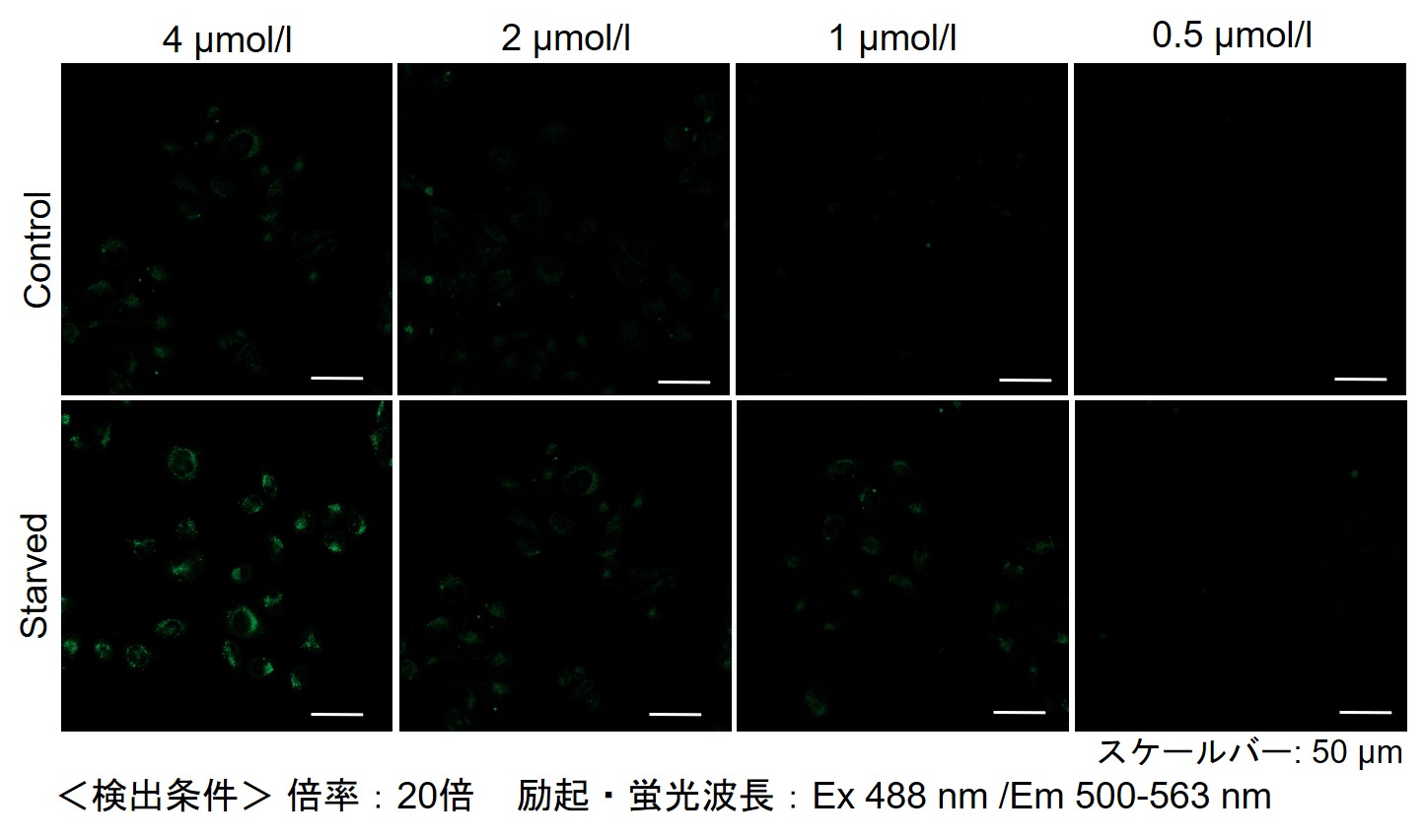
-
Q
タイムラプスイメージングを行う上で注意点はありますか?
-
A
測定条件設定のための予備実験を行ってください。
試薬の特性上、染色直後は初期蛍光値が高くなる傾向があるため、以下の手順を参考に予備実験およびタイムラプスイメージングを行ってください。①予備実験
・コントロール細胞(オートファジーを誘導しない細胞)を用いる。
・取扱説明書に従い、Working soluitonで染色後、培養培地で2回洗浄する。
・通常培地を添加した後、蛍光の時間変化を観察する。
・下図の様に、染色後に細胞内の蛍光が次第に低下した後、蛍光の変化が安定してくる時間(図中 T)を確認する。
※条件は細胞の種類により変わる可能性があります。(参考)
HeLa細胞の場合、染色後の約60分経過すると蛍光強度が安定することを確認しております(DALGreen)。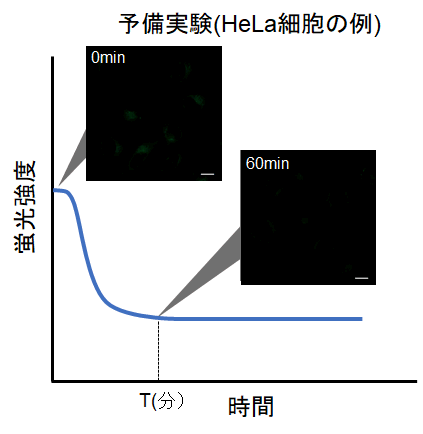
②タイムラプスイメージング
・細胞を Working solutionで染色後、培養培地中で細胞を37℃でインキュベートする。
※予備実験で設定した時間でインキュベートする。
※染色後、直ぐにはオートファジー誘導は行わない。
・インキュベート後にオートファジーの誘導を開始して、タイムラプスイメージングをする。(参考)
HeLa細胞をDALGreenで染色し、通常培地中で60分間(予備実験で設定した時間)培養後、オートファジーを誘導しました。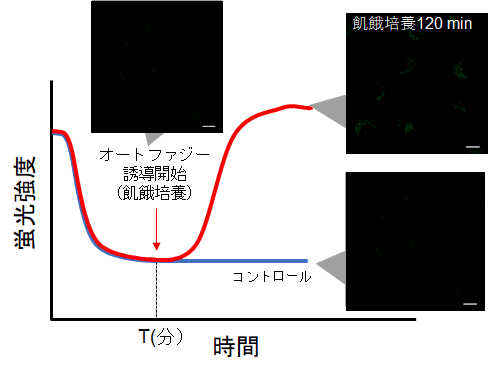
-
Q
オートファジーにはどのような経路があり、DALGreenはどの状態を検出するのですか?
-
A
オートファジーには、Atg5依存的オートファジー(LC3が変化する)とLC3の変化を伴わない、Atg5非依存的オートファジーがあることが知られております*。
DALGreenはオートファゴソーム膜に取り込まれ、その後、リソソームと融合し酸性環境下で蛍光が増大します。
そのため、DALGreenはオートリソソームの状態を検出します。
*参考資料 : 新たなオートファジー機構の発見 清水重臣
▶初めて検出する細胞種や実験系の場合は、よくある問い合わせ【 DALGreenの最適濃度の検討手順】をご参照ください。
-
Q
どのくらいの時間まで蛍光検出できますか?
-
A
染色後72時間まで観察できた実績がございます。