Cell Counting Kit-8®

細胞増殖/細胞毒性アッセイキット
-
製品コードCK04 Cell Counting Kit-8®
| 容 量 | メーカー希望 小売価格 |
富士フイルム 和光純薬 |
|---|---|---|
| 100 回用 | ¥7,100 | 341-07761 |
| 500 回用 | ¥17,600 | 347-07621 |
| 2500 回用 | ¥48,500 | 343-07623 |
| 5000 回用 | ¥90,000 | 341-07624 |
| 10000 回用 | ¥128,400 | 341-08001 |
Cell Counting Kit-8およびCCK-8は、株式会社同仁化学研究所の登録商標です(登録商標第6309021号)
| 100 回用 | 1 ml×1 | |
|---|---|---|
| 500 回用 | 5 ml×1 | |
| 2500 回用 | 5 ml×5 | |
| 5000 回用 | 5 ml×10 | |
| 10000 回用 | 100ml×1 |
性質
Cell Counting Kit-8は細胞増殖または化学物質の感受性試験において、細胞数を測定するキットである。高感度水溶性ホルマザンを生成する新規テトラゾリウム塩WST-8を発色基質として採用することで、従来のCell Counting Kitより高感度測定が可能になった。WST-8は細胞内脱水素酵素により還元され、水溶性のホルマザンを生成する。このホルマザンの450 nmの吸光度を直接測定することにより、容易に生細胞数を計測することができる。細胞数と生成するホルマザンの量は直線的な比例関係にある。1ボトル溶液タイプとし、より使いやすくなった。
特 長
1) [3H]-チミジン取り込み法のようなラジオアイソトープを必要としない。
2) テトラゾリウム塩およびホルマザンとも高水溶性であるため、MTTアッセイのようなホルマザンの溶解操作が不要である。
3) 他の水溶性タイプのテトラゾリウム塩(XTT、MTS)より高感度・低毒性である。
4) 1ボトル溶液タイプであるため、試薬の調製が不要である。
5) 他の測定キットより試薬が安定である。
6) フェノールレッドを含む培地でも使用できる。
「発色基質WSTシリーズ」及び「Cell Counting Kit-8」は小社で開発され、世界中で細胞増殖や細胞毒性試験に利用されています。
細胞死関連製品
| 指標 | 製品名 | 測定対象 | 装置 / 検出波長 |
|---|---|---|---|
| 細胞生存能力 | Cell Counting Kit-8 | 細胞内脱水素 酵素活性 |
プレートリーダー 吸光度 λ= 450nm |
| ネクローシス (細胞毒性) |
Cytotoxicity LDH Assay Kit-WST |
遊離LDH | プレートリーダー 吸光度 λ= 490nm |
| アポトーシス | Annexin V Apoptosis Plate Assay Kit |
ホスファチジルセリン | プレートリーダー 蛍光 Ex: 488 nm / Em: 525 nm |
| フェロトーシス | FerroOrange | 細胞内 鉄イオン(Fe2+) |
蛍光顕微鏡, FCM, プレートリーダー 蛍光 Ex: 543 nm / Em: 580 nm |
| フェロトーシス | Lyso-FerroRed | リソソーム内 鉄イオン(Fe2+) |
蛍光顕微鏡, FCM, プレートリーダー 蛍光 Ex: 551 nm / Em: 571 nm |
| フェロトーシス | Mito-FerroGreen | ミトコンドリア内 鉄イオン(Fe2+) |
蛍光顕微鏡 蛍光 Ex: 505 nm / Em: 535 nm |
| フェロトーシス | Liperfluo | 脂質過酸化 | 蛍光顕微鏡, FCM 蛍光 Ex: 488 nm / Em: 500-550 nm |
| フェロトーシス | Iron Assay Kit -Colorimetric- |
組織内鉄イオン (Fe2+, Fe3+) |
プレートリーダー 吸光度 λ= 593nm |
技術情報
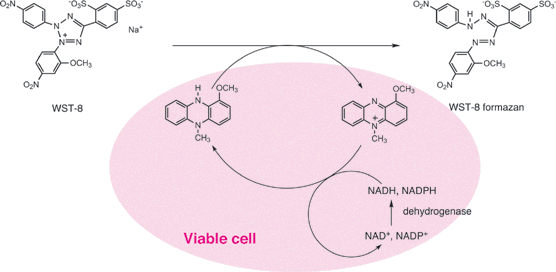
測定原理
Cell Counting Kit-8にはテトラゾリウム塩(WST-8)と電子伝達物質(1-Methoxy PMS)が含まれている。WST-8は、高い水溶性を有するため生細胞膜を透過せず細胞外に存在し、乳酸脱水素酵素の補酵素であるNADHから1-Methoxy PMSを介して電子を受け取ることで還元されて水溶性のWST-8ホルマザン(極大吸収波長450 nm: 下記の吸収スペクトル参照)を生成する。
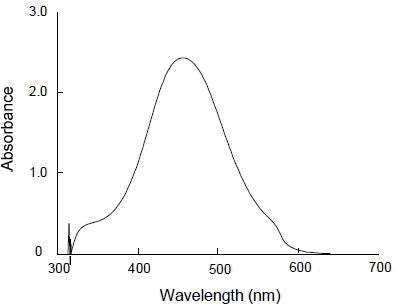
WST-8ホルマザンの吸収スペクトル
測定手順
簡便な測定手順に加えて、必要な試薬を含む1ボトル溶液タイプのため、Working solutionなどの試薬調製が不要で更に時間を節約することができる。
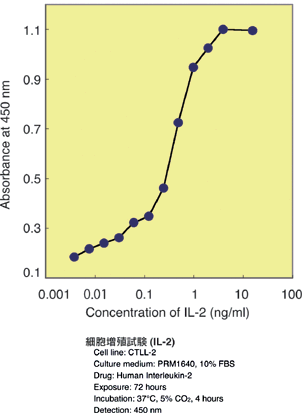
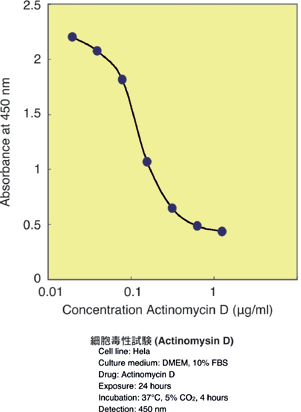
Cell Counting Kit-8を用いた測定例
|
細胞増殖試験(左)と細胞毒性試験(右) |
|
 |
 |
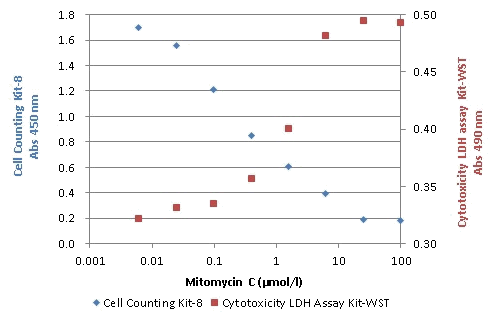
Cell Counting Kit-8 とCytotoxicity LDH Assay Kit-WST を併用した細胞毒性試験
試験物質: Mitomycin C
細胞: HeLa
使用培地: MEM, 10% FBS
インキュベート: 37℃, 5% CO2, 48時間
検出波長: Cell Counting Kit-8 (450 nm), Cytotoxicity LDH Assay Kit-WST (490 nm)
HeLa 細胞にMitomycin C を添加した際の細胞毒性をCell Counting Kit-8とCytotoxicity LDH Assay Kit-WST [Code: CK12]を用いて測定した。Cell Counting Kit-8による細胞内代謝活性を指標とした方法とCytotoxicity LDH Assay Kit-WSTを用いた細胞膜損傷による遊離LDHを指標とした方法では各々の指標が異なるため、細胞毒性が表れる薬剤濃度に違いがあることが確認された。
論文には別指標(遊離LDH法など)の毒性データが望まれています。 [関連記事]
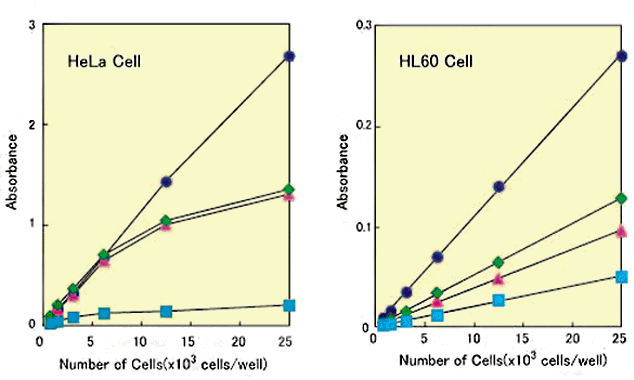
細胞数とWST-8ホルマザン由来の吸光度の関係
Medium: MEM, 10%FBS(HeLa ) , RPM1640(HL60)
Incubation: 37℃, 5%CO2, 2hr (HeLa、HL60)
Detection: Cell Counting Kit-8
(●) 450 nm, XTT (◆) 450 nm, MTS
(▲) 490 nm, MTT(■) 570 nm
HeLa細胞およびHL60細胞を種々の細胞数で96ウェルプレートに播種し、各試薬を添加してインキュベート後の吸光度を測定した。細胞数に応じて吸光度が増加すること、また、細胞の種類によって吸光度の値に違いがあることが確認された。
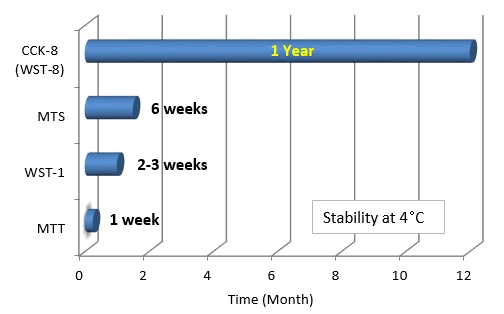
試薬の安定性比較
Cell Counting Kit-8は、冷蔵保存で1年間安定であるため、無駄を減らすことができる。
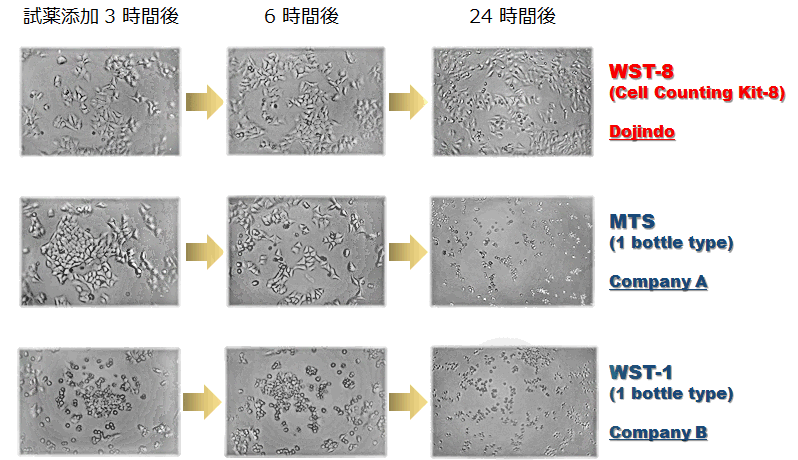
試薬の細胞毒性比較
96ウェルプレートにHeLa細胞を播種(5,000 cells/well)して前培養した後、各試薬溶液を添加した。CO2インキュベーター内で呈色反応を開始して、3, 6, 24時間毎に顕微鏡を用いて細胞の形態を観察した。Cell Counting Kit-8は24時間後も殆どの細胞の形態に変化は認められなかった。薬剤等を用いた細胞毒性試験において、測定試薬自身が細胞毒性に与える影響が極めて低い試薬を選択することが望ましい。
3次元培養モデルの毒性試験ガイドライン
Cell Counting Kit-8(WST-8法)がOECD TG492の3次元培養モデル(角膜)の毒性試験用ガイドラインに掲載されました。
詳細はリンクよりご覧ください。
参考文献
1) M. Ishiyama, Y. Miyazono, K. Sasamoto, Y. Ohkura and K. Ueno, "A Highly Water-Soluble Disulfonated Tetrazolium Salt as a Chromogenic Indicator for NADH as Well as Cell Viability", Talanta., 1997, 44, 1299.
2) H. Tominaga, M. Ishiyama, F. Ohseto, K. Sasamoto, T. Hamamoto, K. Suzuki and M. Watanabe, "A water-soluble tetrazolium salt useful for colorimetric cell viability assay", Anal. Commun., 1999, 36, 47.
3) T. Miyamoto, W. Min and H. S. Lillehoj, "Lymphocyte Proliferation Response During Eimeria tenella Infection Assessed by a New, Reliable, Nonradioactive Colorimetric Assay", Avian Dis., 2002, 46, 10.
4) K. Yoshimura, A. Tanimoto, T. Abe, M. Ogawa, T. Yutsudo, M. Kashimura and S. Yoshida, "Shiga toxin 1 and 2 Induce Apoptosis in the Amniotic cell line WISH", J. Soc. Gynecol. Investig., 2002, 9, 22.
5) Y. Hayakawa, Y. Hirata, H. Nakagawa, K. Sakamoto, Y. Hikiba, H. Kinoshita, W. Nakata, R. Takahashi, K. Tateishi, M. Tada, M. Akanuma, H. Yoshida, K. Takeda, H. Ichijo, M. Omata, S. Maeda and K. Koike, "Apoptosis signal-regulating kinase 1 and cyclin D1 compose a positive feedback loop contributing to tumor growth in gastric cancer", Proc. Natl. Acad. Sci. U.S.A., 2011, 108, (2), 780.
6) R. Chugh, V. Sangwan, S. P. Patil, V. Dudeja, R. K. Dawra, S. Banerjee, R. J. Schumacher, B. R. Blazar, G. I. Georg, S. M. Vickers and A. K. Saluja, "A Preclinical Evaluation of Minnelide as a Therapeutic Agent Against Pancreatic Cancer", Sci. Transl. Med., 2012, 4, (156), 156ra139.
7) R. Kang, T. Loux, D. Tang, N. E. Schapiro, P. Vernon, K. M. Livesey, A. Krasinskas, M. T. Lotze and H. J. Zeh III, "The expression of the receptor for advanced glycation endproducts (RAGE) is permissive for early pancreatic neoplasia", Proc. Natl. Acad. Sci. U.S.A., 2012, 109, (18), 7031.
8) Y. Matsuo, J H Park, T. Miyamoto, S. Yamamoto, S. Hisada, H. Alachkar and Y. Nakamura, "TOPK inhibitor induces complete tumor regression in xenograft models of human cancer through inhibition of cytokinesis", Sci. Transl. Med., 2014, 6, (259), 259ra145.
9) K. Takayam, Y. Morisaki, S. Kuno, Y. Nagamoto, K. Harada, N. Furukawa, M. Ohtaka, K. Nishimura, K. Imagawa, F. Sakurai, M. Tachibana, R. Sumazaki, E. Noguchi, M. Nakanishi, K. Hirata, K. Kawabata and H. Mizuguchi, "Prediction of interindividual differences in hepatic functions and drug sensitivity by using human iPS-derived hepatocytes", Proc. Natl. Acad. Sci. U.S.A., 2014, 111, (47), 16772.
10) T. Ida, T. Sawa, H. Ihara, Y. Tsuchiya, Y. Watanabe, Y. Kumagai, M. Suematsu, H. Motohashi, S. Fujii, T. Matsunaga, M. Yamamoto, K. Ono, N. O. Devarie-Baez, M. Xian, J. M. Fukuto and Takaaki Akaike, "Reactive cysteine persulfides and S-polythiolation regulate oxidative stress and redox signaling", Proc. Natl. Acad. Sci. U.S.A., 2014, 111, (21), 7606.
11) K. Palumbo-Zerr, P. Zerr, A. Distler, J. Fliehr, R. Mancuso, J. Huang, D. Mielenz, M. Tomcik, B. G Furnrohr, C. Scholtysek, C. Dees, C. Beyer, G. Kronke, D. Metzger, O. Distler, G. Schett and J. H W Distler, Orphan nuclear receptor NR4A1 regulates transforming growth factor-β signaling and fibrosis", Nat. Med., 2015, 21, (2), 150.
12) T. Tu, C. Zhang, H. Yan, Y. Luo, R. Kong, P. Wen, Z. Ye, J. Chen, J. Feng, F. Liu, J. Y Wu and X. Yan, "CD146 acts as a novel receptor for netrin-1 in promoting angiogenesis and vascular development", Cell Res., 2015, 25, (3), 275.
13) S. Ji, Y. Qin, S. Shi, X. Liu, H. Hu, H. Zhou, J. Gao, B. Zhang, W. Xu, J. Liu, D. Liang, L. Liu, C. Liu, J. Long, H. Zhou, P J Chiao, J. Xu, Q. Ni, D. Gao and X. Yu, "ERK kinase phosphorylates and destabilizes the tumor suppressor FBW7 in pancreatic cancer", Cell Res., 2015, 25, (5), 561.
14) N. Li, W. Zhang, M. Khan, L. Lin, JM. Lin, "MoS2-LA-PEI nanocomposite carrier for real-time imaging of ATP metabolism in glioma stem cells co-cultured with endothelial cells on a microfluidic system", Biosens Bioelectron., 2017, 99, (2018), 142.
15) R. Watanabe, T. Kurose, Y. Morishige and K. Fujimori, "Protective Effects of Fisetin Against 6-OHDA-Induced Apoptosis by Activation of PI3K-Akt Signaling in Human Neuroblastoma SH-SY5Y Cells.", Neurochem. Res.., 2018, 43, (2), 488-499.
16) Y. Xu, C. Huang, M. Liu, N. Chen, W. Chen, C. Yang, Y. Zhao, X. Li, J. Duan, S. Liu and S. Yang, "Survivin regulated by autophagy mediates hyperglycemia-induced vascular endothelial cell dysfunction", Exp. Cell Res.., 2018,doi: 10.1016/j.yexcr.2018.01.037 .
17) E. E. Mon, F. Y. Wei, R. N. R. Ahmad, T. Yamamoto, T. Moroishi and K. Tomizawa, "Regulation of mitochondrial iron homeostasis by siderofexin 2 ", J Physiol Sci.,2018,doi:10.1007/s12576-018-0652-2.
よくある質問
-
Q
カタログや説明書には96 wellプレートでの測定例が示してありますが、 24 wellや12 wellのプレートで測定を行うことができますか? その場合には試薬(Cell Counting Kit)の添加量はどのようにすれば良いでしょうか?
-
A
96wellプレート以外でも測定できます。
試薬の添加量は使用培地の10分の1を目安にして下さい。
(1 mLであれば試薬を100 μL など)細胞数などにより、試薬の添加量を少なくして測定できる可能性もありますが、最初は10分の1量を目安として検討されることをお勧めします。
-
Q
Cell Counting Kit-8とCell Counting Kit-Fの違いは何ですか?
-
A
Cell Counting Kit-8は細胞内酵素活性を指標とし、比色測定を行います。
【Cell Counting Kit-8】
色素:WST-8
形態:1ボトル
Cell Counting Kit-Fは蛍光での測定となります。
細胞内エステラーゼ活性を指標に蛍光測定を行います。
比色法よりも少ない細胞数から測定出来ます。(50 cells/well 以上)【Cell Counting Kit-F】
色素:Calcein-AM
形態:1ボトル
-
Q
Cell Counting Kit-8とMTTの違いは何でしょうか?
-
A
細胞の酵素により、テトラゾリウムがホルマザンになるというのは共通したところです。
それぞれの違いとしては【Cell Counting Kit-8】
生成するホルマザンが水溶性である。(溶解操作が不要)
測定波長:400~450 nm
細胞全体の酵素活性を反映している。
生成するホルマザンは細胞毒性がない。
細胞が生きたまま測定できる。【MTT】
生成するホルマザンが非水溶性である。(有機溶媒等による溶解が必要)
測定波長:550~600 nm
主にミトコンドリアの酵素活性を反映している。
生成するホルマザンが細胞毒性を示す。
細胞を溶かさないと測定できない。有機溶媒によるホルマザン溶解が必要な分、MTTの方が操作が煩雑になります。
-
Q
ブランク試験を行うとしたらどのような条件で吸光度を測定すればよいでしょうか? (細胞単独、細胞+培地、培地のみ、いずれも無し etc.)
-
A
ブランクとして確認するのは3種類の考え方があります。
①細胞+培地にて600 nm以上で測定する。
→細胞を含む培地の測定試料に濁りがある場合に測定します。
濁りによる散乱が測定誤差となるためで、全波長領域で高くなります。試薬の吸収がない600 nm以上で測定します。しかし、濁りがない、殆ど無視できる程度の濁りであれば、測定する必要はありません。②細胞+培地にて450 nm(測定波長)を測定する。
→細胞を含む培地の測定試料に試薬の発色と同じ吸収がある場合に測定します。
450 nmの吸収ですので、試料の着色で判断できます。着色がなければ必要はありません。③培地+試薬(CCK)にて450 nm(測定波長)を測定する。
→細胞を含まない培地に試薬を添加した場合の吸収を測定するもので、一般的な試薬ブランクです。
培地に還元性物質が含まれると、試薬が発色します。そのような発色がないことを確認します。
発色が僅かであれば、ブランクとして差し引いてもよいです。しかし、発色が強いようであれば培地中の還元物質を除くか、別の培地をご検討下さい。
また、薬物添加試験を行われるのであれば、添加する薬物で発色しないかを確認してください。*ブランクとして大きく出てくるのは②の培地に着色がある場合と③の試薬の誤発色です。
これらをご確認ください。
-
Q
前培養をするように取扱説明書に指示されていますが、これは必要なものですか?
-
A
付着細胞では前培養を推奨しております。
トリプシン処理等により培養用フラスコから回収する際に、細胞はダメージを受けます。
そのため、対数増殖期の状態にために細胞の前培養が必要になります。浮遊細胞の場合は省略しても構いません。
-
Q
Cell Counting Kit-8の発色に阻害を与えるような物質はなんですか?
-
A
一般的に還元物質(アスコルビン酸など)が共存していると正誤差が生じます。
フェノールレッドや血清は問題ありません。
フェノールレッドの場合、若干(5%程度)のブランク上昇がみられますが、使用上は問題ありません。しかし、発色に阻害を与える培地成分が含まれているかもしれませんので、ご使用の培地が誤発色を与えないかご確認の上、ご使用ください。(薬剤も同様です)
また薬剤によっては細胞の機能に影響を与えるものがあるようで、細胞の増殖能は止まっていても酵素活性を働かせたりしていると(タンパク合成を行なったり)発色を起こしたりします。
負誤差の要因としては、特にこの物質が影響があるといわれているものはないのですが、上記と逆で、薬剤により影響を受け、実際には増殖しているのに発色が低く出る
という現象が起ることはあるようです。また、酸化剤も発色を阻害し負誤差を与える要因となることがあります。
-
Q
細胞数は変わらないのに吸光度が上昇します。どのような要因が考えられますか。
-
A
以下の要因が考えられます。
(1)還元物質の影響
(2)細胞当たりの代謝活性の変化詳細は下記をご確認下さい。
----------------------------------------------------------------------------------------------------------------------------------------
(1)還元物質の影響について試料や被験物質に還元性を持つ物質が存在する場合、Cell Counting Kit-8に含まれるWST-8を直接還元し誤発色することがあります。
細胞が無い系で、Cell Counting Kit-8を添加し、発色の有無を予めご確認ください。
発色する場合は、Cell Counting Kit-8を添加する前に培地交換を行ってください。その他発色に影響を与える因子については、
よくある質問「Cell Counting Kit-8の発色に阻害を与えるような物質はなんですか?」をご確認ください。
----------------------------------------------------------------------------------------------------------------------------------------
(2)細胞当たりの代謝活性の変化について細胞当たりの代謝活性が上昇した場合、細胞数が変わらなくても、吸光度が上昇することがあります。
Cell Counting Kit-8は生細胞の脱水素酵素の活性を指標としています。
そのため、細胞数の変化がなくても、細胞の代謝活性が変化した場合に吸光度が変化する可能性があります。細胞の代謝活性の変化の有無は、別の指標で生細胞を測定*1したり、細胞の代謝産物*2を確認することで
複合的に評価される場合があります。下記リンク先の資料もご参考ください。*2:細胞内代謝測定
----------------------------------------------------------------------------------------------------------------------------------------
ご不明点がありましたら、小社カスタマーサポートまでお問合せください。
(free dial:0120-489548 / E-mail:info@dojindo.co.jp)
-
Q
呈色反応を途中で止めたい(測定までに時間が空く)のですが、どうすれば反応を止められますか?
-
A
Cell Counting Kitの発色機構は細胞内に存在する脱水素酵素に依存しているので、
呈色反応を止めるには、この酵素反応を止める為に細胞を死滅させます。下記のいずれかの方法で反応停止を行ってください(添加量は96wellの場合)
反応停止後は24時間以内に測定して下さい。(1)1 w/v% SDSを10 μL添加する。
*SDSを添加する場合には、泡立たないように注意して下さい。
表面に泡があると光散乱して吸光度が高くなります。
(2)0.1 mol/ HClを10 μL添加する。
*もし、緩衝能の高い培地をご使用の場合には、もっと濃い酸を添加してください。
アルカリ溶液による反応停止では定量が出来ません。
反応液をアルカリ性にすると、生成したホルマザン色素が青変し、定量性が失われます。
-
Q
450 nm 以外のフィルターは使用できますか?
-
A
430-490 nm のフィルターが使用できますが、450 nm のフィルターをご使用いただきますと最も高感度に測定できます。
参考)WST-8ホルマザンの吸収スペクトル
-
Q
Cell Counting Kit-8の保存期間を教えてください。
-
A
キット溶液は4℃で12ヶ月安定です。遮光して冷蔵にて保管してください。
長期保存の際は、遮光し-20℃で保存してください。
凍結-融解操作はなるべく行わないで下さい。
*容器をプラスチック容器に変更いたしました。(以前はガラス容器)それに伴い、安定性試験を再度行い冷蔵での長期安定性が確認出来ましたので保管条件を変更しております。
-
Q
溶液の中に沈殿が見えるのですが性能に影響はありますか。
-
A
稀に沈殿物が見られることがあります。この場合、加温(最大37℃)することで析出物は再溶解します。完溶した場合は、そのままご使用いただけます。
もし加温操作でも溶解しない場合は、弊社までお問い合わせください。
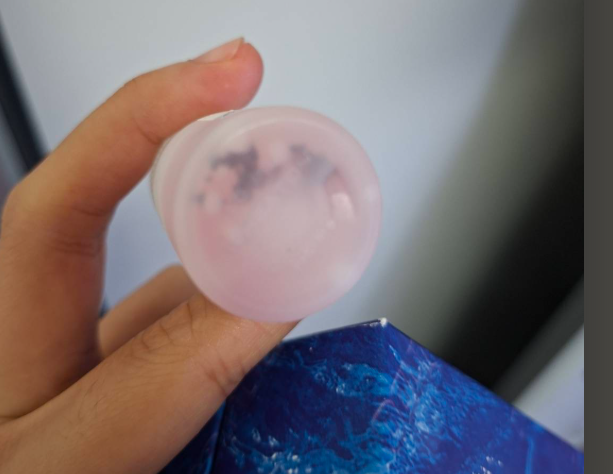
沈殿物の例
取扱条件
| 保存条件: 冷蔵,遮光 |