ExoSparkler Exosome Membrane Labeling Kit-Green
エクソソーム 膜蛍光染色キット Green
- 細胞外で凝集せず、より正確な動態を観察できる
- 本キットだけで蛍光標識から精製まで可能
-
製品コードEX01 ExoSparkler Exosome Membrane Labeling Kit-Green
| 容 量 | メーカー希望 小売価格 |
富士フイルム 和光純薬 |
|---|---|---|
| 5 samples | ¥31,800 | 343-09661 |
精製済エクソソームを染色することができます。
| 5 samples | ・Mem Dye-Green ・Filtration tube |
×1 ×5 |
|---|
ラベル化エクソソームの利用
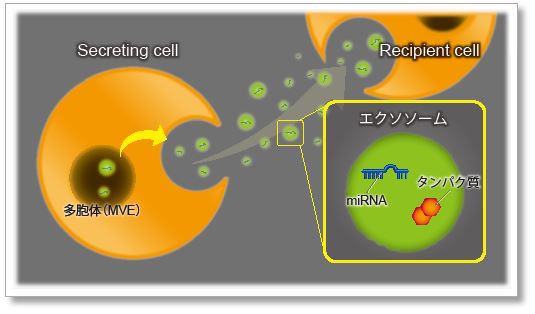
近年、細胞から分泌される細胞外小胞(Extracellular vesicle ;EV)の一種であるエクソソームが、がんの悪性化や転移に促進的に寄与することが明らかとなり注目を集めています。
エクソソームによる細胞間コミュニケーションを解析するためには、細胞への取り込みをモニタリングする技術が重要であり、細胞外小胞の脂質二重膜やタンパク質を蛍光色素で染色する技術が汎用されています。
ExoSparkler シリーズは、精製されたエクソソームの膜またはタンパク質を染色し、細胞に取り込まれるエクソソームをイメージングすることができます。
マニュアル
技術情報
より正確にエクソソームの動態を観察する
エクソソームの膜を染色するためによく用いられている膜染色色素(S 社 製品P)には、色素自体が凝集を起こし、エクソソームに由来しない蛍光起点が生じたり、エクソソームの性質変化やバックグラウンドの上昇などを招く課題が挙げられています1), 2)。
ExoSparkler シリーズで用いている色素(Mem Dye-Green, Red, Deep Red)は凝集を起こさず、エクソソームの性質にもほとんど影響を及ぼさないため、より正確にエクソソームの動態を観察することが可能です。
| 参考文献 | |
| 1) | Mehdi Dehghani et al., “Exosome labeling by lipophilic dye PKH26 results in significant increase in vesicle size”.bioRxiv., 2019, doi:10.1101/532028. |
| 2) | Pužar Dominkuš P et al., “PKH26 labeling of extracellular vesicles: Characterization and cellular internalization of contaminating PKH26 nanoparticles.” Biochim Biophys Acta Biomembr., 2018, doi: 10.1016/j.bbamem.2018.03.013. |
技術や使用製品に関する補足
|
技術情報のデータは京都大学大学院工学研究科高分子化学専攻 秋吉一成先生のご支援のもと取得いたしました。 |
-

細胞外小胞、エクソソームの特性と機能
小社季刊冊子「DojinNews vol.169」に執筆いただいた記事を掲載しています。
色素が細胞外で凝集しない
Mem Dye-Deep Red または製品P(緑または赤)で染色したエクソソームをHeLa 細胞へ添加し、細胞内に取り込まれるエクソソームを蛍光顕微鏡で観察しました。
その結果、製品P(緑または赤)で染色したエクソソームにおいては、色素の凝集が疑われる細胞外の蛍光輝点が確認されました。

|
また、Mem Dye-Deep Red または製品P(緑または赤)の色素溶液をNTA(ナノ粒子トラッキング解析)で確認した結果、Mem Dye-Deep Red では色素の凝集物が確認できなかったのに対して、製品P(緑または赤)では色素の凝集が疑われる100-500 nmの粒子が観察されました。
※測定装置:LM10-HSBFT 14 (Nanosight社製)
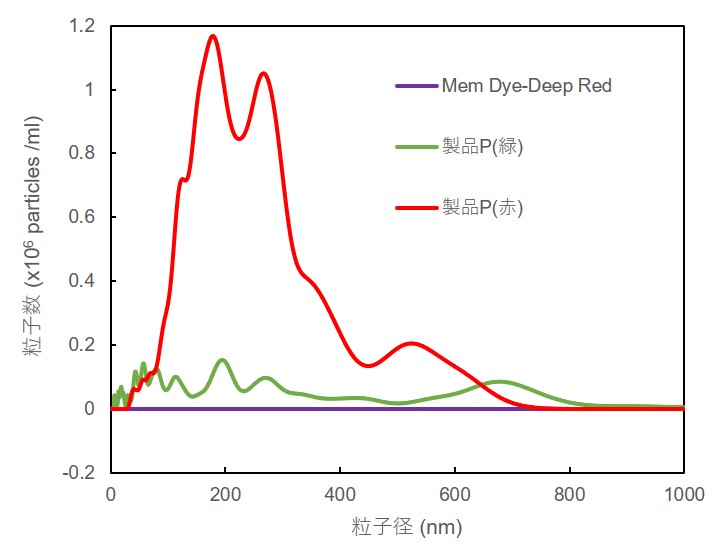 Mem-Dye溶液ならびに製品P溶液の粒子径変化 |
なお、Mem Dye-Green, Red においても、Mem Dye-Deep Red と同様に色素の凝集は確認されませんでした。
エクソソームの性質にほとんど影響しない
Mem Dye-Deep Red または製品P(緑または赤)で染色する前後のエクソソームについて、NTA(ナノ粒子トラッキング解析)とゼータ電位を測定することで、染色によるエクソソームの変化を確認しました。
その結果、Mem-Dyeシリーズ(Green、Red、Deep Red)は、エクソソームの性質にほとんど影響を及ぼさないことが確認されました。
エクソソームの粒子径に対する影響
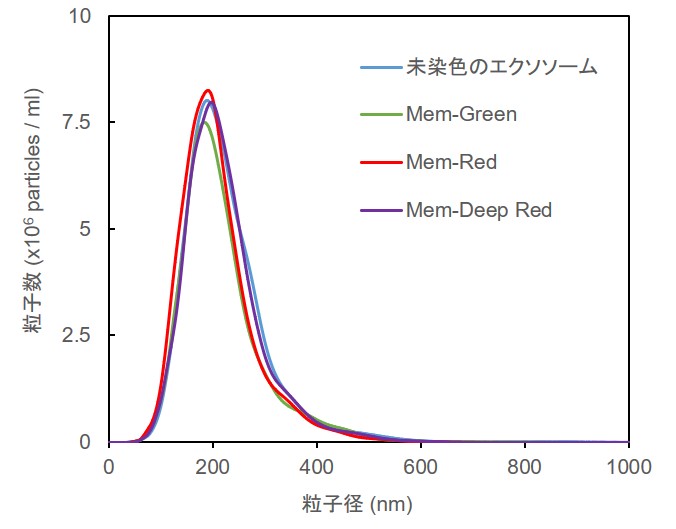
Mem-Dyeシリーズ(Green、Red、Deep Red)ならびに製品P(緑、赤)の各10 µmol/l DMSO溶液を調製し、10 ug(タンパク質量として) のエクソソームを染色後にNTA(ナノ粒子トラッキング解析)を行いました。
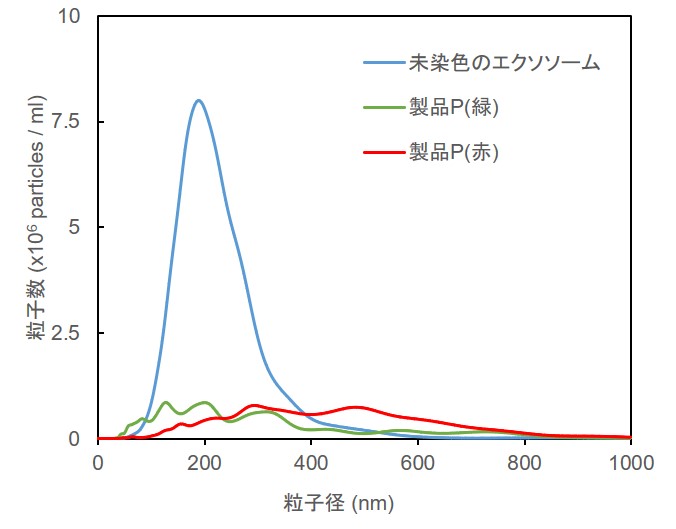
結果としてMem-Dyeシリーズで染色したエクソソームは未染色のエクソソームに対して、粒子数ならびに粒子径への影響がほとんど見られませんでしたが(下図左)、製品Pによる染色前後では粒子数と粒子径に顕著な変化がみられました(下図右)。
※測定装置:LM10-HSBFT 14 (Nanosight社製)
|
エクソソームの膜電位に対する影響
Mem-Dyeシリーズ(Green、Red、Deep Red)ならびに製品P(緑、赤)の各10 µmol/l DMSO溶液を調製し、10 ug(タンパク質量として) のエクソソームを染色後にゼータ電位を測定しました。
結果として、Mem-Dyeシリーズで染色したことによるゼータ電位の変化は、製品Pで染色した場合と比較して小さくなることを確認しました。
※測定装置:Zetasizer Nano ZSP (Malvern Panalytical社製)
Mem-Dyeシリーズならびに製品Pによる染色前後のゼータ電位比較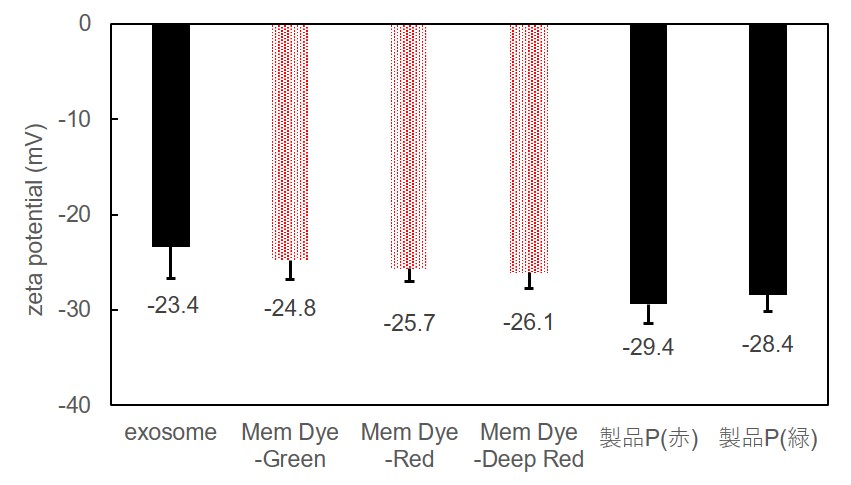 |
参考文献) T. Shimomura, R. Seino, K. Umezaki, A. Shimoda, T. Ezoe, M. Ishiyama, and K. Akiyoshi., "New Lipophilic Fluorescent Dyes for Labeling Extracellular Vesicles: Characterization and Monitoring of Cellular Uptake", BIOCONJUGATE CHEM., 2021, doi:10.1021/acs.bioconjchem.1c00068.
ExoSparklerと既存試薬 におけるEVs染色陽性率の比較
ExoSparkler DeepRed および製品 P を用いて、CD9–sfGFP を発現する ES-2 卵巣がん細胞株由来 EVs の染色を行い、ナノフローサイトメーター CytoFLEX nano*(ベックマン・コールター社)により測定しました。
GFP 陽性 EVs に対する各製品の染色陽性率を算出したところ、ExoSparkler では 99.6%、製品 P では 87.6% の染色陽性率を示しました。
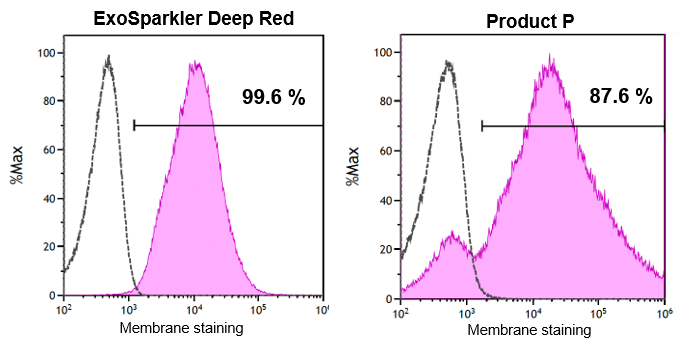
データ提供:東京医科大学 医学総合研究所 分子細胞治療研究部門 吉岡祐亮 先生
*使用装置: ナノフローサイトメーター CytoFLEX nano(ベックマン・コールター社)
各種EVsにおけるExoSparkler による染色効率の評価
ExoSparkler DeepRedを用いて由来の異なる様々なEVを染色し、ナノフローサイトメーター CytoFLEX nano*で測定しましました。
この結果、検討した全てのサンプルにおいて90%以上の高い染色効率が得られました。また、EVsの種類による染色性の違いもほとんど見られませんでした。
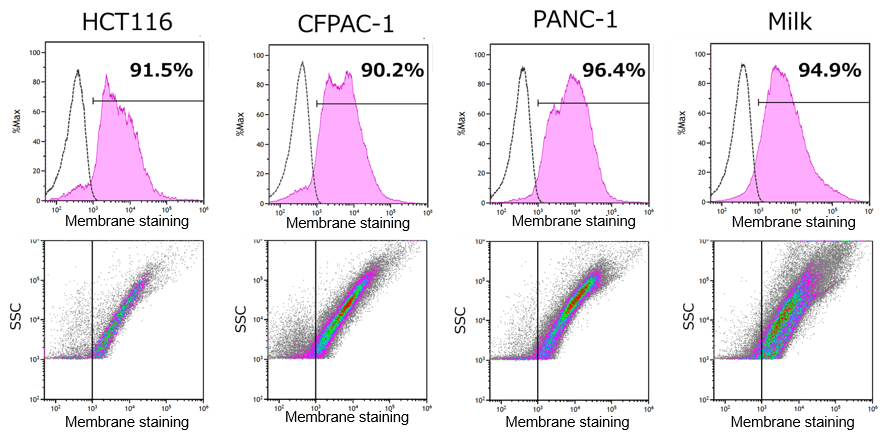
データ提供:東京医科大学 医学総合研究所 分子細胞治療研究部門 吉岡祐亮 先生
*使用装置: ナノフローサイトメーター CytoFLEX nano(ベックマン・コールター社)
このキットだけで蛍光標識から精製まで
ExoSparkler シリーズは、エクソソームの標識に最適化したプロトコルに加え、蛍光標識後の未反応色素を除去できるフィルトレーションチューブを同梱しているため、簡単な操作で蛍光標識エクソソームを調製できます。
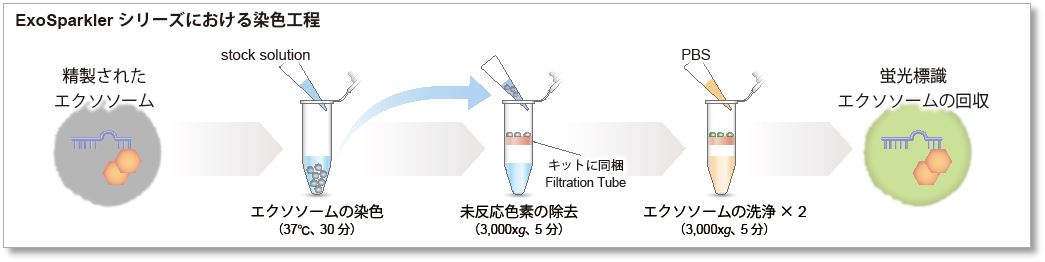 |
精製手法(未反応色素の除去)の比較
ExoSparklarシリーズで未反応色素の除去に使用しているフィルトレーションチューブは、同用途で従来から用いられているゲルろ過法と比較して、高い回収率でエクソソームを精製することが可能です。
| 回収率※ | |
| フィルトレーションチューブ(本キット) | 50% 程度 |
| ゲルろ過法 | 10% 程度 |
| ※ 小社での実施例:精製前後のエクソソーム粒子数をNTA(ナノ粒子トラッキング解析)で比較 | |
フィルトレーションチューブを用いた精製の有効性については、よくある質問:標識後の精製操作でフィルターは着色していますが、未反応の色素は分離できていますか?に掲載しています。
実験例:マクロファージ細胞へのエクソソーム取り込み
ヒト歯肉組織由来間葉系幹細胞(GMSC)由来エクソソームをMagCapture™ エクソソームアイソレーションキット PS(富士フイルム和光純薬株式会社)を用いて精製し、ExoSparkler Exosome Membrane Labeling Kit-Greenで染色しました。その後、ヒト末梢血単核細胞(PBMC)から分化したヒトマクロファージ細胞に添加し、PlasMem Bright Red (コード:P505)でマクロファージ細胞を染色しました。
(九州大学病院 口腔機能修復科 福田隆男 先生よりご提供)
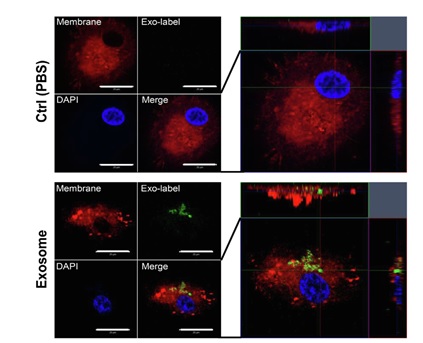
<測定条件>
エクソソーム(Mem Dye - Green、緑):Ex 488 nm / Em 490 - 540 nm
細胞膜(PlasMem Bright Red、赤): Ex. 561 nm / Em. 560 - 700 nm
核(DAPI、青):Ex. 345 nm / Em. 455 nm
<実験操作>
1. 24 well plateに乗せたPLLコートスライドグラス上でPBMC-Mfの分化を誘導(7days)
2. エクソソーム10 µgをExoSparkler Exosome Membrane Labeling Kit-Greenのプロトコールに従い染色
3. 24 well plateにエクソソーム1 µg/mL添加し、3h培養
4. PBSで1回洗浄
5. 培地で調整したPlasMem Bright Red(1/100希釈)を添加し、CO2インキュベーター内で15分静置
6. PBSで3回洗浄
7. 4% PFAを用いて室温、15分間固定
8. PBSで3回洗浄
9. DAPI含有マウント剤(Invitrogen社:ProLong™ Gold Antifade Mountant with DAPI)で封入
10. 共焦点顕微鏡LSM 700 confocal microscope (Carl Zeiss) で撮影
豊富なラインナップ
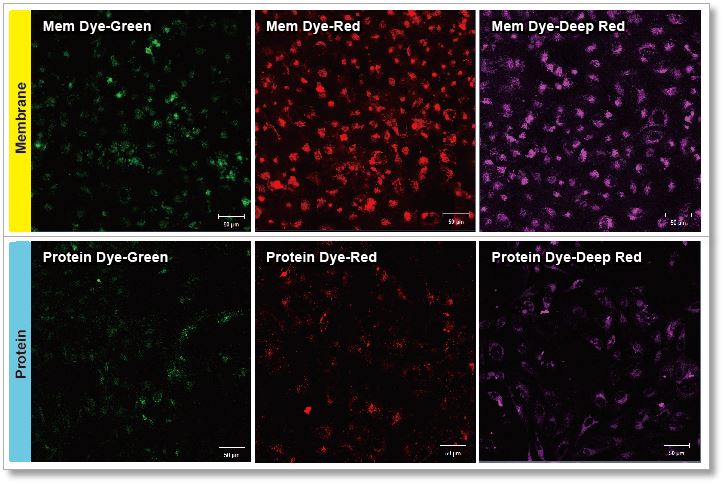
|
| 製品名 | 容量 | 製品コード |
| エクソソーム 膜蛍光染色キット | ||
| ExoSparkler Exosome Membrane Labeling Kit-Green | 5 samples※ | EX01 |
| ExoSparkler Exosome Membrane Labeling Kit-Red | 5 samples※ | EX02 |
| ExoSparkler Exosome Membrane Labeling Kit-Deep Red | 5 samples※ | EX03 |
| エクソソーム タンパク質蛍光染色キット | ||
| ExoSparkler Exosome Protein Labeling Kit-Green | 5 samples※ | EX04 |
| ExoSparkler Exosome Protein Labeling Kit-Red | 5 samples※ | EX05 |
| ExoSparkler Exosome Protein Labeling Kit-Deep Red | 5 samples※ | EX06 |
| ※ 精製済エクソソーム(超遠心法)として、タンパク質:1-10 μg/sample、粒子数:10-100×108 個/sample | ||
参考文献
| 文献No. | 対象サンプル | 装置 | 引用(リンク) |
|---|---|---|---|
| 1) | GMSC由来 マクロファージ取り込み |
蛍光顕微鏡 | R.Kawata, S.Oda, Y. Koya, H.Kajiyama, T. Yokoi, "Macrophage-derived extracellular vesicles regulate concanavalin A-induced hepatitis by suppressing macrophage cytokine production", Toxicology, 2020, doi:10.1016/j.tox.2020.152544. |
| 2) | HEK293s由来 HeLa取り込み |
蛍光顕微鏡 | Y. Nakao, T. Fukuda, Q. Zhang, T. Sanui, T. Shinjo, X. Kou, C. Chen, D. Liu, Y. Watanabe, C. Hayashi, H. Yamato, K. Yotsumoto, U. Tanaka, T. Taketomi, T. Uchiumi, A. D. Le, S. Shi, F. Nishiura, "Exosomes from TNF-α-treated human gingiva-derived MSCs enhance M2 macrophage polarization and inhibit periodontal bone loss", Acta Biomater., 2020, doi:10.1016/j.actbio.2020.12.046. |
| 3) | HEK293.2sus由来 磁性ナノゲルと融合 |
フローサイトメーター | R. Mizuta, Y. Sasaki, k. Katagiri, S. Sawada and K. Akiyoshi, "Reversible conjugation of biomembrane vesicles with magnetic nanoparticles using a self-assembled nanogel interface: single particle analysis using imaging flow cytometry", Nanoscale Adv., 2022, doi:10.1039/d1na00834j. |
| 4) | マウス T細胞由来 マウス肝臓、腎臓、足細胞取り込み |
蛍光顕微鏡 | H. Chuang, M. Chen, Y. Chen, Y. Ciou, C. Hsueh, C. Tsai and T. Tan, "Induction of Interferon-γ and Tissue Inflammation by Overexpression of Eosinophil Cationic Protein in T Cells and Exosomes", Arthritis Rheumatol., 2021, doi:10.1002/art.41920. |
| 5) | HeLa; MSC(mesenchymal stem cells)細胞由来 | 蛍光顕微鏡 | N. Kamei, H. Nishimura, A. Matsumoto, R. Asano, K. Muranaka, M. Fujita, M. Takeda, H. Hashimoto, M. Takeda-Morishita, "Comparative study of commercial protocols for high recovery of high-purity mesenchymal stem cell-derived extracellular vesicle isolation and their efficient labeling with fluorescent dyes,", 2021, doi:10.1016/j.nano.2021.102396. |
| 6) | Lck-BPI Tg T cells-由来 | 蛍光顕微鏡 | H. Chuang, M. Chen, Y. Chen, H. Yang, Y. Ciou, C. Hsueh, C. Tsai, T. Tan, "BPI overexpression suppresses Treg differentiation and induces exosome-mediated inflammation in systemic lupus erythematosus", 2021, doi:10.7150/thno.63743. |
| 7) | Colorectal Cancer細胞由来 | 蛍光顕微鏡 | H. Takakura, T. Nakao, T. Narita, M. Horinaka, Y. Nakao-Ise, T. Yamamoto, Y. Iizumi, M. Watanabe, Y. Sowa, K. Oda, N. Mori, T. Sakai, and M. Mutoh, "Citrus limon L.-Derived Nanovesicles Show an Inhibitory Effect on Cell Growth in p53-Inactivated Colorectal Cancer Cells via the Macropinocytosis Pathway ", 2022, doi:10.3390/biomedicines10061352. |
よくある質問
-
Q
推奨されるエクソソームの精製法はありますか?
-
A
超遠心法での精製を推奨しておりますが、免疫沈降法や磁気ビーズで精製したエクソソームの染色実績もございます。
また、超遠心法と同等の回収実績のある、ExoIsolator Exosome Isolation Kit(EX10)もご利用いただけます。
なお、ポリマー沈殿法で精製したエクソソームは下記の理由により、残存するポリマーの影響を受けるため、本キットでの染色はできません。1)未反応色素の精製工程で使用するフィルトレーションチューブにポリマーがつまり、精製できなくなる可能性がございます。
2)ポリマーがエクソソームと相互作用し、エクソソームの膜電位が変わる可能性がございます。膜電位が変わると、細胞取り込みアッセイに標識エクソソームを使用する場合、細胞内動態が変化する恐れがございます。
-
Q
標識後の精製操作でフィルターは着色していますが、未反応の色素は分離できていますか?
-
A
未反応の色素はフィルターに保持されるために着色が見られますが、小社では以下の実験でフィルター上の回収物に未反応色素が含まれないことを確認しております。
<実験条件>
超遠心法で精製した ①エクソソーム(タンパク質量として10µg)のバッファー溶液 または ②バッファーのみ を各キットのプロトコルに従って染色操作したのち、得られた回収物をHeLa細胞(1.25×104 cells)に添加して、4時間後の蛍光画像を観察しました。結果として、バッファーのみで得られた回収物は細胞へ添加しても蛍光輝点が観察されず、回収物に未反応の色素が残っていないことを確認しました。
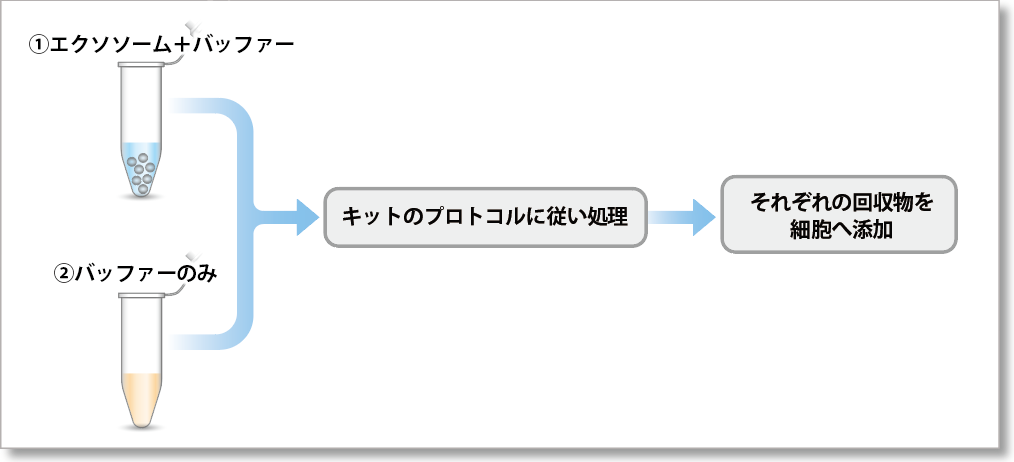
①エクソソーム+バッファーをキットで処理した場合
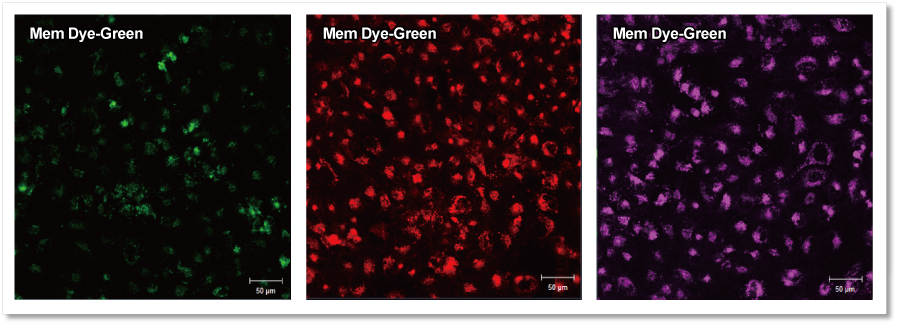
細胞へ添加後(4h)の蛍光画像
②バッファーのみをキットで処理した場合

細胞へ添加後(4h)の蛍光画像
■ 検出条件
Green:Ex 488 nm / Em 490 – 540 nm
Red :Ex 561 nm / Em 570 – 640 nm
Deep Red:Ex 640 nm / Em 640 – 760 nm
-
Q
染色後のエクソソームは保存できますか?
-
A
染色後のエクソソームの保存は推奨しておりません。
エクソソームの染色後はできるだけ早く実験にご使用ください。
-
Q
エクソソームの取込実験で使用実績のある培地を教えてください。
-
A
小社では染色後のエクソソームを用いた細胞への取り込み実験において、
MEM(Minimum Essential Medium)ならびにDMEM(Dulbecco's Modified Eagle's Medium)での実績がございます。なお、ExoSparklerシリーズは血清含有培地中での取込実験に最適化しているため、
無血清培地中で使用することはお勧めできません。
-
Q
1sampleあたりの染色できるエクソソーム量(タンパク質量、粒子数)を教えてください。
-
A
1sampleあたりのエクソソーム量(タンパク質量、粒子数)は以下の通りです。
精製済エクソソーム(超遠心法)として、タンパク質:1-10 μg/sample, 粒子数 10-100x 108 個/sample
-
Q
エクソソーム以外に夾雑物が含まれる場合、夾雑物も染色されますか?
-
A
はい。エクソソームにタンパク質やポリマー*等の夾雑物が含まれると、夾雑物も染色されてしまいます。
そのため、精製したエクソソームをご準備ください。
*精製方法によっては、ポリマーが残存する場合があります。精製方法については、「推奨されるエクソソームの精製法はありますか?」をご参照ください。
取扱条件
| 保存条件: 冷蔵,遮光 |