Mito-FerroGreen

ミトコンドリア内鉄イオン検出試薬
-
製品コードM489 Mito-FerroGreen
-
CAS番号-
| 容 量 | メーカー希望 小売価格 |
富士フイルム 和光純薬 |
|---|---|---|
| 50 μg x 2 | ¥33,600 | 344-09211 |
※ 50 μg当たり35 mm dish 5枚分染色可能(終濃度 5 μmol/l使用時)
性質
鉄は、生体内で最も多く存在する遷移金属元素であり、様々な生理活性を示すことが報告されています。近年、タンパク質非結合型の鉄イオン(自由鉄)としての存在が注目されており、その高い反応性は細胞損傷や細胞死にも関与していることが示唆されています。自由鉄は安定な化学種である鉄(II)イオン及び鉄(III)イオンとして存在しますが、生細胞内において、細胞内還元的環境、水溶性、トランスポーターの存在等を考慮すると鉄(III)イオンよりも鉄(II)イオンの挙動を知ることが重要であると考えられています。
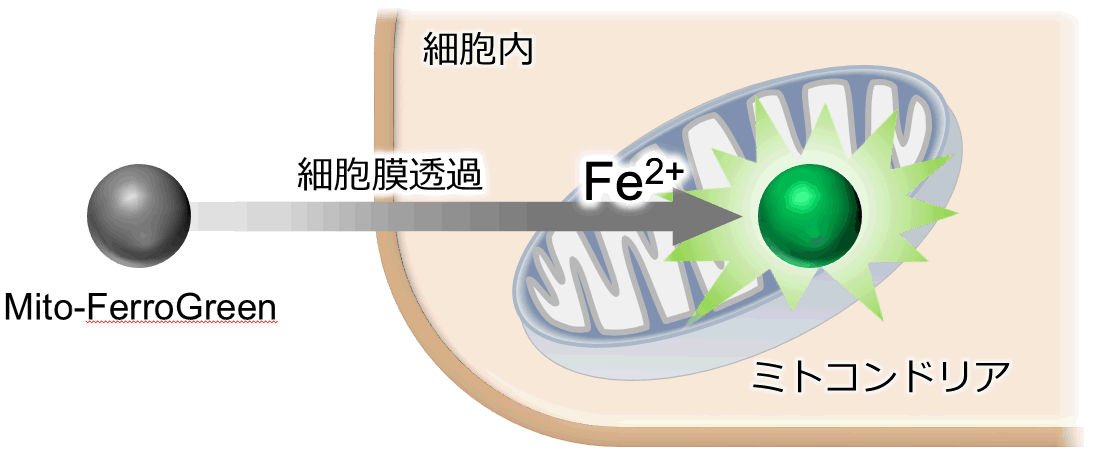
Mito-FerroGreen は、FeSクラスターやヘム合成の場として知られるミトコンドリア内の鉄(II)イオンと選択的に反応し強い蛍光(λex=505 nm, λem=535 nm)を発する試薬であり、細胞内鉄(II)イオンのライブセルイメージングに利用することが可能です。Mito-FerroGreenにはキレート能はありません。Mito-FerroGreenとFe2+は非可逆的に反応するため、Fluo 3のようなカルシウムイオンプローブの検出原理とは異なります。
本製品は、岐阜薬科大学薬化学研究室 永澤秀子先生、平山祐先生のご指導の下、製品化しました。
細胞死関連製品
| 指標 | 製品名 | 測定対象 | 装置 / 検出波長 |
|---|---|---|---|
| 細胞生存能力 | Cell Counting Kit-8 | 細胞内脱水素 酵素活性 |
プレートリーダー 吸光度 λ= 450nm |
| ネクローシス (細胞毒性) |
Cytotoxicity LDH Assay Kit-WST |
遊離LDH | プレートリーダー 吸光度 λ= 490nm |
| アポトーシス | Annexin V Apoptosis Plate Assay Kit |
ホスファチジルセリン | プレートリーダー 蛍光 Ex: 488 nm / Em: 525 nm |
| フェロトーシス | FerroOrange | 細胞内 鉄イオン(Fe2+) |
蛍光顕微鏡, FCM, プレートリーダー 蛍光 Ex: 543 nm / Em: 580 nm |
| フェロトーシス | Lyso-FerroRed | リソソーム内 鉄イオン(Fe2+) |
蛍光顕微鏡, FCM, プレートリーダー 蛍光 Ex: 551 nm / Em: 571 nm |
| フェロトーシス | Mito-FerroGreen | ミトコンドリア内 鉄イオン(Fe2+) |
蛍光顕微鏡 蛍光 Ex: 505 nm / Em: 535 nm |
| フェロトーシス | Liperfluo | 脂質過酸化 | 蛍光顕微鏡, FCM 蛍光 Ex: 488 nm / Em: 500-550 nm |
| フェロトーシス | Iron Assay Kit -Colorimetric- |
組織内鉄イオン (Fe2+, Fe3+) |
プレートリーダー 吸光度 λ= 593nm |
技術情報
測定原理
鉄検出試薬の選択
鉄検出時の実験方法および測定機器に応じて試薬を選択頂けます。
| FerroOrange | Mito-FerroGreen | |
|
細胞内の局在 |
細胞内 |
ミトコンドリア |
|---|---|---|
|
蛍光特性 |
λex : 543 nm、λem : 580 nm |
λex : 505 nm、λem : 535 nm |
|
対応装置 |
蛍光顕微鏡、プレートリーダー (Cy3) |
蛍光顕微鏡 (FITC、GFP) |
|
測定対象 |
生細胞 |
生細胞 |
|
染色回数 |
24 μgで35 mm dish 17枚分染色可能 |
50 μgで35 mm dish 5枚分染色可能 |
確かなミトコンドリア集積性
Mito-FerroGreen のミトコンドリア内局在を確認するため、ミトコンドリア染色試薬(MitoBright Deep Red※)と共染色を行い、Mito-FerroGreen がミトコンドリアを選択的に染色していることを確認した。
Mito-FerroGreen
励起波長:488 nm
蛍光波長:500-565 nm
MitoBright Deep Red
励起波長:640 nm
蛍光波長:656-700 nm
HeLa 細胞に 5 μmol/l Mito-FerroGreen およびミトコンドリア染色試薬 200 nmol/l MitoBright Deep Redを添加し炭酸ガスインキュベータ内で30 分間インキュベート。更に100 μmol/l 硫酸アンモニウム鉄(Ⅱ)を添加し、炭酸ガスインキュベータ内で1 時間インキュベートし、蛍光イメージングにより観察。
※ MitoBright Deep Redは現在販売しておりません。
滞留性を高めた改良品 MitoBright LT Deep Red (製品コード:MT12)をご参照ください。
ミトコンドリア内鉄のライブイメージング
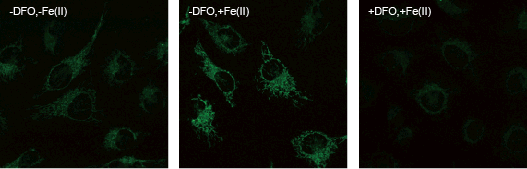
血清を含むMEM 増殖培地にて培養したHeLa 細胞へMito-FerroGreen を添加することで、ミトコンドリアに内在する鉄を蛍光にて検出した(左図)。一方、鉄を添加したHeLa 細胞では、Mito-FerroGreen の強い蛍光がみられ(中央図)、鉄キレート試薬と鉄を添加した細胞では、Mito-FerroGreen の蛍光はほどんど見られなかった。この様にミトコンドリア内鉄量の差を蛍光強度の差として確認した。
励起起波︓488 nm
蛍光波長︓500-565 nm
HeLa 細胞に5 μmol/l Mito-FerroGreen を添加し更に炭酸ガスインキュベータ内で30 分間インキュベート(左図)。その後、100 μmol/l硫酸アンモニウム鉄(II)を添加(中央図)、または、10 mmol/l DFO および100 μmol/l硫酸アンモニウム鉄(II)を添加し(右図)、それぞれを炭酸ガスインキュベータ内で1 時間インキュベートしたものを蛍光イメージングにより観察。
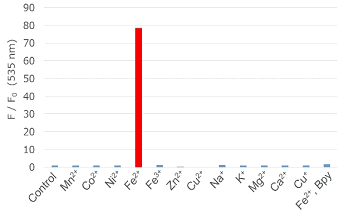
Fe2+への高い選択性
Fe2+への高い選択性と高いシグナルが得られる。
50 mmol/l HEPES Buffer (pH7.4) 1 ml中に1 mmol/l Mito-FerroGreen 2 μl、10 mmol/l各種金属 2 μl 及び 1 mg/ml エステラーゼ 20 μlを加え室温にて1時間反応後の蛍光強度を測定。
励起起波:500 nm
蛍光波長:535 nm
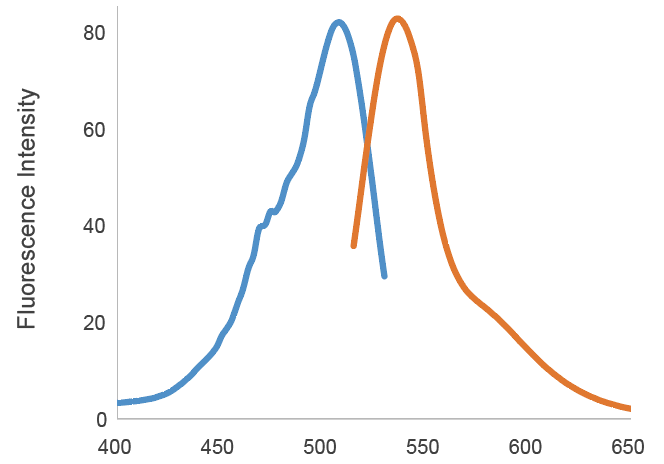
汎用フィルターに適応
極大励起波長が505 nmにあるMito-FerroGreenは 488 nmでの励起が可能である。
50 mmol/l HEPES Buffer (pH7.4) 3 ml中に1 mmol/l Mito-FerroGreen 6 μl、10 mmol/l硫酸アンモニウム鉄(Ⅱ)6μl 及び 1 mg/ml エステラーゼ 20 μlを加え37℃にて1時間反応後の蛍光強度を測定。
励起起波:505 nm
蛍光波長:535 nm
参考文献
参考文献
1) T. Hirayama, S. Kadota, M. Niwa and H. Nagasawa, "A mitochondria-targeted fluorescent probe for selective detection of mitochondrial labile Fe(II)", Metallomics., 2018, DOI: 10.1039/C8MT00049B, ※論文中では「Mito-FerroGreen」を「Ac-MtFluNox」で表記。.
2) T. Issitt, E. Bosseboeuf, N. Winter, N. Dufton, G. Gestri, V. Senatore, A. Chikh, A. Randi, C. Raimondi, "Neuropilin-1 controls endothelial homeostasis by regulating mitochondrial function and iron-dependent oxidative stress via ABCB8", iScience., 2018,DOI: 10.1016/j.isci.2018.12.005 .
3) E. E. Mon, F. Y. Wei, R. N. R. Ahmad, T. Yamamoto, T. Moroishi and K. Tomizawa, "Regulation of mitochondrial iron homeostasis by siderofexin 2 ", J Physiol Sci., 2018,doi:10.1007/s12576-018-0652-2.
4) M. Fujimaki, N. Furuya, S. Saiki, T. Amo, Y. Imamichi and N. Hattori, "Iron supply via NCOA4-mediated ferritin degradation maintains mitochondrial functions", Mol. Cell. Biol.., 2019,doi: 10.1128/MCB.00010-19.
5) K. Tomita, M. Fukumoto, K. Itoh, Y. Kuwahara, K. Igarashi, T. Nagasawa, M. Suzuki, A. Kurimasa and T. Sato, "MiR-7-5p is a key factor that controls radioresistance via intracellular Fe2+ content in clinically relevant radioresistant cells.", Biochem Biophys Res Commun.., 2019,doi: 10.1016/j.bbrc.2019.08.117.
6) Y. Wang and M. Tang, "PM2.5 induces ferroptosis in human endothelial cells through iron overload and redox imbalance", Environ. Pollut., 2019, 264, doi: 10.1016/j.envpol.2019.07.105.
7) KF. Yambire, C. Rostosky, T. Watanabe, D. Pacheu-Grau, S. Torres-Odio,A. Sanchez-Guerrero,O. Senderovich, EG. Meyron-Holtz,I.Milosevic, J. Frahm, AP. West and N. Raimundo, "Impaired lysosomal acidification triggers iron deficiency and inflammation in vivo.", Elife, 2019, 3, (8), doi:10.7554/eLife.51031.
8) H. Nishizawa, M. Matsumoto, T. Shindo, D. Saigusa, H. Kato, K. Suzuki, M. Sato, Y. Ishii, H. Shimokawa and K. Igarashi, "Ferroptosis is controlled by the coordinated transcriptional regulation of glutathione and labile iron metabolism by the transcription factor BACH1", J. Biol. Chem., 2019,doi: 10.1074/jbc.RA119.009548.
9)Y. akashima, A. Hayano and B. Yamanaka, Metabolome analysis reveals excessive glycolysis via PI3K/AKT/mTOR and RAS/MAPK signaling in methotrexate-resistant primary CNS lymphoma-derived cells.", Clin. Cancer Res., 2020, DOI:10.1158/1078-0432.
よくある質問
取扱条件
| 性状: | 本品はアセトニトリル、メタノール、ジメチルスルホキシドに溶解する。 |
|---|---|
| 純度(HPLC): | 90.0% 以上 |
| 蛍光スペクトル: | 試験適合 |
| 保存条件: 冷凍,遮光 , 取扱条件: 窒素置換,吸湿注意 |