ICG Labeling Kit - NH2
抗体・タンパク質標識キット
- 簡単な操作で実験したい
- 抗原認識部位を妨害しない低分子で標識したい
- in vivo イメージングで見たい
-
製品コードLK31 ICG Labeling Kit - NH2
| 容 量 | メーカー希望 小売価格 |
富士フイルム 和光純薬 |
|---|---|---|
| 3 samples | ¥63,500 | 345-91431 |
| サンプル量 | 50-200 µg |
|---|---|
| 所要時間 | 2時間 |
| 標識部位 | -NH2 |
| 検出方法 | 顕微鏡・FCM |
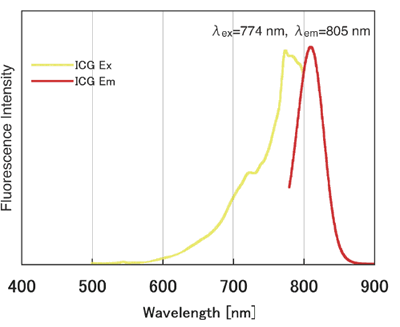
| 蛍光特性 | [Ex:774, Em:805] |
|
・分子量50,000以上のタンパク質が標識できる。 ・Filtration Tubeを用いた分離操作により抗体の場合は高い回収率で標識体が得られる。 ・付属の保存溶液でICG標識体の保存ができる。 |
|
| 3 samples | ・NH2-Reactive ICG ・WS Buffer ・Reaction Buffer ・Filtration Tube |
3 tubes 4 ml x1 500 μl x1 3 tubes |
|---|
性質
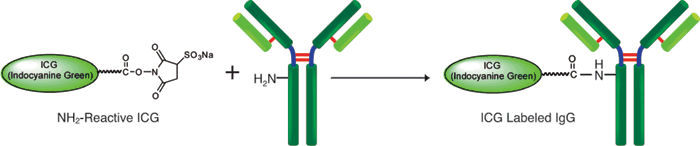
ICG (Indocyanine Green)は肝機能、肝予備能検査のための色素負荷試験にも用いられているシアニン色素で、近赤外領域に蛍光を持つ。励起波長は774 nm付近、蛍光波長は805 nm付近で、生体内で用いた場合でもヘモグロビンなどによる妨害を受けにくいという蛍光特性がある。そのため近赤外蛍光を利用したin vivo蛍光イメージングへの応用が期待されている。ICG Labeling Kit - NH2はアミノ基を有するタンパク質、特に抗体にICGを標識するためのキットである。既に発売しているFluorescein Labeling Kit - NH2(Code: LK01)やHiLyte FluorTM 555 Labeling Kit - NH2(Code: LK14), HiLite FluorTM 647 Labeling Kit - NH2(Code: LK15)と同様にキット付属のNH2-Reactive ICGは分子内に活性エステルを有しているため、アミノ基を有する分子と混合するだけで安定な共有結合を形成する。タンパク質にICGを標識する場合、標識反応を阻害するような低分子化合物(トリスなど)や未反応のNH2-Reactive ICGは付属のFiltration Tubeを用いて、容易に除去することができる。ICG標識IgGの場合、蛍光波長は774/805 nmである。
本キットには標識に必要な試薬と作製したICG標識体を保存するための溶液が含まれている。
| 開発元 | Dojindo Molecular Technologies, Inc. |
|---|
マニュアル
技術情報
特長
1) 約2時間で標識体が調製できる。
2) 分子量50,000以上のタンパク質に標識できる。
3) 50~200 μgのタンパク質に標識可能である。
4) Filtration Tubeを用いた分離操作により高い回収率で標識体が得られる。
5) 付属の保存溶液で標識体の保存ができる。
注意事項
|
・ |
市販の抗体などでゼラチンやアルブミン等を安定化剤として含む場合、それらの成分を除いてからご使用ください。試料中の共存物質の影響については「よくある質問:サンプル溶液中の共存物は反応に影響しますか?」に詳細を記載しておりますのでご参照ください。 |
|
・ |
NH2-Reactive ICGは、アルミラミジップに3本入っています。アルミラミジップを一旦開封した後は、未使用のNH2-Reactive ICGは、アルミラミジップに入れたまま、チャックをしっかりと閉め、-20℃で保存してください。NH2-Reactive ICG以外は、0~5℃で保存してください。 |
|
・ |
冷蔵保存中もしくは室温に戻した際に、フィルトレーションチューブに水滴様の液粒が見られることがあります。これはメンブランの乾燥防止剤が液粒化したもので、製品の性能に問題はございません。 |
|
・ |
本キットには溶液の入ったマイクロチューブのコンポーネントが含まれています。チューブ内壁やキャップに溶液が付着していることがありますので、開封前に振り落としてご使用ください。 |
キット以外に必要なもの
・10 μl, 200 μlマイクロピペッター ・インキュベーター(37℃)
・遠心機(マイクロチューブ用) ・マイクロチューブ(標識体保存用) ・DMSO
反応原理
ICGラベル抗体を用いたマウス皮下腫瘍の蛍光観察
●装置:Clairvivo OPT(島津製作所)
尾静注によりICGラベル抗体50 μg投与(投与48時間後に測定)
マウス:BALB/c nu/nu (雌 11週齢) , 腫瘍細胞:HeLa(右腋皮下移植,移植後4週)
抗体:抗インテグリンα2抗体
測定条件:励起波長 785 nm , 蛍光波長 845/55 nm(中心波長/帯域波長), 露光時間10秒
参考文献
1) M. Ogawa, C. A. S. Regino, J. Seidel, M. V. Green, W. Xi, M. Williams, N. Kosaka, P. L. Choyke and H. Kobayashi, "Dual-Modality Molecular Imaging Using Antibodies Labeled with Activatable Fluorescence and a Radionuclide for Specific and Quantitative Targeted Cancer Detection", Bioconjugate Chem., 2009, 20(11), 2177.
2) M. Ogawa, N. Kosaka, P. L. Choyke and H. Kobayashi, "In vivo Molecular Imaging of Cancer with a Quenching Near-Infrared Fluorescent Probe Using Conjuates of Monoclonal Antibodies and Indocyanine Green", Cancer Res., 2009, 69(4), 1268.
3) N. Kosaka, M. Ogawa, P. L. Choyke and H. Kobayashi, "Clinical implications of near-infrared fluorescence imaging in cancer", Future Oncology, 2009, 5(9), 1501.
4) 伊藤進, 六車直樹, 林重仁, 日下至弘, 多田津昌也, 多田津陽子, 岡本耕一, 井本佳孝, 稲山久美, 坂東輝美, 田岡聡子, 高川真由子, 矢野充保, 伊井邦雄, 長尾善光, 佐野茂樹, 芝村誠一, 島田典昭, 石田和彦, 中村一成, "赤外線蛍光内視鏡の原理と臨床応用”, Biomedical THERMOLOGY, 2003, 23(2), 77.
5) S. Ito, N.Muguruma, S. Hayashi, S. Taoka, T. Bando, K. Inayama, M. Sogabe, T. Okahisa, S. Okamura, H. Shibata, T. Irimura, K. Takesako and S. Shibamura, "Development of Agents for Reinforcement of Fluorescence on Near-infrared Ray Excitation for Immunohistological Staining", Bioorg. Med. Chem., 1998, 6, 613.
6) S. Ito, N. Muguruma, Y. Kakehashi, S. Hayashi, S. Okamura, H. Shibata, T. Okahisa, M. Kanamori, S. Shibamura, K. Takesako, M. Nozawa, K. Ishida and M. Shiga, "Development of Fluorescence-Emitting Antibody Labeling Substance by Near-Infrared Ray Excitation", Bioorg. Med. Chem. Lett., 1995, 5, 2689.
7) K. Inayama, S. Ito, N. Muguruma, Y. Kusaka, T. Bando, Y. Tadatsu, M. Tadatsu, K. Ii, S. Shibamura and K. Takesako, "Basic Study of an Agent for Reinforcement of Near-infrared Fluorescence on Tumor Tissue", Digestive and Liver Disease, 2003, 35, 88.
8) S. Ito, N. Muguruma, S. Hayashi, S. Taoka, T. Bando, Y. Kusaka, M. Yano, S. Ichikawa, A. Hiasa, T. Omoya, H. Honda, I. Shimizu, K. Ii, K. Nakamura, K. Takesako, Y. Goto and S. Shibamura, "Visualization of Human Gastric Cancer with a Novel Infrared Fluorescent Labeling Marker of Anti-carcinoembryonic Antigen Antibody in vitro", Dig. Endosc., 2000, 12, 33.
9) S. Taoka, S. Ito, N. Muguruma, S. Hayashi, Y. Kusaka, K. Ii, K. Nakamura, K. Imaizumi, K. Takesako and S. Shibamura, "Reflected Illumination-type Imaging System for the Development of Infrared Fluorescence Endoscopy", Dig. Endosc.,1999, 11(4), 321.
10) S. Ito, N. Muguruma, S. Hayashi, S. Taoka, A. Tsutsui, T. Fukuda, T. Okahisa, Y. Ohkita, H. Matsunaga, I. Shimizu, K. Nakamura, K. Imaizumi, K. Takesako and S. Shibamura,"Development of an Imaging System Using Fluorescent Labeling Substances Excited by Infrared Rays", Dig. Endosc., 1997, 9, 278.
11) S. Ito, N. Muguruma, Y. Kusaka, M. Tadatsu, K. Inayama, Y. Musashi, M. Yano, T. Bando, H. Honda, I. Shimizu, K. Ii, K. Takesako, H. Takeuchi and S. Shibamura, "Detection of Human Ganstric Cancer of Resected Specimens Using a Novel Infrared Fluorescent Anti-Human Carcinoembryonic Antigen Antibody with an Infrared Fluorescence Endoscope in Vitro", Endoscopy, 2001, 33(10), 849.
12) N. Muguruma, S. Ito, T. Bando, S. Taoka, Y. Kusaka, S. Hayashi, S. Ichikawa, Y. Matsunaga, Y. Tada, S. Okamura, K. Ii, K. Imaizumi, K. Nakamura, K. Takesako and S. Shibamura, "Labeled Carcinoembryonic Antigen Antibodies Excitable by Infrared Rays: a Novel Diagnostic Method for Micro Cancers in the Digestive Tract", Internal Medicine, 1999, 38(7), 537.
13) T. Bando, N. Muguruma, S. Ito, Y. Musashi, K. Inayama, Y. Kusaka, M. Tadatsu, K. Ii, T. Irimura, S. Shibamura and K. Takesako, "Basic Study on a Labeled anti-mucin Antibody Detectable by Infrared-fluorescence Endoscopy", J. Gastroenterol., 2002, 37, 260.
14) N. Muguruma, S. Ito, S. Hayashi, S. Taoka, H. Kakehashi, K. Ii, S. Shibamura and K. Takesako, "Antibodies Labeled with Fluorescence-agent Excitable by Infrared Rays", J. Gastroenterol., 1998, 33, 467.
15) 伊藤進, 六車直樹,“不可視情報の画像化-新しい内視鏡診断学の展望 (5)赤外蛍光を用いた微小癌診断”, 臨牀消化器内科, 1999, 14(8), 1205.
16) W. Aung, A. Tsuji, H. Sudo, A. Sugyo, T. Furukawa, Y. Ukai, Y. Kurosawa and T. Saga, "Immunotargeting of Integrin α6β4 for Single-Photon Emission Computed Tomography and Near-Infrared Fluorescence Imaging in a Pancreatic Cancer Model", Molecular Imaging, 2016, 15, 1.
よくある質問
-
Q
Labeling Kitで1次抗体を直接標識する利点を教えてください。
-
A
はじめて抗体標識をされる方を対象としたプロトコルを作成しております。
カスタマーサポートの視点から直接標識法の利点や実施例等を記載しておりますので、ご参照下さい。下記リンクよりダウンロード可能です。
「はじめての抗体標識プロトコル ~カスタマーサポートの視点から~」
-
Q
サンプル溶液中の共存物は反応に影響しますか?
-
A
共存物の種類により影響することがあります。
溶液中にどのような物質が含まれるかを確認の上、状況に応じてラベル化に用いるサンプルの精製を行い、標識反応にご使用ください。<高分子:分子量1万以上>
影響する可能性があります。
BSAやゼラチンなどアミノ基をもつ化合物が含まれると、抗体への標識効率が低下します。また、高分子のためFiltration Tubeでも除くことができません。また、アミノ基を持たない化合物でも、高分子の不純物が多いとフィルターの目詰まりの原因になり、標識・精製操作に支障がでる可能性もあります。反応に使用する前に別途精製を行ってください。
*本製品に限らず他のLabeling kit に関しても同様の注意が必要です。
-
Q
低分子のタンパク質(分子量50,000以下)に標識する場合の方法を教えて下さい。
-
A
キット付属のフィルトレーションチューブは分画分子量30Kの限外濾過フィルターのため、余裕をもって50,000以上のタンパク質のご使用を推奨しております。
分子量50,000以下のタンパク質を標識される場合は、下記のような分画分子量の小さい限外濾過フィルターに変更して頂くことで、低分子のタンパク質でもラベル化可能でございます。
------------------------------------------
PALL社 ナノセップ 3K 製品No.OD003C33
PALL社 ナノセップ 10K 製品No.OD010C33
------------------------------------------キット同梱のフィルターを用いた場合に比べ遠心に時間を要することがございますので遠心時間はご検討下さい。
取扱条件
| 保存条件: 冷蔵 , 取扱条件: 吸湿注意 |