HiLyte Fluor™ 555 Labeling Kit - NH2
抗体・タンパク質標識キット
- 簡単な操作で実験したい
- 抗原認識部位を妨害しない低分子で標識したい
- Cy3と類似した蛍光特性を持つ色素でみたい
-
製品コードLK14 HiLyte Fluor™ 555 Labeling Kit - NH2
| 容 量 | メーカー希望 小売価格 |
富士フイルム 和光純薬 |
|---|---|---|
| 3 samples | ¥30,400 | 348-91041 |
| サンプル量 | 50-200 µg |
|---|---|
| 所要時間 | 2時間 |
| 標識部位 | -NH2 |
| 検出方法 | 顕微鏡・FCM |
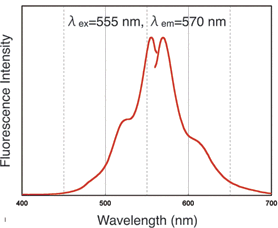
| 蛍光特性 | [Ex:555, Em:570] |
|
・分子量50,000以上のタンパク質が標識できる。 ・Filtration Tubeを用いた分離操作により高い回収率で標識体が得られる。 ・付属の保存溶液でHiLyte Fluor™標識体の保存ができる。 |
|
| 3 samples | ・NH2-Reactive Hilyte FluorTM 555 ・WS Buffer ・Reaction Buffer ・Filtration Tube |
3 tubes 4 ml x1 500 μl x1 3 tubes |
|---|
性質
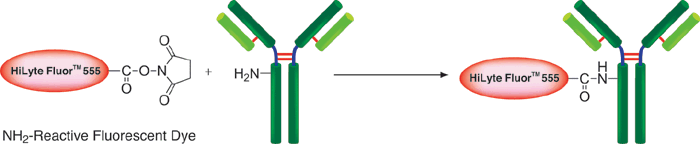
HiLyte FluorTM 555 Labeling Kit - NH2は、アミノ基を有するタンパク質、特に抗体へHiLyte FluorTM 555色素を標識するためのキットである。HiLyte FluorTM 色素は米AnaSpec社が開発した蛍光色素である。キット付属のNH2-Reactive HiLyte FluorTM 555は、その分子内に活性エステル基を有しているため、アミノ基を有する分子と混合するだけで安定な共有結合を形成する。タンパク質にHiLyte FluorTM 555を標識する場合、標識反応を阻害するような低分子化合物(トリスなど)や未反応のNH2-Reactive HiLyte FluorTM 555は付属のFiltration Tubeを用いて容易に除去することができる。HiLyte FluorTM 555標識IgGの場合、蛍光波長はλex/em=555/570 nmである。
本キットには、標識に必要なすべての試薬と作製したHiLyte FluorTM 555標識体を保存するための溶液が含まれている。
| 開発元 | Dojindo Molecular Technologies, Inc. |
|---|
マニュアル
技術情報
特長
1) 約2時間でHiLyte FluorTM標識体が調製できる。
2) 分子量50,000以上のタンパク質が標識できる。
3) 50~200 μgのタンパク質を標識可能である。
4) Filtration Tubeを用いた分離操作により高い回収率で標識体が得られる。
5) 付属の保存溶液でHiLyte FluorTM標識体の保存ができる。
*HiLyte FluorTMはAnaSpec 社の商標です。同仁化学では試験・研究用として許諾を得ております。
注意事項
|
・ |
市販の抗体などでゼラチンやアルブミン等を安定化剤として含む場合、それらの成分を除いてからご使用ください。試料中の共存物質の影響については「よくある質問:サンプル溶液中の共存物は反応に影響しますか?」に詳細を記載しておりますのでご参照ください。 |
|
・ |
NH2-Reactive HiLyte FluorTM 555は、アルミラミジップに3本入っています。アルミラミジップを一旦開封した後は、未使用のNH2-Reactive HiLyte FluorTM 555は、アルミラミジップに入れたまま、チャックをしっかりと閉め、-20℃で保存してください。NH2-Reactive HiLyte FluorTM 555以外は、0~5℃で保存してください。 |
|
・ |
冷蔵保存中もしくは室温に戻した際に、フィルトレーションチューブに水滴様の液粒が見られることがあります。これはメンブランの乾燥防止剤が液粒化したもので、製品の性能に問題はございません。 |
キット以外に必要なもの
・10 μl, 200 μl マイクロピペッター
・インキュベーター(37℃)
・DMSO
・遠心機(マイクロチューブ用)
・マイクロチューブ(標識体保存用)
反応原理
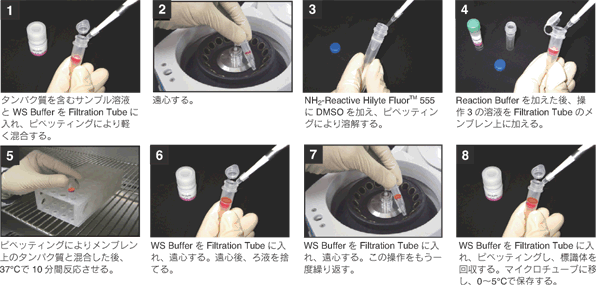
操作方法
実験例
HiLyte Fluor™ 標識抗IV 型コラーゲンα5(IV) 鎖抗体を用いて、各組織の基底膜を染色した。
各組織のα5(IV) 鎖を持つ基底膜のみ明瞭に染まっていることが確認できる。
使用抗体:IV 型コラーゲンα5(IV) 鎖特異的ラット単クローン抗体
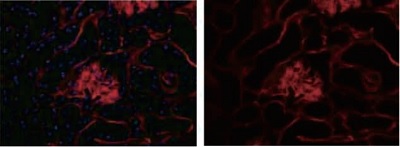
マウス腎の免疫組織画像(右)および核をヘキストによる核染色との二重染色(左)(撮影倍率 x64)
A5(IV)鎖がある糸球体基底膜、Bowman嚢基底膜、尿細管基底膜は染まっているが、毛細血管基底膜やメザンギウム基底膜は染まっていない。
使用キット:HiLyte Fluor™ 555 Labeling Kit-NH2
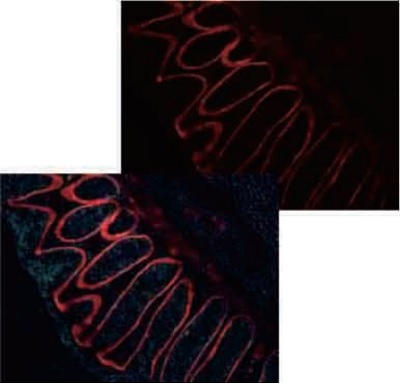
HiLyte Fluor™標識b14抗体を用いた
ヒト横行結腸の免疫染色画像(上)およびその位相差像との合成(下)
使用キット:HiLyte Fluor™555 Labeling Kit-NH2 (撮影倍率x20)
画像提供:岡山大学大学院 歯学総合研究科 人体構成学分野 内藤一郎先生、重井医学研究所 佐渡義一先生
参考文献
1) A. Nagao, K. Sato, K.M. Nishida, H. Siomi, M.C. Siomi, "Gender-specific hierarchy in nuage localization of PIWI-interacting RNA factors in Drosophila", Front Genet.,2011, 2, 55.
2) H. Hoshino, G. Shioi, S. Aizawa, "AVE protein expression and visceral endoderm cell behavior during anterior–posterior axis formation in mouse embryos: Asymmetry in OTX2 and DKK1 expression", Dev. Biol.., 2015, 402, (2), 175.
3) T. Kaneko, T. Minohara, S. Shima, K. Yoshida, A. Fukuda, N. Iwamori, T. Inai and H. Iida, "A membrane protein, TMCO5A, has a close relationship with manchette microtubules in rat spermatids during spermiogenesis", Mol. Reprod. Dev.., 2019, 86, (3), 330.
4) Y. Nakashima, T. Mima, M. Yashiro, T. Sonou, M. Ohya, A. Masumoto, S. Yamanaka, D. Koreeda, K. Tatsuta, Y. Hanba, M. Moribata, S. Negi, T. Shigematsu, "Expression and localization of fibroblast growth factor (FGF) 23 and Klotho in the spleen: its physiological and functional implications", Growth Factors ., 2016, 34, (5-6), 196.
5) Z. Zhang, K. Kakutani, K. Maeno, T. Takada, T. Yurube, M. Doita, M. Kurosaka and K. Nishida, "Expression of silent mating type information regulator 2 homolog 1 and its role in human intervertebral disc cell homeostasis", Arthritis Res. Ther.., 2011, 13, (6), R200.
6) I. Hasan, M. Gerdol, Y. Fujii and Y. Ozeki, "Functional Characterization of OXYL, A SghC1qDC LacNAc-specific Lectin from The Crinoid Feather Star Anneissia Japonica.", Mar Drugs., 2019, 17, DOI:10.3390/md17020136.
7)Y. Fujii, M. Gerdol, S.M.A. Kawsar, I. Hasan, F. Spazzali, T. Yoshida, Y. Ogawa, S. Rajia, K. Kamata, Y. Koide, S. Sugawara, M. Hosono, J.R.H. Tame, H. Fujita, A. Pallavicini and Y. Ozeki, "A GM1b/asialo-GM1 oligosaccharide-binding R-type lectin from purplish bifurcate mussels Mytilisepta virgata and its effect on MAP kinases.", FEBS J., 2019, DOI: 10.1111/febs.15154.
よくある質問
-
Q
Labeling Kitで1次抗体を直接標識する利点を教えてください。
-
A
はじめて抗体標識をされる方を対象としたプロトコルを作成しております。
カスタマーサポートの視点から直接標識法の利点や実施例等を記載しておりますので、ご参照下さい。下記リンクよりダウンロード可能です。
「はじめての抗体標識プロトコル ~カスタマーサポートの視点から~」
-
Q
サンプル溶液中の共存物は反応に影響しますか?
-
A
共存物の種類により影響することがあります。
溶液中にどのような物質が含まれるかを確認の上、状況に応じてラベル化に用いるサンプルの精製を行い、標識反応にご使用ください。<高分子:分子量1万以上>
影響する可能性があります。
BSAやゼラチンなどアミノ基をもつ化合物が含まれると、抗体への標識効率が低下します。また、高分子のためFiltration Tubeでも除くことができません。また、アミノ基を持たない化合物でも、高分子の不純物が多いとフィルターの目詰まりの原因になり、標識・精製操作に支障がでる可能性もあります。反応に使用する前に別途精製を行ってください。
*本製品に限らず他のLabeling kit に関しても同様の注意が必要です。
-
Q
サンプルが溶液でも問題ないでしょうか?
-
A
溶液であること自体は問題ありません。
ただし、下記の点をご確認いただいた上でご使用ください。
-濃度-
サンプル濃度が0.5mg/ml以下(50μg/100μl以下)である場合には
Filtration tubeを用いてサンプル量が50~200μgとなるように
遠心して濃縮を行ってください。
フィルター上に残ったサンプルは再溶解させる必要はありません。
そのまま反応にご使用ください。-溶液量-
Filtration tubeの容量に制限がありますので、溶液の量は100μl以下でご使用ください。-共存物-
・不溶性の低分子が含まれる場合は、予め遠心して上清のみを使用してください。
・分子量10,000以上の物質が含まれる場合には、別途精製を行ってからご使用ください。
(市販の抗体の中には安定化剤としてBSAやアルブミンを含む場合があります)
-
Q
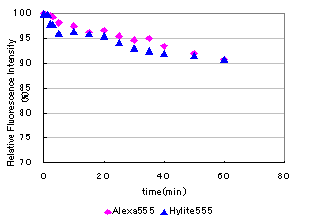
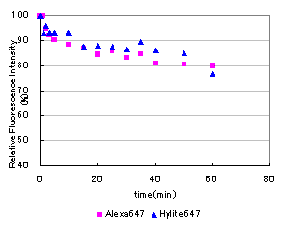
光による退色は起こりにくいのでしょうか?
-
A
当社での確認試験では、HiLyte Fluor 555, HiLyte Fluor 647ともにAlexaと同等の耐光性を示しています。
-
Q
低分子のタンパク質(分子量50,000以下)に標識する場合の方法を教えて下さい。
-
A
キット付属のフィルトレーションチューブは分画分子量30Kの限外濾過フィルターのため、余裕をもって50,000以上のタンパク質のご使用を推奨しております。
分子量50,000以下のタンパク質を標識される場合は、下記のような分画分子量の小さい限外濾過フィルターに変更して頂くことで、低分子のタンパク質でもラベル化可能でございます。
------------------------------------------
PALL社 ナノセップ 3K 製品No.OD003C33
PALL社 ナノセップ 10K 製品No.OD010C33
------------------------------------------キット同梱のフィルターを用いた場合に比べ遠心に時間を要することがございますので遠心時間はご検討下さい。
-
Q
標識後、フィルトレーションチューブを遠心してもメンブレン上に液が残る。
-
A
(1)メンブレンを目視で確認した際、メンブレンカップの淵にうっすら液が残る程度であれば、次の操作に進んで下さい。
メンブレン上に液が残っていたり、メンブレンカップを傾けて回転させたとき、液が垂れてくるようであれば、さらに遠心を8,000g で15分~30分程度行って下さい。(2)1)の遠心操作後もメンブレン上に液が残る場合は、標識体が凝集していないか確認してください。
抗体やタンパク質自身の性質によりますが、低分子標識剤を標識することで抗体やタンパク質の疎水性が増し、凝集する場合がございます。
標識体に凝集が見られる場合は、一度別のマイクロチューブに移し、遠心し上澄みをご使用ください。(抗体・タンパク質の回収量は低下いたします。)
上記でも解決しない場合は、小社カスタマーサポートまでお問い合わせください。
※フィルターの目詰まりが疑われる場合は、メンブレンフィルターを新しいものに交換すると解決する場合がございます。
代替品: PALL社製 ナノセップ 30K (メーカーコード:OD030C33)
-
Q
IgG1分子に色素が幾つ標識されますか?
-
A
IgG1分子あたり、3~7個の色素が標識されます。
プロトコルや製品添付の説明書にも標識率を計算する式を載せてあります。HiLyte Fluor 555/タンパク質の標識率=[A555/150,000]/[(A280-A555x0.1)/ε]
A555:555nmの吸光度
A280:280nmの吸光度
ε:タンパク質の280nmのモル吸光係数(IgGの場合には216,000)
-
Q
未反応の色素は除去できますか?
-
A
説明書にある反応後の2回の洗浄で、未反応色素の95%は除去されます。
必要であれば、WS buffer等での洗浄をさらに2~3回繰り返すことで未反応色素はほぼ除去されます。
取扱条件
| 保存条件: 冷蔵 , 取扱条件: 吸湿注意 |