-Nucleostain- DNA Damage Quantification Kit -AP Site Counting-
ストレスマーカー検出試薬
-
製品コードDK02 -Nucleostain- DNA Damage Quantification Kit -AP Site Counting-
| 容 量 | メーカー希望 小売価格 |
富士フイルム 和光純薬 |
|---|---|---|
| 20 samples | ¥98,500 | 346-90143 |
| 20 samples | ・ARP-DNA Standard Solution ×(0, 2.5, 5.0, 10, 20, 40 AP sites/100,000 bp) ・ARP Solution ・DNA Binding Solution ・Washing Buffer ・HRP-Streptavidin ・TE Buffer ・Substrate Solution ・Filtration Tube ・96-well Microplate/U Bottom |
各 250 μl × 1 250 μl × 1 10 ml × 1 × 1 25 μl × 1 40 ml × 1 10 ml × 1 20 tubes × 1 |
|---|
性質
生物の遺伝情報を保持しているDNAは、複製時のDNA polymeraseのエラーに加えて、環境中の放射線や紫外線、またはアルキル化剤等の化学物質、生体内における活性酸素等の代謝産物により損傷を受ける。これらのエラーや損傷が正しく修復されなければ突然変異を誘発し、これが癌や老化の原因となる。
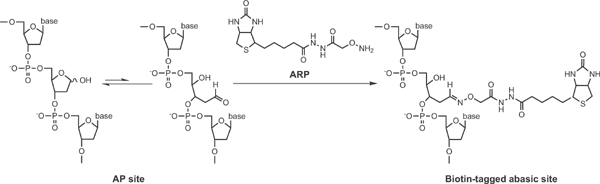
DNA損傷部位には修復機構が働き、その一つとして塩基除去修復がある。この時AP site (apurinic / apyrimidinic site)と呼ばれる塩基除去部位が出現する。つまりAP siteの検出はDNA損傷部位を測定し得る有効な方法となる。
ARP(N'-Aminooxymethylcarbonylhydrazino-D-biotin)はこのAP siteと特異的に結合しビオチン化できる試薬として知られている。-Nucleostain- DNA Damage Quantification Kit -AP Site Counting-は、ARPを用いてDNAをビオチン化し96穴マイクロプレートに固定化して検体DNA中のAP siteを簡便に定量できるキットである。
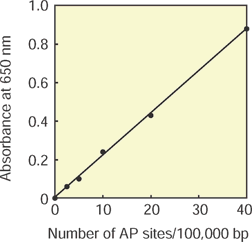
このキットには、AP site数が既定された標準DNAが含まれており、HRP標識ストレプトアビジンによるビオチン検出法を用いることによってAP siteの定量ができる。
使用方法は、プロトコルをご覧下さい。
*冷蔵保存中もしくは室温に戻した際に、フィルトレーションチューブに水滴様の液粒が見られることがあります。
これはメンブランの乾燥防止剤が液粒化したもので、製品の性能に問題はございません。
*本キットには溶液の入ったマイクロチューブのコンポーネントが含まれています。
チューブ内壁やキャップに溶液が付着していることがありますので、開封前に振り落としてご使用ください。
| 開発元 | Dojindo Molecular Technologies, Inc. |
|---|
マニュアル
技術情報
<キット以外に必要なもの>
・10 μl, 200 μl, 1 mlマイクロピペッター(可変式) ・200 μl 8連マイクロピペッター(可変式) ・インキュベーター(37℃) ・マイクロプレートリーダー ・0.5 ml, 1.5 ml遠心チューブ ・遠心機 ・DNA精製キット ・ペーパータオル
測定原理
操作方法
参考文献
参考文献
1) A. Sancar and G. B. Sancar, "DNA Repair Enzymes", Annu. Rev. Biochem., 1988, 57, 29.
2) T. Lindahl and B. Nyberg, "Rate of Depurination of Native Deoxyribonucleic Acid", Biochemistry, 1972, 11, 3610.
3) M. Liuzzi and M. Talpaert-Borle, "A New Approach to the Study of the Base-excision Repair Pathway Using Methoxyamine", J. Biol. Chem., 1985, 260, 5252.
4) M. Weinfeld, M. Liuzzi and M. C. Paterson, "Response of Phage T4 Polynucleotide Kinase Toward Dinucleotides Containing Apurinic Sites: Design of a 32P-postlabeling Assay for Apurinic Sites in DNA", Biochemistry, 1990, 29, 1737.
5) B. X. Chen, K. Kubo, H. Ide, B. F. Erlanger, S. S. Wallace and Y. W. Kow, "Properties of a Monoclonal Antibody for the Detection of Abasic Sites, a Common DNA Lesion", Mutat. Res., 1992, 273, 253.
6) J. A. Gralnick and D. M. Downs, "The YggX Protein of Salmonella enterica Is Involoved in Fe(II) Trafficking and Minimizes the DNA Damage Cause by Hydroxyl Radicals:Residue CYS-7 is Essential for YggX Function", J. Biol. Chem., 2003, 278, 20708.
7) J. W. Pippin, R. Durvasula, A. Petermann, K. Hiromura, W. G. Couser and S. J. Shankland, "DNA Damage is a Novel Response to Sublytic Complement C5b-9 Induced Injury in Podocytes", J. Clin. Invest., 2003, 111, 877.
8) S. Watanabe, T. Ichimura, N. Fujita, S. Tsuruzono, I. Ohki, M. Shirakawa, M. Kawasuji and M. Nakao, "Methylated DNA-binding Domain 1 and Methylpurine DNA Glycosylase Link Transcriptional Repression and DNA Repair in Chromatin", Proc. Natl. Acad. Sci. USA, 2003, 100, 12859.
9) M. Endres, M. Ahmadi, I. Kruman, D. Biniszkiewicz, A. Meisel and K. Gertz, "Folate Deficiency Increases Postischemic Brain Injury", Stroke, 2005, 36, 321.
10) J.-M. Li, M. Mogi, K. Tsukuda, H. Tomochika, J. Iwanami, L.-J. Min, C. Nahmias, M. Iwai and M. Horiuchi, "Angiotensin II-Induced Neural Differentiation via Angiotensin II Type 2 (AT2) Receptor-MMS2 Cascade Involving Interaction between AT2 Receptor-Interacting Protein and Src Homology 2 Domain-Containing Protein-Tyrosine Phosphatase 1", Mol. Endocrinolo., 2007, 21(2):499.
11) D. R. McNeill and D. M. Wilson III, "A Dominant-Negative Form of the Major Human Abasic Endonuclease Enhances Cellular Sensitivity to Laboratory and Clinical DNA-Damaging Agents", Mol. Cancer Res., 2007, 5(1), 61.
よくある質問
-
Q
40 AP sites/100,000以上のstandard solutionを作成することは出来ますか?
-
A
このキットのstandard DNAは0~40AP site/100,000 です。
弊社では、50 AP sites/100,000までのARP-DNAを調製したことは
ありますが、それ以上はありません。理論的にはそれ以上のARP-DNAを調製することは可能ですが、
検量線の直線性がどこまで保持されるかは保証できません。
高いレベルの塩基損傷を検出するには、サンプルDNAを同じ濃度の損傷の無いDNA
つまり、0AP site-DNAで測定レンジに希釈してアッセイを行い、
その後に実際のAP数を換算して求める方が良いと思います。
-
Q
DNA中の塩基損傷部位であるAP Siteは酸化ストレスの指標として使用されますが、 AP Siteの他に酸化ストレスマーカーとなるものはありますか?
-
A
酸化ストレスマーカーについてまとめた資料を作成しております。
カスタマーサポートの視点から、各酸化ストレスマーカーの特徴・測定サンプルの前処理方法などを記載しておりますので、ご参照ください。下記URLよりダウンロード可能です。
-
Q
DNAの純度が吸光度比で1.8以上を推奨されていますが、1.5程度でも測定出来ますか?
-
A
1.5では確認していませんので、保証は出来ません。
1.6~1.7のDNAでの測定では大きなバラツキは見られません。
推奨として1.8以上としております。精製度が低いということは、タンパク質の混入が考えられます。
タンパク質はブロッキング作用を持ち、DNAがプレートに吸着するのを
防ぐ可能性がありますので、出来るだけ精度が高いものをご使用ください。
-
Q
抽出したDNAをARP化せずに保存することは可能でしょうか?
-
A
溶液状態での保存はAP siteが増えてくるので望ましくありません。(冷蔵・冷凍ともに)
ARP化せずに保存するのであれば、エタノール沈殿を行い、ペレット状にして冷凍保存してください。AP部位は確かに切断が起こりやすい部位です。
ただ、catalist freeの状態で保存されていれば3'側に切断があってもARPの検出には支障ありません。
むしろ抽出DNAは凍結状態以外の環境下で保存されていた場合、
自然に起こる脱塩基によって形成されたAP部位の方が重要な問題になります。
この場合、サンプルに同一条件下で保存されていた標準DNAが含まれる場合は
補正が可能になります。
ARP修飾後のAP部位は安定ですので、抽出後の速やかなAPR処理をお勧めします。
-
Q
このキットを使用して何を測定することが出来るのでしょうか?
-
A
DNA中のAP siteの定量が出来ます。
AP siteとは[apurinic/apyrimidinic site]の略で、損傷したDNAに働く
塩基除去修復の過程で現れるものです。DNAの損傷は複製時のDNA polymeraseのエラーに加えて、環境中の放射線や
紫外線またはアルキル化剤等の化学物質、生体内における活性酸素などの
代謝産物により起こります。AP siteを測定することによりDNA損傷をみることが出来ます。
-
Q
このキットで測定できる検体数はどのくらいでしょうか?
-
A
20 samplesが20検体となります。
それぞれFiltration Tubeが20 samplesで20本入っています。
Filtration Tubeを一つのサンプルに1本使用しますので、このTubeの数が
測定できる検体数となります。20 samplesも測定用のプレートは1枚です。
-
Q
96-wellマイクロプレートやフィルトレーションチューブ以外の溶液が余ったのですが、 廃棄方法を教えて下さい。
-
A
余った溶液は、以下の成分情報をご確認の上、ご所属の機関の廃棄ルールに従って廃棄して下さい。
<キットコンポーネント成分>・ARP-DNA standard solution (水に希釈後廃棄、有害成分含まず)
・ARP solution (水に希釈後廃棄、有害成分含まず)
・DNA binding solution (水に希釈後廃棄、有害成分含まず)
・Washing buffer (水に希釈後廃棄、有害成分含まず)
・HRP-streptavidin (水に希釈後廃棄、有害成分含まず)
・TE buffer (水に可溶、EDTA・2NA 0.1%以下)
・Substrate solution (水に希釈後廃棄、有害成分含まず)
取扱条件
| 保存条件: 冷蔵 |