内外分泌細胞における硫化水素をはじめとしたガス性情報伝達物質の細胞内 Ca2+ 動態に及ぼす作用
Effects of hydrogen sulfide and other gasotransmitters on intracellular Ca2+ dynamics in exocrine and endocrine cells
 |
葉原 芳昭 北海道大学 大学院獣医学研究科 比較形態機能学講座 生理学教室 |
 |
Moustafa Amira Zagazig University Department of Physiology Faculty of Veterinary Medicine, Egypt |
Abstract
Ca2+ plays pivotal roles in regulating a variety of physiological functions in various endocrine and exocrine cells. Stimulation of these cells with specific secretagogues triggers an increase in intracellular Ca2+ concentration ([Ca2+]i ). In addition to these secretagogues, gasotransmitters such as H2S, NO, and CO also modulate [Ca2+]i. Here, we attempted to introduce effects of gasotransmitters on [Ca2+]i and presumed intracellular machineries deduced from our recent investigatuons carried out in pancreatic acinar cells, parotid acinar cells, pancreatic islet β-cells and peritoneal mast cells. Potential interactions among the gases will also be discussed.
キーワード: NO、CO、H2S/polysulfide、膵腺房細胞、耳下腺腺房細胞、膵島β細胞、肥満細胞、cross-talk、細胞内 Ca2+、SSP4
1. はじめに
1998年に F. Murad, L. Ignarro, R. Furchgott の 3 氏に「循環器系における信号伝達物質としての一酸化窒素 (NO)の発見」という功績でノーベル生理学・医学賞が授与されてからすでに 20 年が経とうとしている。この発見は、常温・常気圧で気体で、生体機能に毒性作用をもたらすことはあっても、シグナル分子として生理機能の調節に関わっているとは多くの科学者が予想だにしていなかった時代の秀逸なブレークスルーであった。今では NO の血管弛緩・降圧作用の細胞内メカニズムが明らかにされ、内皮細胞・平滑筋細胞ともに細胞内の Ca2+ が中心的な役割を担っていることがわかっている。
ところで、気体状態の物質が生理機能を制御している例は NO にとどまらない。 NO に続いて、近年、第 2 のガス性情報伝達物質として一酸化炭素(CO)が、第 3 のガスとして硫化水素(本稿では H2S と記載する) が注目されている 1-3)。いずれについても多彩な生理作用が想定されているが、NO に比較して細胞内 Ca2+ 動態との関連については一部の組織を除いて不明な点が多い。
私どもはこれまで様々な内外分泌細胞の開口放出における Ca2+ の役割についてもっぱら Ca2+ 画像解析法によって研究を進めてきている。ここ数年、三種類のガスの細胞内 Ca2+ 動態に及ぼす作用について検討を加えていることから、本稿では主に H2S ならびにポリスルフィドの細胞内 Ca2+ 動態に及ぼす作用について最近の知見を中心にまとめてみたい。
2.膵腺房細胞における H2S の[Ca2+]i に対する作用
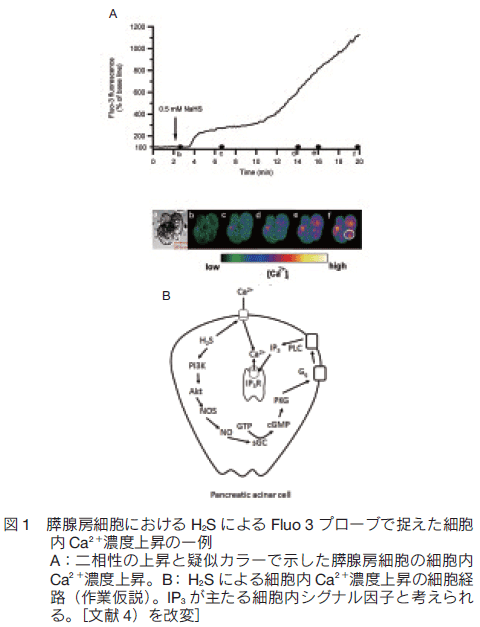
酵素原を放出する膵臓の腺房細胞において、細胞内 Ca2+ は開口放出を始動する必須因子である。この細胞には CBS と CSE が発現していることから、 H2S の産生と作用が想定されている。 H2S のドナーである Na HS を、実験的に作用させたところ、容量依存性で、二相性かつ細胞内外の Ca2+ に依存する[Ca2+]i 上昇が認められた(図 1A)。また、H2S の合成基質のひとつである L-cysteine を加えても[Ca2+]i が上昇した。細胞内の Ca2+ 遊離に依存する上昇は、フォスフォリパーゼ C 阻害薬の U73122、Gq タンパク質拮抗薬の GP2A および IP3 感受性の Ca2+ 遊離を阻害する xestospongin C によって抑制されたことから、 H2S による IP3 産生が関係していると推測された。さらに興味深いことに、 H2S による[Ca2+]i 上昇が、非特異的 NO 合成酵素阻害薬の L-NMMA および NO 消去剤の cPTIO で抑制されることを見いだした。この結果は、 H2S の[Ca2+]i 上昇作用に一部 NO が介在していることを推測させる。実際、 NO の蛍光指示薬である DAF-2 を用いて NO 産生を調べたところ、容量依存性に NO が産生されていることを示す結果が得られた。また、 H2S による[Ca2+]i 上昇は、可溶性グアニル酸シクラーゼ阻害薬の ODQ およびプロテインキナーゼ阻害薬の KT5823 によって抑制されたことからも NO の関与が強く示唆された。以上の結果を基に現在私どもが想定している H2S の膵腺房細胞内作用経路を図 1B に示した 4)。
3.耳下腺腺房細胞における H2S の[Ca2+]i に対する作用
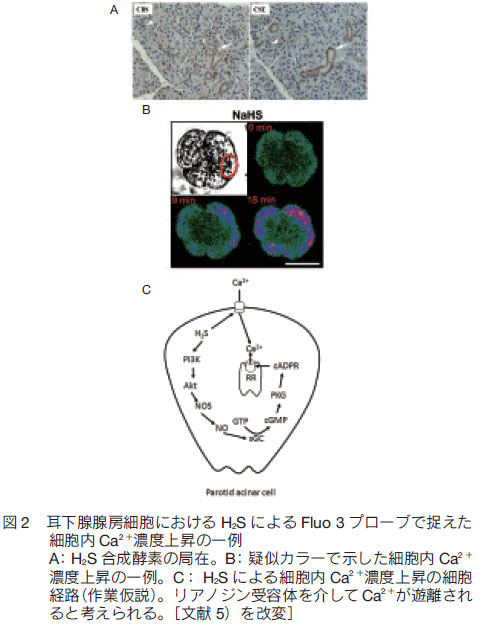
膵腺房細胞と構造・機能が類似している耳下腺腺房細胞についても H2S の作用を検討した。この細胞でも CBS と CSE が発現していた(図 2A)。膵腺房細胞同様、H2S はこの外分泌細胞でも容量及び細胞内外の Ca2+ 依存性に[Ca2+]i を上昇させた(図 2B)。 この上昇は H2S の消去剤であるハイポタウリンおよび L-NMMA と cPTIO によって抑制された。また DAF-2 により NO の産生も示唆されたことから、一部は膵腺房細胞同様 NO を介するものと推測された。なお、本細胞に nNOS と eNOS の発現が認められた 8)。 ここまでは膵臓と耳下腺で共通と考えられたが、両者で細胞内経路に大きな違いがあることが浮かび上がった。膵臓では有効であった U73122 と xestospongin C が耳下腺では無効である一方、ODQ, KT5823 およびリアノジン受容体阻害薬のルテニウムレッドは H2S による[Ca2+]i 上昇を有意に抑制した。この結果は耳下腺腺房細胞では、もっぱらリアノジン受容体チャネルを介する Ca2+ 遊離であることを示している(図 2C ) 5)。
4.腹腔肥満細胞におけるポリスルフィドと H2S の[Ca2+]i に対する作用
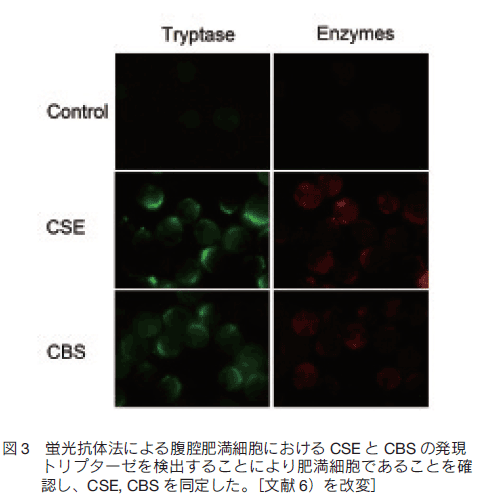
肥満細胞で CBS と CSE が認められた(図 3)。また、 nNOS と eNOS も発現していた 6)。本細胞については H2S に加え、より低濃度で作用を発揮する事が報告されているポリスルフィド 7) の作用を検討した。ポリスルフィドドナーの Na2S4 及び、よりゆっく りと H2S を遊離する GYY4137 により、いずれも容量依存性に[Ca2+]i が上昇し、L-NMMA と cPTIO はこれを抑制した。また DAF-2 によって NO 産生も確認された。このことから、先の二種類の外分泌細胞同様、H2S の作用の一部が、産生された NO によるものであると考えられた。加えて、ポリスルフィドの蛍光プローブである SSP4 を用いて GYY4137 および NO ドナーの DEA NONOate によるポリスルフィド生成の可能性を検討したところ、両者ともに容量依存性にポリスルフィドを生成していた 6)。 H2S と NO 間のみならず、ポリスルフィドも加わった複雑な細胞内現象が [Ca2+]i 動態に関わっているようである。
5.膵島β細胞における H2S の[Ca2+]i に対する作用
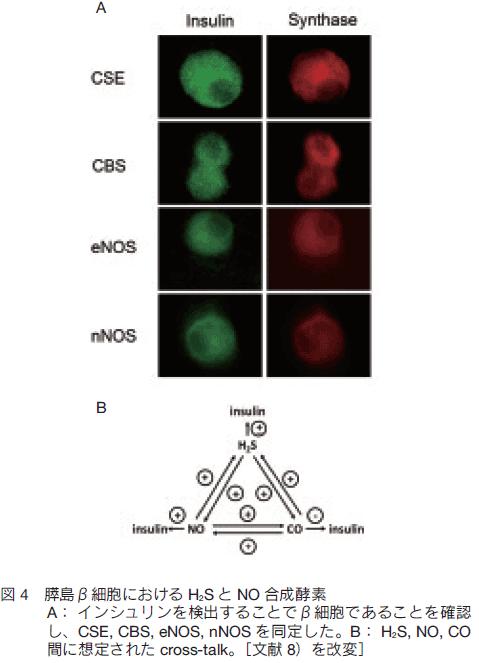
膵島β細胞で、CSE, CBS, eNOS, nNOS の発現が認められた(図 4A)。膵島β細胞でも H2S は[Ca2+]i を上昇させ、L-NMMA はこの上昇を抑制し、H2S による NO 産生も確認された。複雑なことに、H2S の作用は CO 合成酵素抑制物質の SnPP で阻害されたことから CO も関係している可能性が浮かび上がった。実際、ミオグロビンを用いて CO 産生を測定したところ H2S によって容量依存的に CO が産生されていることがわかった。さらに検討を重ねた結果、NO は H2S/ポリスルフィドと CO の産生を、CO は NO と H2S/ポリスルフィドの産生を促すという、たいへん複雑な相互作用が三種類のガス間に存在している可能性が示唆された(図 4B) 8)。NO はインシュリンの基礎分泌を促進し、H2S は有意な効果を示さない一方、CO はむしろ抑制するという三者三様の結果を得ており、分泌に対する作用についても明快な説明は難しい。
6.おわりに
H2S とポリスルフィドは相互変換し、後者は前者の 300 倍生理作用が強い。NO 関連で注目すべきは、H2S は eNOS のシステイン残基を s-スルフヒドリル化して二量体形成を促進し活性化する。
また、PI3K-Akt 経路により eNOS のリン酸化も促進する。このことから NO の産生が促される可能性がある。H2S およびポリスルフィドの作用の一部が NO を経由している可能性がある。H2S と NO からポリスルフィドが生成され、ここに一酸化炭素も加わり、極めて複雑な細胞内 cross-talk がある可能性がある。
| 著者プロフィール | |
| 氏名 | 葉原 芳昭(Yoshiaki Habara) |
|---|---|
| 所属 | 北海道大学 大学院獣医学研究科 比較形態機能学講座 生理学教室 特任教授 |
| 連絡先 | 〒060-0818 札幌市北区北 18 条西 9 丁目 TEL: 011-706-5199 FAX: 011-706-5202 E-mail: habara@vetmed.hokudai.ac.jp |
| 出身大学 | 北海道大学獣医学部 |
| 学位 | 博士(獣医学) |
| 専門分野 | 細胞生理学 |
| 現在の研究テーマ | 内外分泌細胞の分泌機序 |
| 著者プロフィール | |
| 氏名 | ムスタファ アミラ(Moustafa Amira) |
|---|---|
| 所属 | Zagazig University, Faculty of Veterinary Medicine, Department of Physiology, Associate Professor |
| 連絡先 | Zagazig 44519, Egypt TEL: +20-55-228-4283 FAX: +20-55-228-3683 E-mail: al_mrmr@yahoo.com |
| 出身大学 | Zagazig University, Faculty of Veterinary Medicine |
| 学位 | 博士(獣医学) |
| 専門分野 | 生理学 |
| 現在の研究テーマ | ガス性情報伝達物質と細胞内 Ca2+ |