Peroxidase Labeling Kit - SH
抗体・タンパク質標識キット
- アミノ基でうまくいかなかった
- ELISAを組みたい
-
製品コードLK09 Peroxidase Labeling Kit - SH
| 容 量 | メーカー希望 小売価格 |
富士フイルム 和光純薬 |
|---|---|---|
| 3 samples | ¥24,700 | 345-90831 |
| サンプル量 | 50-200 µg |
|---|---|
| 所要時間 | 3時間 |
| 標識部位 | -SH |
| 検出方法 | 顕微鏡・ウエスタンブロット・プレートリーダー |
| 基質 | TMB,DAB等 |
|
・高分子化合物(MW>50,000)および低分子化合物(MW<5,000)を標識できる。 ・SH-Reactive Peroxidaseと混合するだけでPOD標識体を形成する。 ・付属の還元剤を用いることで遊離SH基を持たないタンパク質への標識も可能である*。 ・Filtration tubeを用いた分離操作により高い回収率で標識体が得られる。 ・付属の保存溶液でPOD標識体の保存ができる。 |
|
| 3 samples | ・SH-Reactive Peroxidase ・Reducing Agent ・Solution A ・Solution B ・Reaction Buffer ・Storage Buffer ・Filtration Tube |
3 tubes 3 tubes 4 ml ×1 1 ml ×1 200 μl ×1 4 ml ×1 3 tubes |
|---|
性質
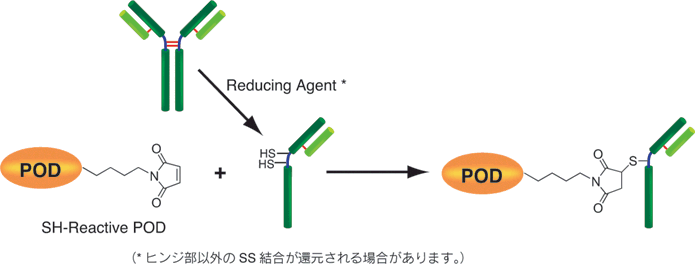
Peroxidase Labeling Kit - SHは、SH基を有する分子にペルオキシダーゼ(POD)を標識するためのキットである。SH-Reactive Peroxidaseは、その構造内にマレイミド基を有しているため、SH基を有する分子と混合するだけで安定な共有結合を形成する。タンパク質がSH基を持っていない場合には、付属の還元剤を用いて遊離SH基を調製することが可能である。(ただし、S-S結合の切断によってタンパク質の活性が失われる場合がある。)IgGヒンジ領域のSH基を標識に利用すれば、抗体活性を損なわずにPODを標識することができる。
IgGのようなタンパク質をサンプルに使用する場合、POD活性を阻害するような低分子のアジ化ナトリウムなどは、付属のFiltration Tubeを用いた前処理によって除去されるため、透析やゲルろ過などの処理は不要である。また、低分子化合物を標識する場合、未反応の低分子化合物はFiltration Tubeを用いた精製操作により除去されるため、高純度のPOD標識体を得ることができる。
| 開発元 | Dojindo Molecular Technologies, Inc. |
|---|
マニュアル
技術情報
特徴
1) 約3時間でPOD標識体が調製できる。
2) 高分子化合物(MW>50,000)および低分子化合物(MW<5,000)を標識できる。
3)50~200 μgのタンパク質を標識可能である。
4) SH-Reactive Peroxidaseと混合するだけでPOD標識体を形成する。
5) 付属の還元剤を用いることで遊離SH基を持たないタンパク質への標識も可能である*。
6) Filtration tubeを用いた分離操作により高い回収率で標識体が得られる。
7) 付属の保存溶液でPOD標識体の保存ができる。
注意事項
|
・ |
Reducing Agentは、還元型のIgG調製に最適化されています。IgG以外のS-S結合を有するサンプルの使用の場合、S-S結合の切断によって標識対象分子の活性が失われる場合があります。還元による失活が起きないことをご確認の上、ご使用下さい。 |
|
・ |
市販の抗体などでゼラチンやアルブミン等を安定化剤として含む場合、それらの成分を除いてからご使用ください。試料中の共存物質の影響については「よくある質問:サンプル溶液中の共存物は反応に影響しますか?」に詳細を記載しておりますのでご参照ください。 |
|
・ |
SH-Reactive Peroxidaseは、アルミラミジップに3本入っています。アルミラミジップを一旦開封した後は、未使用のSH-Reactive Peroxidaseは、アルミラミジップに入れたままチャックをしっかりと閉め、-20℃で保存してください。SH-Reactive Peroxidase以外は、0~5℃で保存してください。 |
|
・ |
冷蔵保存中もしくは室温に戻した際に、フィルトレーションチューブに水滴様の液粒が見られることがあります。これはメンブランの乾燥防止剤が液粒化したもので、製品の性能に問題はございません。 |
|
・ |
本キットには溶液の入ったマイクロチューブのコンポーネントが含まれています。チューブ内壁やキャップに溶液が付着していることがありますので、開封前に振り落としてご使用ください。 |
キット以外に必要なもの
・10 μl, 200 μl マイクロピペッター
・インキュベーター(37℃)
・遠心機(マイクロチューブ用)
・マイクロチューブ(標識体保存用)
反応原理
操作方法
実験例 Peroxidse標識抗体での検出例
抗Tom20抗体をPeroxidase標識後、 固定化、膜透過処理を行ったHeLa細胞に添加し免疫反応後、DAB[code: D006]添加によりミトコンドリアを染色した。
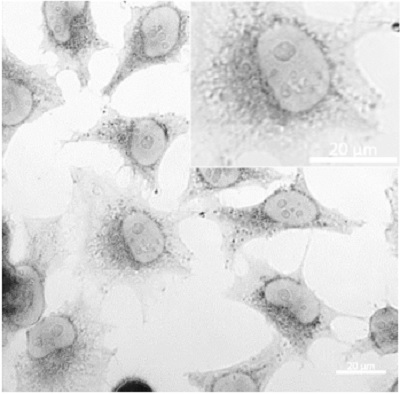 標識済抗体の添加量:2.5µg/ml
標識済抗体の添加量:2.5µg/ml
実験例
Peroxidase Labeling Kit -NH2、Peroxidase Labeling Kit -SHおよび他社品Kitを用いて作製したHRP標識抗ビオチン抗体を用いたELISA
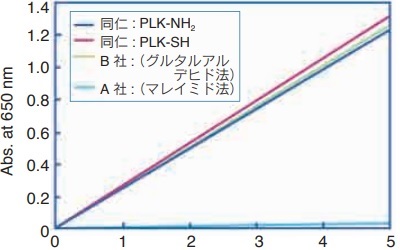
参考文献
1) 広田次郎, 清水眞也, "キットを用いたモノクローナル抗体への迅速・簡便なペルオキシダーゼ標識法", 動物衛生研究所研究報告, 2005, 111, 37.
2) K. Inoue, A. Sugiyama, P. C. Reid, Y. Ito, K. Miyauchi, S. Mukai, M. Sagara, K. Miyamoto, H. Satoh, I. Kohno, T. Kurata, H. Ota, A. Mantovani, T. Hamakubo, H. Daida and T. Kodama, "Establishment of a High Sensitivity Plasma Assay for Human Pentraxin3 as a Marker for Unstable Angina Pectoris", Arterioscler. Thromb. Vasc. Biol., 2007, 27, 161.
3) N. Esaki, Y. Ohkawa, N. Hashimoto, Y. Tsuda, Y. Ohmi, R. H. Bhuiyan, N. Kotani, K. Honke, A. Enomoto, M. Takahashi, K. Furukawa, and K. Furukawa, "ASC amino acid transporter 2, defined by enzyme-mediated activation of radical sources, enhances malignancy of GD2-positive small-cell lung cancer.", Cancer Sci.., 2018, 109, (1), 141.
4) G.W.Zhanga, S.J.Lai, Y.Yoshimura, and N.Isobe, "Messenger RNA expression and immunolocalization of psoriasin in the goat mammary gland and its milk concentration after an intramammary infusion of lipopolysaccharide", Vet. J.., 2014, 202, (1), 89.
5) G-W. Zhang, S-J. Lai, Y. Yoshimura, and N. Isobe, "Expression of cathelicidins mRNA in the goat mammary gland and effect of the intramammary infusion of lipopolysaccharide on milk cathelicidin-2 concentration", Vet. Microbiol.., 2014, 170, (1-2), 125.
6) H. Tateno, S. Saito, K. Hiemori, K. Kiyoi, K. Hasehira, M. Toyoda, Y. Onuma, Y. Ito, H. Akutsu, and J. Hirabayashi, "α2–6 sialylation is a marker of the differentiation potential of human mesenchymal stem cells", Glycobiology., 2016, 26, (12), 1328.
7) K. Iizumi, H. Kawasaki, A. Shigenaga, M. Tominaga, A. Otsu, A. Kamo, Y. Kamata, K. Takamori, and F. Yamakura, "Tryptophan nitration of immunoglobulin light chain as a new possible biomarker for atopic dermatitis", J Clin Biochem Nutr., 2018, 63, (3), 197.
8) K. Morioka, K. Fukai, K. Yoshida, R. Yamazoe, H. Onozato, S. Ohashi, T. Tsuda, and K. Sakamoto, "Foot-and-Mouth Disease Virus Antigen Detection Enzyme-Linked Immunosorbent Assay Using Multiserotype-Reactive Monoclonal Antibodies", J. Clin. Microbiol.., 2009, 47, (11), 3663.
9) M. Watanabe, I. Takemasa, N. Kaneko, Y. Yokoyama, E. Matsuo, S. Iwasa, M. Mori, N. Matsuura, M. Monden, and O. Nishimura, "Clinical significance of circulating galectins as colorectal cancer markers", Oncol. Rep.., 2011, 25, (5), 1217.
10) M. Yasunaga, S. Saijou, S. Hanaoka, T. Anzai, R. Tsumura, and Y. Matsumura, "Significant antitumor effect of an antibody against TMEM180, a new colorectal cancer‐specific molecule", Cancer Sci.., 2019, 110, (2), 761.
11) N. Esaki, Y. Ohkawa, N. Hashimoto, Y. Tsuda, Y. Ohmi, R. H. Bhuiyan, N. Kotani, K. Honke, A. Enomoto, M. Takahashi, K. Furukawa, and K. Furukawa, "ASC amino acid transporter 2, defined by enzyme‐mediated activation of radical sources, enhances malignancy of GD2‐positive small‐cell lung cancer", Cancer Sci.., 2018, 109, (1), 141.
12) N. Hashimoto, K. Hamamura, N. Kotani, K. Furukawa, K. Kaneko, K. Honke, and K. Furukawa,  "Proteomic analysis of ganglioside‐associated membrane molecules: Substantial basis for molecular clustering", Proteomics., 2012, 12, (21), 3154.
"Proteomic analysis of ganglioside‐associated membrane molecules: Substantial basis for molecular clustering", Proteomics., 2012, 12, (21), 3154.
13) N. Kotani, Y. Ida, T. Nakano, I. Sato, R. Kuwahara, A. Yamaguchi, M. Tomita, K. Honke, and T. Murakoshi, "Tumor-dependent secretion of close homolog of L1 results in elevation of its circulating level in mouse model for human lung tumor", Biochem. Biophys. Res. Commun.., 2018, 501, (4), 982.
14) R. Yamashita, N. Kotani, Y. Ishiura, S. Higashiyama, and K. Honke, "Spatiotemporally-regulated interaction between β1 integrin and ErbB4 that is involved in fibronectin-dependent cell migration", J. Biol. Chem.., 2011, 149, (3), 347.
15) T. Noro, E. Oishi, T. Kaneshige, K. Yaguchi, K. Amimoto, and M. Shimizu, "Identification and characterization of haemagglutinin epitopes of Avibacterium paragallinarum serovar C", Vet. Microbiol.., 2008, 131, (3-4), 406.
16) K. Okada, H. Itoh and M. Ikemotob, "Circulating S100A8/A9 is potentially a biomarker that could reflect the severity of experimental colitis in rats', Heliyon, 2020, 6, (2), e03470.
よくある質問
-
Q
Labeling Kitで1次抗体を直接標識する利点を教えてください。
-
A
はじめて抗体標識をされる方を対象としたプロトコルを作成しております。
カスタマーサポートの視点から直接標識法の利点や実施例等を記載しておりますので、ご参照下さい。下記リンクよりダウンロード可能です。
「はじめての抗体標識プロトコル ~カスタマーサポートの視点から~」
-
Q
サンプル溶液中の共存物は反応に影響しますか?
-
A
共存物の種類により影響することがあります。
溶液中にどのような物質が含まれるかを確認の上、状況に応じてラベル化に用いるサンプルの精製を行い、標識反応にご使用ください。<高分子:分子量1万以上>
影響する可能性があります。
高分子でSH基をもつ化合物は、Filtration Tubeでも除くことができません。 そのため標識され、蛍光性不純物として影響します。反応に使用する前に別途精製を行ってください。 一方、SH基を持たない化合物でも、高分子の不純物が多いとフィルターの目詰まりの原因になり、標識・精製操作に支障がでる可能性もあります。
*本製品に限らず他のLabeling kit に関しても同様の注意が必要です。
-
Q
使用できるIgGの量が少量しかありませんが標識できますか?
-
A
本キットでは、標識に必要なIgGの量は50~200 μgとしています。
この範囲であれば性能に大きな違いはありません。
10 μgのIgGでも標識可能ですが、バックグランドの上昇などの問題が生じる可能性があります。
-
Q
サンプルは溶液になっていても問題ないでしょうか?
-
A
問題ありません。
但し、添付のFilitration tubeの容量に制限がありますので、サンプル溶液の容量は100 μl以下である必要があります。
また、サンプルの濃度が0.5 mg/mL以下(50 μg/100 μL以下)である場合は、Filitration tubeを用いてサンプル量が50~200 μgとなるようにして下さい。
溶液をFilitration tubeにいれて遠心して溶液を除く操作を行って下さい(必要であれば繰り返す)。
フィルター上に残っているサンプルの量が50~200 μgとなればよいので、改めて溶解させる必要はありません。*注:低分子の阻害物質は最初の段階で除かれますが、高分子(分子量1万以上)の阻害物質(例;BSA、ゼラチン)は除くことが出来ません。使用前に別途除去してください。
-
Q
低分子のタンパク質(分子量50,000以下)に標識する場合の方法を教えて下さい。
-
A
キット付属のフィルトレーションチューブは分画分子量30Kの限外濾過フィルターのため、余裕をもって50,000以上のタンパク質のご使用を推奨しております。
分子量50,000以下のタンパク質を標識される場合は、下記のような分画分子量の小さい限外濾過フィルターに変更して頂くことで、低分子のタンパク質でもラベル化可能でございます。
-------------------------------------------------------------------
PALL社 ナノセップ 3K 製品No.OD003C33
PALL社 ナノセップ 10K 製品No.OD010C33
-------------------------------------------------------------------キット同梱のフィルターを用いた場合に比べ遠心に時間を要することがございますので遠心時間はご検討下さい。
-
Q
どのようなものが標識できますか?
-
A
分子量が「50,000以上」で[S-S]もしくは[SH]を有しているもの、分子量が「5,000以下」で[SH]を有している化合物(抗体、蛋白質など)であれば標識できます。
分子量が「5,000以下」、「50,000以上」で操作方法が若干異なりますので、製品に添付の説明書をご覧いただき標識反応を行ってください。
-
Q
IgG 1分子に対して、どれくらいのPeroxidaseが標識されますか?
-
A
IgG 1分子に対して平均2~4分子のPeroxidaseが標識されます。
-
Q
標識率は出せますか?
-
A
標識後のサンプル溶液には、未反応のReactive体が含まれるため標識率を算出することはできません。
取扱条件
| 保存条件: 冷蔵 , 取扱条件: 吸湿注意 |