細胞機能解析における「Click-to-Release」反応の可能性
株式会社同仁化学研究所 吉村 建司
生きた細胞内で特定の分子や反応を時空間的に制御することは、生命現象の理解や創薬研究において重要な課題である。しかし、細胞内環境は極めて複雑であり、通常の化学反応をそのまま適用すると、生体分子との非特異的な副反応や細胞機能の錯乱を引き起こす恐れがある。これらの問題を克服する概念として「生体直交化学(bioorthogonal chemistry)」が提唱され、生体分子と干渉しない選択的反応の開発が進められてきた1, 2, 3)。
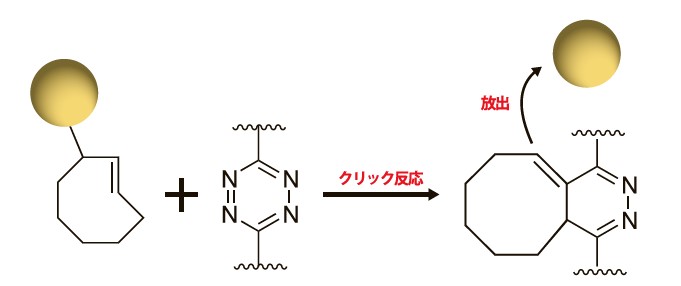
この分野の発展を支えてきた代表的手法が「クリックケミストリー(click chemistry)」である4)。Sharplessらにより提唱された本概念は、高効率・高選択性・操作の簡便性を特徴とする反応群を指し、主として分子間の共有結合形成を目的として利用されてきた。近年、このクリックケミストリーの概念は「結合」から「切り離し」へと拡張され、「click-to-release」反応として新たな展開を見せている5)。この反応は、「クリックケミストリー」を化学的トリガーとして利用し、標的分子の放出・活性化の時空間的な制御を可能にしており(図1)、近年、抗体-薬物複合体(ADC)やプロドラッグ設計などのドラッグデリバリー分野への広がりを見せている6, 7)。そこで本稿では、「click-to-release」反応を利用した細胞機能解析への応用例について紹介する。
樹状細胞(DCs)は、CD1d受容体を介して外因性糖脂質抗原を提示し、不変型ナチュラルキラー T 細胞(iNKT細胞)を活性化する。また、DCsはMHC-I分子を介して外因性ペプチド抗原を交差提示し、CD8+ T細胞を活性化する。これら外因性抗原はエンドサイトーシスによってDCs内に取り込まれるものの、取り込み後に抗原提示へ至る過程でリソソームをどの程度経由するのかについては長らく明らかでなかった。この問題を解決するために、Ligthartらは「click-to-release」反応を利用して、外因性の糖脂質抗原およびペプチド抗原が抗原提示の過程でリソソームを通過するか否かを検証した8)。
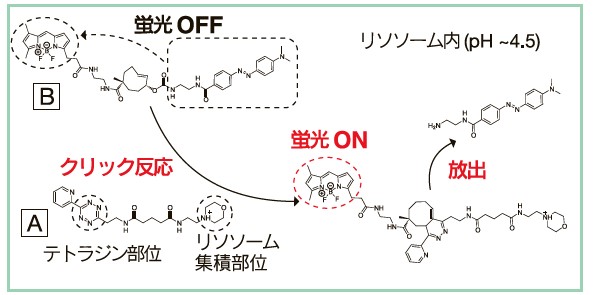
著者らはまず、リソソームに選択的に集積するテトラジン誘導体を新たに設計した(図2,A)。このテトラジン誘導体のリソソーム集積性を確認するため、蛍光色素を導入したtrans-cyclooctene(TCO)誘導体を作成した(図2,B)。この誘導体は、放出分子として消光基が導入されており、この分子自体は無蛍光であるが、テトラジンと反応すると消光基が脱離し、蛍光を発するプローブである。あらかじめリソソーム集積性のテトラジン誘導体を添加した細胞に、このTCO誘導体を導入したところ、リソソームに蛍光が観察された。この結果は、開発したテトラジン誘導体が細胞内のリソソームに選択的に集積し、リソソーム内でTCO誘導体と「click-to-release」反応を惹起できることを示している(図2)。
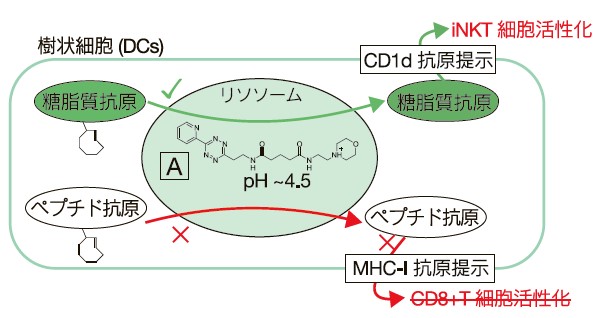
その後、著者らは糖脂質抗原またはペプチド抗原を放出分子として結合させたTCO誘導体を作製した。この抗原-TCO誘導体は、TCOが結合した状態ではDCsによって抗原提示されず、それぞれiNKT細胞やCD8+ T細胞を活性化しないことが確認されている。これらの抗原-TCO誘導体を、リソソーム集積性テトラジン誘導体を導入した細胞に添加したところ、糖脂質抗原においてはiNKT細胞の活性化が観察されたが、ペプチド抗原ではCD8+ T細胞の活性化は観察されなかった。これらの結果は、糖脂質抗原は抗原提示過程でリソソームを通過する一方、ペプチド抗原はリソソームを経由しないことを示している(図3)。
本稿で取り上げた研究は、リソソームを標的とした「click-to-release」反応設計により、DCsにおける外因性抗原処理経路について、リソソームをどの程度経由するのかを解明した。このように特定の細胞小器官に「click-to-release」反応を適用する技術は、より複雑な細胞機能の解析を進展させる新しい手法として、今後さらなる応用と発展が期待される。
[参考文献]
- E. M. Sletten et al., “Bioorthogonal Chemistry: Fishing for Selectivity in a Sea of Functionality”, Angew. Chem. Int. Ed., 2009, 48(38), 6974-6998.
- C. R. Bertozzi, “A Decade of Bioorthogonal Chemistry”, Acc. Chem. Res., 2011, 44(9), 651-653.
- R. Chaudhuri et al., “Bioorthogonal Chemistry in Translational Research: Advances and Opportunities”, Chem. Bio. Chem., 2023, 24(23), e202300474.
- H. C. Kolb et al., “Click Chemistry: Diverse Chemical Function from a Few Good Reactions”, Angew. Chem. Int. Ed., 2001, 40(11), 2004-2021.
- R. M. Versteegen et al., “Click to Release: Instantaneous Doxorubicin Elimination upon Tetrazine Ligation”, Angew. Chem. Int. Ed., 2013, 52(52), 14112-14116.
- R. Rossin et al., “Chemically triggered drug release from an antibody-drug conjugate leads to potent antitumour activity in mice”, Nat. Commun., 2018, 9(1484).
- J. M. Mejia Oneto et al., “In Vivo Bioorthogonal Chemistry Enables Local Hydrogel and Systemic Pro-Drug To Treat Soft Tissue Sarcoma”, ACS Cent. Sci., 2016, 2(7), 476-482.
- S. T. Ligthart et al., “A Lysosome-Targeted Tetrazine for Organelle-Specific Click-to-Release Chemistry in Antigen-Presenting Cells”, J. Am. Chem. Soc., 2023, 145(23), 12630-12640.

