N-オキシド化学に基づく二価鉄蛍光プローブの開発
Development of N-oxide chemistry-based ferrous ion fluorescent probes

平山 祐
岐阜薬科大学
創薬化学大講座
ケミカルバイオロジー研究室
教授
Abstract
Iron is vital yet toxic in excess, triggering ferroptosis via reactive oxygen species generation 1). To visualize labile Fe2+ dynamics, we developed reaction-based turn-on fluorescent probes utilizing N-oxide chemistry, where Fe2+ selectively reduces a non-fluorescent N-oxide moiety. The N-oxide chemistry, initiated with RhoNox-1, was expanded to target specific organelles, revealing significant Fe2+ accumulation in the endoplasmic reticulum (ER) and lysosomes during ferroptosis. We also established the highly sensitive probe RhoNox-4 (FerroOrange), which has enabled high-throughput screening for iron-modulating compounds. Notably, because the N-oxides selectively oxidize Fe2+ to Fe3+, probes localizing to the ER and lysosomes were found to effectively inhibit ferroptosis, highlighting their utility as both imaging tools and biological modulators.
1. はじめに
鉄は、人体のみならずほとんどの地球上の生命体において最も多く存在する遷移金属元素である。酸素運搬やエネルギー産生など、必須の役割を担いつつも、過剰な鉄イオンは、酸化ストレスをもたらすことから、その濃度は厳密に制御されている1)(図1)。そのため、鉄代謝異常は多くの重度疾患との関連が報告されており2)、さらに2012年には鉄依存的細胞死(フェロトーシス)といった、鉄が起点となる細胞死が報告されている3)。二価鉄は、フェントン反応: Fe(II) + H2O2 (or L-OOH, Lは脂質) → Fe(III) + HO• (L-O•) + HO− により、非常に高反応性のヒドロキシルラジカルや脂質ラジカルを生成することが知られており、本反応が酸化ストレスにおける細胞傷害の根源となっている4)(図1)。また、細胞内における鉄イオン輸送は二価鉄の状態で行われており、生細胞中において二価鉄を検出することは、細胞内鉄代謝だけでなく、酸化ストレスの理解を深める上でも重要な課題の一つであった。本稿では、筆者らが開発してきた二価鉄検出用蛍光プローブについて、その原理と応用例について紹介する。
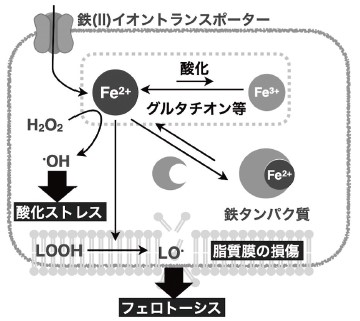
ヒト細胞では鉄トランスポーターや鉄シャペロンタンパク質は二価鉄を認識する。また、細胞内が還元的環境であることから輸送の中心は二価鉄である。同時に、フェントン反応により酸化ストレスを生じさせるのも二価鉄である。
2. N-オキシド化学を使った各種二価鉄蛍光プローブ
2.1 初の蛍光増大型二価鉄蛍光プローブ RhoNox-1
鉄イオンが強力な蛍光消光作用を持つことから、キレート効果に基づく蛍光プローブでは、蛍光応答様式が消光型となることを避けられない5)(図2.1)。そこで化学反応を使った分子設計を採用することにした。化学反応型の蛍光プローブは、活性酸素種等、反応性の生体内化学種の検出によく使われている(図2.2)が、金属イオンとの化学反応を使用した蛍光プローブは当時まだ限定的であった5)。満たすべき要件は①二価鉄選択的に進行する反応であること、②蛍光が増大するものであること、③細胞内環境(水溶液中)で反応が起こることの3つである。鉄を使った化学反応自体は無数に存在するものの、上記の3要件を満たすものとなると限られてくる。筆者は、第三級アミンN-オキシド(以下、N-オキシド)という化合物群が、鉄により還元的に三級アミンに変換される反応が、水溶液中でも進行することに着目し、これを蛍光団(ローダミンB)に組み込んだ化合物RhoNox-1を合成した(図3.1)。RhoNox-1は、水溶液中にて二価鉄選択的に蛍光強度の増大を示し(図3.2、3.3)、また、生細胞イメージングにおいても二価鉄に応答することがわかった(図3.4)。本化合物は、世界初の二価鉄選択的かつ蛍光増大型の蛍光プローブとして報告した6)。
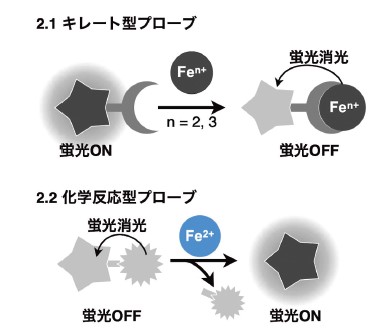
2.1 キレート型蛍光プローブは鉄イオンとキレートを形成することで蛍光がOFFになる。例としてCalceinやPhenGreen-SKがある。
2.2 化学反応プローブでは、蛍光がOFFになるように反応基を導入し、それが二価鉄と反応することにより除去され、蛍光がONになる。
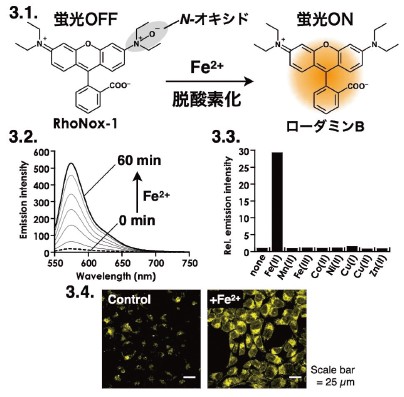
3-1. RhoNox-1の構造と作用機序。二価鉄によりN-オキシド部が脱酸素化を受け、蛍光がONになる。
3-2. RhoNox-1に二価鉄を添加した際の蛍光スペクトル変化。励起波長:540 nm。
3-3. RhoNox-1の金属イオン選択性試験。二価鉄を加えた際のみ蛍光強度が増大する。
3-4. RhoNox-1を使った生細胞二価鉄イメージングの例。
2.2 N-オキシド化学の展開:多色化と多機能化
ローダミンBの蛍光性は、窒素原子上の孤立電子対が非局在化したπ共役系によりもたらされる。N-オキシド化によりこの非局在化が阻害されると、蛍光強度が減弱し、二価鉄により脱酸素化が起こると蛍光が回復するという仕組みになっている。このことから、RhoNox-1の蛍光OFF/ON原理は類似の性質を持つキサンテン系色素やアミノクマリン系蛍光色素にも拡張できる。筆者らは、ローダミンB同様に、窒素原子を含むπ共役系を持つクマリン、ロドール、ケイ素ローダミンをN-オキシド化した化合物を合成し(それぞれ、CoNox-1、FluNox-1、およびSiRhoNox-1)(図4.1)、二価鉄への蛍光応答を確認したところ、これらプローブ群はすべて、水溶液中、生細胞いずれにおいても二価鉄に対して蛍光増大を示した(図4.2)。この中でSiRhoNox-1が深赤色蛍光での観察が可能であることを利用して、スフェロイド中心部では低酸素状態により二価鉄濃度が上昇していることを明らかにした7)(図4.3)。筆者らはさらなる多機能化の例として、細胞内小器官局在化について検討した。現在、ターゲッティングに成功している小器官は、ミトコンドリア8)、リソソーム9)、小胞体7)、ゴルジ体10)、および細胞膜11)である(図5)。このうち、ミトコンドリア、リソソーム、小胞体を標的とした蛍光プローブ(それぞれ、Mito-FluNox、Lyso-RhoNox、SiRhoNox-1)は、蛍光応答性が同レベルであり、かつ、励起・蛍光波長が互いに異なることから、蛍光顕微鏡観察にて同時に使用することができ、上記3つの蛍光プローブカクテルを使った同時多色イメージングにて各小器官での二価鉄検出に成功している12)。フェロトーシス(鉄依存的細胞死)においては、二価鉄量が上昇することは、他のグループから報告されていたものの、小器官レベルでの二価鉄動態は不明であった。そこで、本イメージング法をフェロトーシスへと応用したところ、リソソーム、小胞体にて二価鉄が上昇していることが明らかになった12)(図6)。フェロトーシスでは脂質過酸化・損傷が細胞死に重要なプロセスであるが、他のグループからも小胞体13)およびリソソーム14)において脂質過酸化が進行していることが報告され、筆者らの観察結果と良く一致しており、現在はこれらの小器官がフェロトーシスにおける過酸化脂質発生の場であることが示唆されている。
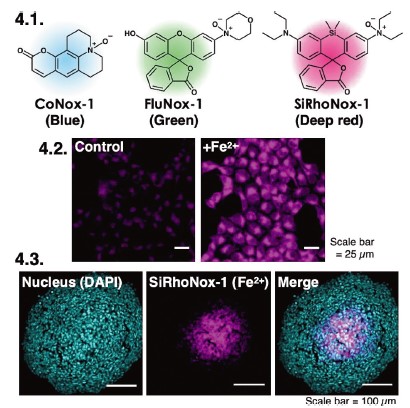
4-1. 青色、緑色、深赤色二価鉄蛍光プローブの構造と励起・蛍光波長。これらプローブはRhoNox-1と同等かそれ以上の蛍光応答を示す。
4-2. SiRhoNox-1を使った生細胞二価鉄イメージングの実例。
4-3. スフェロイド培養したHepG2細胞の二価鉄蛍光イメージング。一定の大きさ以上のスフェロイドでは中心部が低酸素状態になっていることが知られている。酸素濃度の低い部位にて二価鉄濃度が上昇していることが分かった。
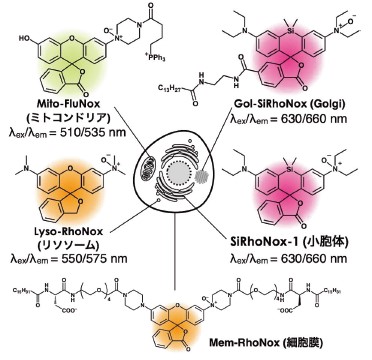
ミトコンドリア、ゴルジ体、リソソーム、小胞体、および細胞膜局在型蛍光プローブの構造と励起・蛍光波長。
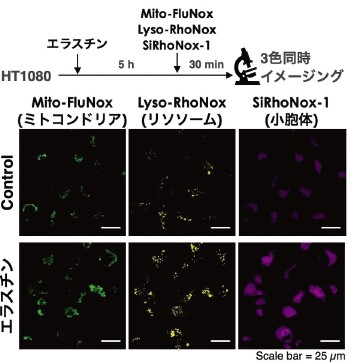
エラスチンによりフェロトーシスを誘導し、Mito-FluNox(ミトコンドリア)、Lyso-RhoNox(リソソーム)、SiRhoNox-1(小胞体)を同時に使用し、三色同時に二価鉄イメージングを実施した。
これまでの蛍光プローブと少し異なる性能を示すのが膜局在型二価鉄蛍光プローブMem-RhoNoxである11)。本プローブは、膜アンカリングのためのパルミトイル基が、ローダミン-N-オキシド構造の両端に導入されている(図5)。アスパラギン酸を間に挟むことで膜透過による細胞内移行を防ぎ、二価鉄検出部位が細胞膜の外側を向くように設計してある(図7.1)。本化合物は、トランスフェリンによる鉄取り込みをリアルタイムで可視化すること、および、同鉄取り込み過程において、エンドソーム内で三価鉄が二価鉄に還元されることを明らかにするべく、設計・開発した。プローブで処理したHepG2細胞(ヒト肝がん細胞)にトランスフェリンを処理したところ、直後5分以内に蛍光性の輝点が次々に出現した(図7.2)。本現象はエンドサイトーシスの阻害薬(アジ化ナトリウム)、エンドソーム酸性化阻害薬(塩化アンモニウム)、鉄キレート剤(デフェロキサミン、DFO)で抑制され、さらに、マンガントランスフェリン(三価鉄の代わりに二価マンガンが結合したもの)では蛍光シグナルの上昇は確認されなかったことから、トランスフェリンによる鉄取り込み時には、エンドソーム内での還元反応により二価鉄が生成することを明らかにすることができた。さらに、本プローブを初代培養神経細胞に応用し、同様にトランスフェリンを使ったイメージングから、神経細胞ではスパイン様の構造体において鉄取り込みが亢進していることが示唆された(図7.3)。
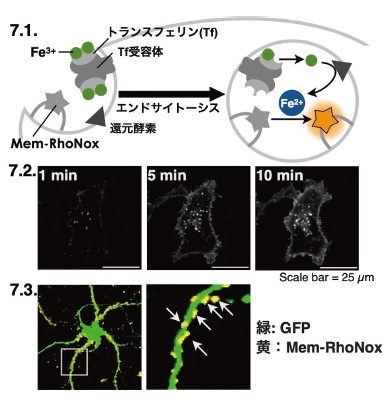
7-1. トランスフェリン(Tf)による鉄取り込み経路と、Mem-RhoNox の作用機序。プローブがエンドサイトーシスによりTf と同時に取り込まれ、エンドソーム内で生じる二価鉄と反応して蛍光を示す。
7-2. HepG2細胞にMem-RhoNoxを作用させ、Tfを加えた際のタイムラプスイメージング。5分後には細胞内に輝点が多く発生している様子がわかる。
7-3. マウス初代培養神経細胞にMem-RhoNoxを作用させ、Tfを加えた30分後のイメージング画像。左:神経細胞一細胞。右:左画像の四角部を拡大したもの。神経細胞の細胞室は緑色蛍光タンパク質(GFP)にて染色(緑色)。プローブのシグナルは黄色にて描画。神経突起に沿って輝点が確認される(矢印)。
2.3 超高感度二価鉄蛍光プローブ RhoNox-4 の開発
RhoNox-1はプロトタイプとしては十分な性能を発揮していたものの、その蛍光応答性、特に細胞イメージングにおける応答性には改善の余地があった。そこで、多機能化と同時に、高感度化にも取り組んだ。N-オキシド化学の拡張について検討している際、環状アミン構造を持つローダミン系色素のN-オキシド化体が、比較的蛍光応答性が良くなる傾向を見出していた。そこで、様々な環状アミンN-オキシド構造を有する誘導体群(RhoNox-2~RhoNox-8)を合成(図8.1)し、これらの二価鉄応答性を水溶液中および生細胞にて評価した。すべての環状アミン型プローブはRhoNox-1(鎖状アミン型)に比較して反応速度、蛍光強度増大比ともに向上したが、特にRhoNox-4、RhoNox-7、及びRhoNox-8が15分以内に100倍を超える蛍光強度の上昇を示し、これらが有用な候補化合物となった。生細胞イメージングに応用したところ、RhoNox-4が他を圧倒的に凌駕する蛍光応答を示した15)(図8.2)。RhoNox-4を使った二価鉄イメージングは条件検討がほぼ不要なレベルであり、その鋭敏かつ堅実な応答性を利用し、筆者らは、かねてより検討していた、「鉄摂動化合物」探索のためのハイスループットスクリーニング(HTS)を実施した。東京大学創薬機構より供与いただいた3399化合物について、3回のスクリーニング・対照実験を繰り返した結果、lomofunginを見出した。まだ作用機序解析の途中であるが、lomofunginの処理により細胞内のフェリチン量が減少することがわかっており、鉄貯蔵タンパク質であるフェリチンの分解が促進されることにより、遊離の二価鉄が上昇したものと考えられる。この超高感度二価鉄蛍光プローブRhoNox-4は、FerroOrangeという名称にて同仁化学より販売されており、フェロトーシス研究の隆盛もあいまって、これまでに2000報を超える研究論文に貢献している(2025年11月、Google Scholar調べ)。
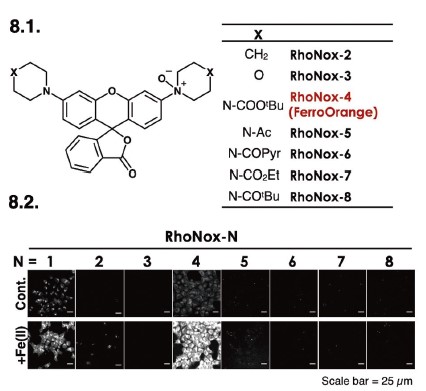
8-1.高感度化に向けた構造活性相関と各プローブの構造。
8-2.各プローブを使った生細胞二価鉄イメージングの結果。RhoNox-4が圧倒的に良好な応答を示した。
2.4 N-オキシド型蛍光プローブのフェロトーシス阻害作用
N-オキシド化学を使った蛍光プローブは、「化学反応型」であるが、二価鉄による脱酸素過反応では、プローブ側から酸素原子が除去されるため、還元されることになる。このことから、二価鉄側は酸化されていると予想される。そこで、鉄イオンの酸化状態を決定すべく、X-ray absorption near edge structure(XANES)スペクトルを測定したところ、予想通り、N-オキシドとの反応後、二価鉄は三価鉄に酸化されていることがわかった16)。フェロトーシスにおいては、過酸化脂質と二価鉄の反応により、ラジカル連鎖反応が進行することが、最終的な細胞死のトリガーとなる(図9.1)。N-オキシド型蛍光プローブの二価鉄選択性の高さを考慮すると、これらプローブ群は、細胞内において二価鉄を三価鉄へと変換できる可能性がある。実際、九州大学の池田らは、Mito-FerroGreen(Ac-Mito-FluNox)が、ドキソルビシンにより誘発されるミトコンドリア傷害型のフェロトーシスを阻害する効果があることを報告していた17)。そこで筆者らは、これまで開発してきた一連のN-オキシド型蛍光プローブについて、フェロトーシス阻害活性を評価した。エラスチンにてフェロトーシスを誘導し、各プローブの濃度を変えて共存させたところ、RhoNox-1、SiRhoNox-1、RhoNox-4、およびLyso-RhoNoxが、1 μM 前後のIC50値にてフェロトーシスを阻害することがわかった(図9.2)。これは、鉄キレート薬デフェロキサミン(DFO)による阻害効果と同等、あるいはやや強い効果であった。エラスチンはシスチントランスポーター(System Xc−)を阻害することでフェロトーシスを誘導するが、作用点の異なるフェロトーシス阻害薬RSL-3(グルタチオンペルオキシダーゼ 4、GPx4阻害)、FIN56(GPx4阻害)、FINO2(二価鉄によるラジカル反応活性化)に対しても阻害効果を示した。一方で、スタウロスポリン等、アポトーシス・ネクローシスの誘導時には全く効果がなく、フェロトーシス選択的な阻害作用が確認された。さらに興味深いことに、Mito-FerroGreenや、H-FluNox(N-オキシドを使ったヘム蛍光プローブ)、Mem-RhoNoxはフェロトーシス阻害作用が無く、上述の4つと活性の差があることがわかった。RhoNox-1、SiRhoNox-1、RhoNox-4、およびLyso-RhoNoxは、小胞体あるいはリソソームに局在が見られることが特徴であり、既出のとおり、小胞体とリソソームはフェロトーシス誘導時において二価鉄の蓄積が見られた小器官である。また、既出のとおり、これらの小器官では脂質過酸化が亢進していることが報告されており、当該小器官への局在性を持つプローブ群が効果的であったことは、たいへん興味深い。また、N-オキシド化学とならんで、二価鉄蛍光プローブ開発に使用されるエンドパーオキシド化学は、FINO2で見られるようにフェロトーシス誘導作用があることがわかっている17, 18)。両者とも二価鉄との反応性を有するものの、フェロトーシスに対する効果が正反対である。現在、この活性の差についてはよくわかっていないが、細胞内の局在や反応する二価鉄の成分が異なるものと推察される。
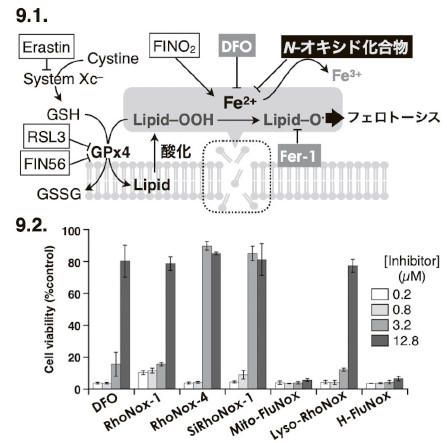
9-1. 各種フェロトーシス誘導薬と作用機序。GSH:グルタチオン、GSSG:酸化型グルタチオン、GPx4:グルタチオンペルオキシダーゼ 4、DFO:デフェロキサミン、Fer-1:Ferrostatin-1。黒文字+黒枠:フェロトーシス誘導薬。白文字化合物:フェロトーシス阻害薬
9-2. 各 N-オキシド化合物のフェロトーシス阻害作用。エラスチンと同時に各濃度のプローブを投与し、細胞生存率を測定したところ、RhoNox-1、RhoNox-4、SiRhoNox-1、Lyso-RhoNox にて阻害効果が見られた。
3. おわりに
本稿では、筆者らが開発してきた二価鉄蛍光プローブとその応用について概説させていただいた。奇しくもフェロトーシスの報告(2012年5月)と初のN-オキシド型二価鉄蛍光プローブRhoNox-1の報告(2012年12月)が同時期であったことは不思議な縁を感じる(筆者が一方的に感じているだけである)。また、今回紹介させていただいた蛍光プローブのうちいくつかは下記の名称にて市販されているので、容易に入手可能になっている(RhoNox-4: FerroOrange、Mito-FluNox: Mito-FerroGreen、Lyso-RhoNox: Lyso-FerroRed、SiRhoNox-1: FerroFarRed)。 現在は細胞レベルのイメージングが主流であるが、マウスをはじめとする個体への応用ができる新たなプローブ開発が進めば、フェロトーシスを含む鉄の関与する生命科学の理解がより深まると期待される。
最後に、本稿で紹介した筆者らの研究は、位田雅俊教授、保住功教授(岐阜薬科大学薬物治療学研究室)、王丹准教授(当時、京都大学iCeMS)、野澤俊介准教授(高エネルギー加速器研究機構)との共同研究の成果であり、この場を借りて深く感謝申し上げる。
| [ 著者プロフィール ] | |
| 氏名 | 平山 祐(Tasuku Hirayama) |
|---|---|
| 所属 |
岐阜薬科大学 創薬化学大講座 ケミカルバイオロジー研究室 〒501-1196 岐阜市大学西 1-25-4 |
| 出身学校 | 京都大学大学院人間・環境学研究科 |
| 学位 | 博士(人間・環境学) |
| 専門分野 | ケミカルバイオロジー |
| 現在の研究テーマ | 鉄のケミカルバイオロジー研究 |

