Biofilm Viability Assay Kit

バイオフィルム薬剤効果測定キット
- バイオフィルム内微生物の生存率や活性度合を確認できる
- 測定の手間を大幅に低減
- バラツキを抑えることが可能
-
製品コードB603 Biofilm Viability Assay Kit
| 容 量 | メーカー希望 小売価格 |
富士フイルム 和光純薬 |
|---|---|---|
| 96 tests | ¥23,200 | 347-09583 |
・独自開発の蓋(TestPiece Holder)で、任意の素材をを簡便に測定できます
| 96 tests | ・WST Solution ・Electron Mediator Reagent ・96-peg lid ・96-well Plate |
1 ml×1 0.12 ml×1 ×1 ×10 |
|---|
|
令和2年度 九州・沖縄 産業技術オープンイノベーションデーにてポスター発表されました。
|
|
公益財団法人 日本分析化学会 機関紙「ぶんせき」に本技術が掲載されました。 |
性質
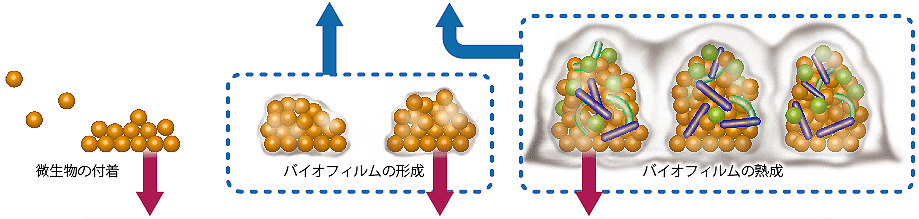
バイオフィルムは、微生物とその代謝物である細胞外多糖から構成される集合体で、あらゆる環境に存在しています。近年、バイオフィルム形成阻害能を有する薬剤や、食品成分の探索が注目を集めています。
バイオフィルム薬剤効果測定キット(Biofilm Viability Assay Kit)は、バイオフィルム形成から測定にピンプレートを用いた操作を採用し、必要なコンポーネントが1つにまとまっています。
マニュアル
技術情報
測定原理
本キットはバイオフィルム内の生菌の代謝活性を測定することで、バイオフィルム内微生物に対する薬剤効果を確認するキットです。エネルギー代謝活動に関与する補酵素であるNADH(NADPH)は電子メディエーターを介してWSTを有色のformazanへと還元します。この還元能を利用することで微生物の代謝活性を検出します。
.png)
操作
蓋に固定されたピン(PEG)にバイオフィルムを形成させるため、洗浄・発色操作によりバイオフィルムが剥がれることがなく、多検体を簡便に測定することが可能です。
.png)
目的に応じた2種類のキット
同一の測定手法でバイオフィルムの形成量、またはバイオフィルムに含まれる生菌の代謝活性を測定するキットを取り揃えております。
ご利用の目的に応じてキットをご選択ください。
| バイオフィルム(生菌+死菌+細胞外高分子物質)の総量 |
| バイオフィルム形成量・形成阻害測定キット Biofilm Formation Assay Kit(関連製品) |
| Biofilm Formation Assay Kitはクリスタルバイオレット(CV)染色法によりバイオフィルム形成量および薬剤のバイオフィルム形成阻害を測定することができます。 |
 |
| 菌等の増殖活性 |
| バイオフィルム薬剤効果測定キット Biofilm Viability Assay Kit(本製品) |
| Biofilm Viability Assay Kitはバイオフィルム内の生菌の代謝活性をWST法により測定することで、バイオフィルム内の微生物に対する薬剤の殺菌効果を確認することができます。 |
2種類のキットの選び方
※ バイオフィルムの形成条件は菌種や株によって異なります。まず、形成条件の検討にBiofilm Formation Assay Kit(関連製品)をご利用ください。 |
測定例
バイオフィルムに対する薬剤の形成阻害や抗菌効果の指標としては、MBIC(minimum biofilm inhibitory concentrations):最小バイオフィルム形成阻害濃度や、MBEC(minimum biofilm eradication concentrations):最小バイオフィルム撲滅濃度が指標として用いられています。S. aureusについて、各キットでMBICならびにMBECを測定しました。
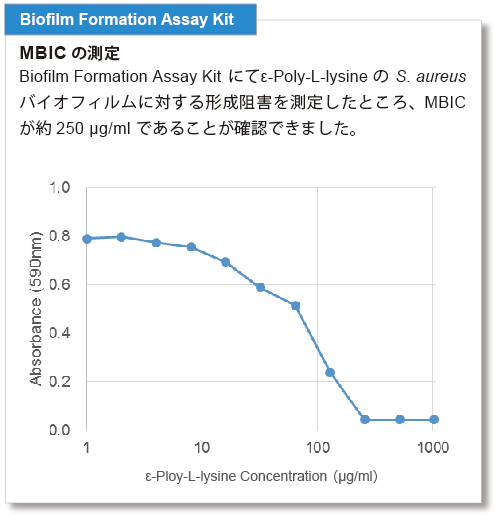
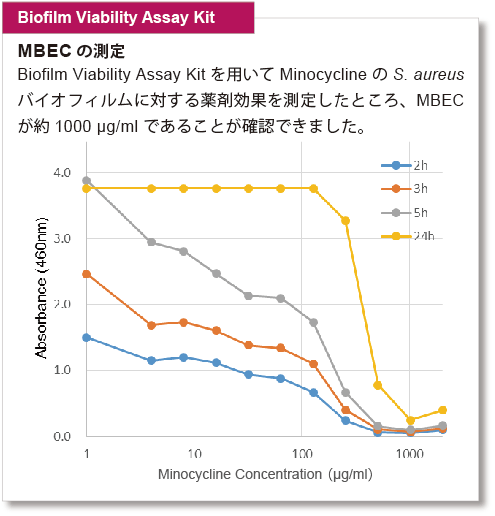
※実験の条件は取扱説明書に記載しておりますので、ご参照ください。
その他ラインナップの紹介
試験片用バイオフィルム形成能測定キット
Biofilm TestPiece Assay Kit (製品コード B606)
様々な素材の試験片を用いて、各素材に対するバイオフィルム形成能を評価する場合に最適なキットです。
本製品は、独自の技術であるTestPiece Holderを用いることで、既存法と比較してデータのバラツキ(再現性の低さ)と測定の手間を大幅に改善することが可能です。


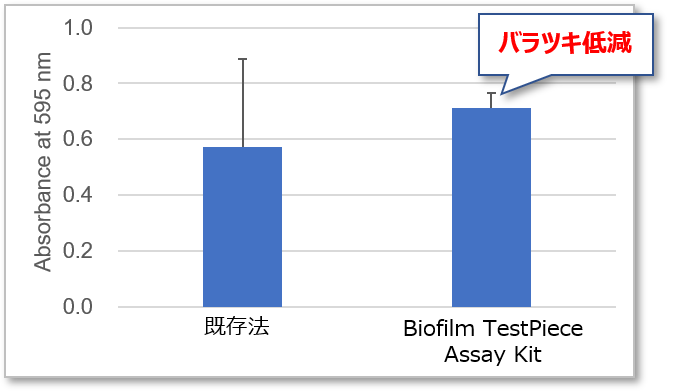
クリスタルバイオレット法によるばらつきの比較
菌種:Staphylococcus aureus NBRC13276
各 n=8の平均
参考文献
1) 古畑勝則, "Legionella pneumophilaの実験的バイオフィルム形成条件の検討", Bacterial adherence & Biofilm., 2019, 33, 39-42.
2) Y. Sato, T. Ubagai, S. T.-Nagakawa, Y. Yoshino, Y. Ono, "Effects of colistin and tigecycline on multidrug-resistant Acinetobacter baumannii biofilms: advantages and disadvantages of their combination", Sci. Rep.., 2021, 11, 11700. doi:10.1038/s41598-021-90732-3.
よくある質問
-
Q
発色試薬添加後のインキュベートはどのくらい行えばいいですか?
-
A
微生物種や代謝活性により、発色に要する時間は異なります。
初回は一定時間ごとに吸光度を確認しながら、24時間ほどインキュベートされる事をお勧めします。
取扱説明書の図2および図3にS.aureus、S.mutansを用いた実験例を掲載してます、ご参照ください。
-
Q
450 nm以外のフィルターで測定することは可能ですか?
-
A
440~480 nmの範囲に入るフィルターをご利用いただけます。
-
Q
バイオフィルムの形成阻害や薬剤効果を評価するには、どの程度のバイオフィルム形成量が必要ですか?
-
A
Biofilm Formation Assay Kit(製品コード:B601)を利用した場合、測定手順の最後に得られるクリスタルバイオレット(CV)溶液の吸光度として、0.5以上(590 nm)を目安としております。
-
Q
どのような菌種での測定実績がありますか?
-
A
小社ではBiofilm Formation Assay Kit(製品コード:B601)ならびにBiofilm Viability Assay Kit(本製品)を用いたバイオフィルムの評価において、以下の菌種での評価実績がございます。
・Staphylococcus aureus(黄色ブドウ球菌)
・Pseudomonas aeruginosa(緑膿菌)
・Escherichia coli(大腸菌)
・Streptococcus mutans(虫歯の原因菌のひとつ)
・Porphyromonas gingivalis(歯周病の代表的な原因細菌)上記の細菌を用いた実験例や培養条件等は、取扱説明書をご参照ください。
取扱条件
| 保存条件: 冷蔵 | |
|
危険・有害 シンボルマーク |

|
|---|---|



















