|
| トップページ > 新しいナノ材料としてのカーボンナノチューブ |
 |
|
連載
|
| -最近の展開(バイオからエネルギーまで) ③ 中嶋 直敏、福丸 貴弘、藤ヶ谷 剛彦 九州大学 |
1 . カーボンナノチューブ複合材料創製(機能材料創製)
第 3 回はカーボンナノチューブ(CNT)と他の材料(有機分子、高分子、金属ナノ粒子、バイオ分子)との複合による新しい CNT 複合材料体のデザイン、創成について、in vitro および in vivo バイオアプリケーション研究を含め紹介する。
1-1. CNT と合成高分子との複合化
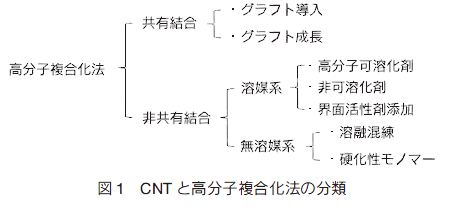
高分子と CNT との複合化ではファイバー、フィルムや塗布膜など固体状態での応用展開が主に進められている。ここで CNT はフィラーとみなすことができるが、他の無機・金属フィラーと異なり、CNT では、共有結合で複合化させる手法を用いることもできる(図 1)。
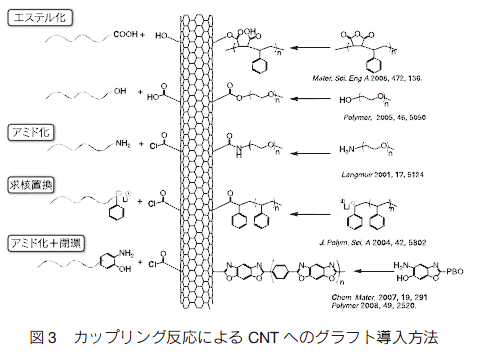
共有結合による複合化法としては、あらかじめ合成した高分子を CNT にグラフトさせる「グラフト導入(grafting ‘to’)法」、及び CNT から高分子鎖を成長させる「グラフト成長(grafting ‘from’)法」などが試みられている。「グラフト導入(grafting ‘to’)法」としては、CNT への直接付加であるラジカル付加 1) や環化付加 2) の利用(図 2)や、酸化処理 CNT に導入された OH 基や COOH 基へのカップリング利用が挙げられる(図 3)。カップリングは、ポリマー鎖末端官能基のみならず側鎖に官能基がある場合でも可能である。高分子/CNT 界面の相互作用は、複合化物そのものの物性に大きな影響があるため、複合化に用いる CNT の純度、マトリックス高分子との結合形成の化学的な評価が極めて重要である。
「グラフト成長(grafting ‘from’)法」は、CNT 表面に重合開始点を CNT 上に導入し、そこから重合を開始させる手法である(図 4)。最も報告例が多いのはリビングラジカル重合の一種である Atom Transfer Radical Polymerization(ATRP)法や、Reversible Addition Fragmentation Chain Transfer (RAFT)法である。 ATRP 法ではスチレンの他、メタクリレート誘導体、N- イソプロピルアクリルアミド、およびそれらのブロック共重合体などの重合が報告されている 3)。また RAFT 法ではスチレン、アクリルアミド、N- イソプロピルアクリルアミドなどが用いられる。これらの修飾法は、これまで種々の基板表面で確立されていた反応重合開始剤導入法をそのまま CNT 表面に適用できるため利便性も高い。
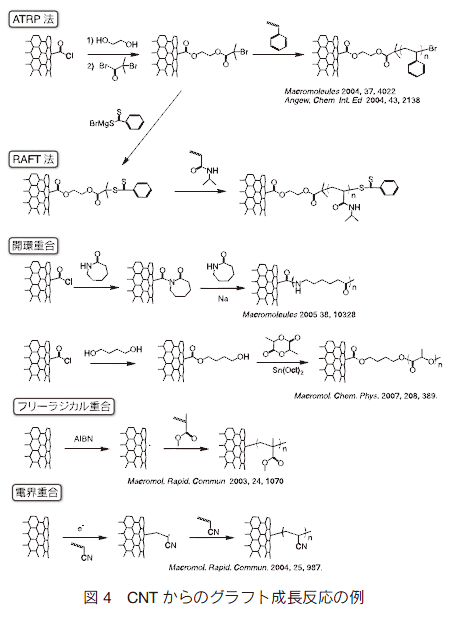
開環重合では脂肪族ポリエステルや脂肪族ポリアミド、対象とするモノマーに適応可能な開始点をデザインして導入する。フリーラジカル重合では AIBN によりラジカルが導入され、そこを反応開始点として重合が進行する。一方で、系中の成長末端ラジカルと付加反応も起こすことから grafting ‘to’も系中では同時に進行する。
CNT 存在下でフリーラジカル重合を行った場合、CNT 表面と共有結合を形成する可能性が非常に高い。また、CNT の高い電気伝導性を生かして、電界重合の反応場として利用することが可能である。 ATRP 法や、RAFT 法の場合は開始点の導入効率により重合の数が決定されてしまう制限があるが、電界重合の場合、理論上は表面全体が反応点となりうることから均一な被覆化などに有利であると予想できる。アクリロニトリルの他、ポリアニリンの表面電界重合などが報告されている。その他の例については総説 4-6) にまとめられているのでそちらを参考にしていただきたい。
非共有結合による複合化で、我々の最近の研究を一例紹介する。ポリベンゾオキサゾールはモノマーユニット内にオキサゾール環を有する重縮合系高分子であり、ポリイミドやポリベンゾイミダゾール(PBI)と同様スーパーエンジニアリングプラスチックの一種である。中でもポリ(p- フェニレンベンゾビスオキサゾール)(PBO)(図 5)はその剛直な構造から、市販されている高分子繊維の中で「最高」の強度・弾性率・耐熱性・難燃性を有し(表 1)、消防服や防弾チョッキなどに利用されている 7)。
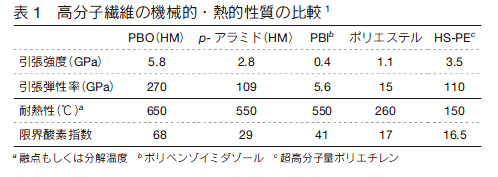
PBO は優れた強度および耐熱性を有することから、カーボンナノチューブ(CNT)高分子複合体の高分子マトリックスとして有望である。しかしながら、PBO と CNT は強酸にしか溶解しないため、その複合化や成形加工には、多くの難点がある。
いくつか例を挙げる。Kumar ら 8) は、単層 CNT (SWNT)存在下ポリリン酸(PPA)中での in situ (その場)重合法および液晶紡糸法により PBO/SWNT ファイバーを得ている。 SWNT を 10 wt% 添加することにより、引張強度が 50%、引張弾性率が 20% 増加した複合体が得られている。 Zhou ら 9) は、PBO の前駆体であるポリヒドロキシアミドオリゴマー(oHA)を多層 CNT (MWNT)と反応させることで PPA への溶解性が向上した MWNT-oHA を作製し、MWNT-oHA 存在下 PPA 中での in situ 重合法および液晶紡糸法により MWNT/PBO ファイバーを得ている。MWNT を 0.54 wt% 添加することにより、引張強度が 28%、引張弾性率が 50% 増加した複合体が得られる。
これらの PBO/CNT 複合体の弾性率の増加率は理論モデルから予想される値よりも低い値であり、CNT の低い分散性がその原因として考えられる。 CNT と高分子間の弱い界面相互作用による CNT の低い分散性は CNT による効率的な補強効果を妨げる 10) 。
強酸による CNT の短尺化および補強効果の低下 11) が報告されており、産業面のみならず強酸を用いない複合体作製法が望まれる。
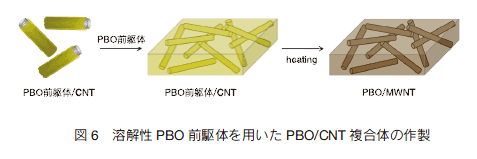
我々は強酸を用いずに PBO/CNT 複合体を得る新たな手法を開発した(図 2) 12)。有機溶媒に可溶な PBO 前駆体と CNT を有機溶媒中で複合化させ、加熱処理を行うことで PBO/CNT 複合体を得る。紫外可視近赤外吸収分光およびフォトルミネッセンス分光により、CNT の分散状態を評価でき、PBO 前駆体は有機溶媒中で CNT を孤立分散する(図 6 左)。 PBO 前駆体主鎖の芳香環と CNT 表面との π-π 相互作用によるものと考えられる。 PBO/CNT 複合体フィルムは PBO 前駆体/CNT 複合体フィルムを減圧下 300 度、350 度、400 度各 1 時間ずつ加熱処理することで得られる。
Raman 分光により、CNT の欠陥の度合いを評価したところ、複合化処理および加熱処理後も CNT には欠陥がそれほど導入されないことがわかった。 CNT を 1.7 wt% 添加することにより、引張強度が 130%、引張弾性率が 179% 増加した複合体が得られた。この補強効果はこれまで報告されている PBO/CNT 複合体の補強効果よりも大きなものであった。複合体フィルム断面の走査型電子顕微鏡観察により、PBO 中で CNT が効率よく分散している様子が見られ、欠陥の少ない CNT が効率よく分散しているために、効率的な補強効果が得られたと考えられる。 CNT 添加後も PBO の優れた耐熱性は保持されており、このような高強度・高耐熱性高分子フィルムは金属代替材料として有望である。
1-2.CNT とナノ粒子との複合化
CNT はその大きな比表面積と高い電気伝導性、ファイバー状構造とそれらが作るメッシュ構造ゆえに反応に伴う電子の授受を行う場、すなわち電極材料として最適な構造を有している。従って、反応サイトとして何らかの触媒作用のあるナノ粒子と組み合わせた CNT/ナノ粒子複合体は、CNT の有効な利用法の 1 つだと言える。触媒作用のある物質としては金属ナノ粒子や半導体ナノ粒子等がある 13)。これらナノ粒子と CNT との間での高効率な電子の授受はデバイス効率向上へのポイントとなるため、両者を空間的に近接させる必要がある。従って CNT とナノ粒子の単純な混合ではなく、ナノ粒子を CNT に直接担持する様々な手法が提案されている。
ベンゼン環からなる CNT はナノ粒子の足場となるサイトがなく、効率のよい直接担持が困難である。そこで酸処理などで CNT 表面にカルボキシル基などの極性基を導入し、そこを足場としてナノ粒子を担持する方法が一般的である(ただし、ここでは CNT は本来の特性を幾分なくしている可能性があることに注意)。一方で、CNT 表面にダメージを与えない担持法として、CNT 表面に吸着した分子(リンカー分子)を足場として担持する方法を用いる。リンカーとなる分子としては低分子系の界面活性剤 14) や芳香族系化合物、あるいは DNA やポリアニリン等の高分子系が報告されている。芳香族系化合物の中でも、特にピレン誘導体は CNT との強い相互作用を利用した粒子担持へのリンカー分子としての報告が多い。
これら 2 種類の足場形成方法それぞれに対し、主に 2 種類のナノ粒子担持法が報告されている。一方はあらかじめ調製したナノ粒子を担持する方法(ex situ 法)と、もう一方は CNT 存在下で粒子を直接 CNT 上に成長させる方法(in situ法)である。 CdSe 等の半導体ナノ粒子や TiO2、ZnO 等の金属酸化物ナノ粒子は ex situ 法で、Au、Pt、Pd 等の金属ナノ粒子は in situ 法で担持されることが多い。
2. バイオアプリケーション(CNT とバイオ分子との複合化)
これまで、高分子ミセル、金属ナノ粒子や量子ドットなどのナノ物質がバイオテクノロジーの分野に応用され、薬剤送達システムや生体プローブとして研究されてきた。最近では CNT のバイオテクノロジー素材として利用が期待されている。特に単層 CNT(SWNT)は、生体を構成する水や血液が吸収を持たない近赤外領域に強い吸収を持つ稀有な特徴ゆえ非常に魅力的である。この特長は分かりやすく言えば、もし近赤外の光で見ると体内の SWNT を体外から透かして見られるということを意味し、体内でも見たり使ったりしやすいということに他ならない。
これまでに多くの培養細胞を使った実験(in vitro)を経て、最近ではマウスを使った体内(in vivo)での実験が行われ始めている。これらの流れを本節で紹介する。
2-1.in vitro アプリケーション
可溶化剤自身に機能性がある場合、CNT の機能と組み合わせることにより高機能な複合体を作ることができる。例えば、ポリエチレングリコール(PEG)鎖が導入された分子で可溶化した CNT は、PEG 鎖の高い生体適合性と CNT との組み合わせにより、体内への薬剤送達材料やプローブ分子として利用できる。代表的な機能性可溶化剤としては DNA を挙げることができる。 DNA と CNT は、同程度の直径をもつ。第 2 回で紹介した様に、私たちは、DNA が単層カーボンナノチューブ(SWNT)を孤立溶解することを発見した 15)。 DNA/SWNT 複合体は安定であり、核酸デリバリーや DNA (RNA)センシングなど、長い研究の歴史を持つ DNA(RNA)に CNT の特徴(形状、サイズ、分光特性、電気特性)を付与できる材料として展開を見せている。具体的な例を挙げる。 DNA の B 構造から Z 構造へのコンフォメーション転位を SWNT の近赤外領域の蛍光シフトとして捉えた研究、DNA ハイブリダイゼーションを同様な蛍光シフトとしてのナノモル(nM)レベル検出に成功した研究、SWNT/DNA 複合体上の DNA ハイブリダイゼーションを電気化学的検出手法を用いることでアットモル(aM)レベルの超高感度で検出した論文など多くの論文が報告されている。私たちは、DNA/SWNT 複合体のアプリケーションの 1 つとして、DNA/SWNT 複合体と PEG グラフト化ポリ-L-リジン(PLL-g- PEG )を複合化させることで、SWNT に分散安定性と生体親和性を付与した新規の三元複合体(PLL-g- PEG/DNA/SWNT 複合体)を作製し、これが HeLa 細胞へ高効率で取り込まれることを明らかにした 16)。
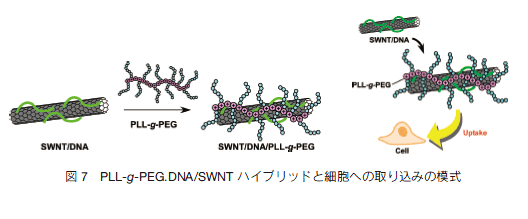
Weisman らは、非イオン系界面活性剤である Pluronic F108 で分散された SWNT が細胞内に取り込まれ、その空間分布を SWNT の近赤外発光をプローブとしてマッピングできることを報告した 17)。この報告は、SWNT が「色素プローブ」として有用であることを意味している。Dai らは SWNT をバイオアプリケーションに展開した先駆者の一人である 18)。まず、がん細胞を使った実験で DNA/SWNT 複合体をエンドサイトーシスにより細胞質内に取り込ませることに成功し、さらに複合体を取り込んだ細胞への近赤外光レーザー(808 nm)照射により DNA が SWNT 上から放出され、核内まで到達することを発見した。さらに SWNT 吸着部位としてアルキル鎖を持ち、生体組織への非特異吸着を防ぐ PEG を連結したリン脂質誘導体(PEG 化リン脂質)を SWNT 可溶化剤とした複合体についての報告も行っている。さらに近赤外光照射による SWNT 発熱でがん細胞を死滅させることにも成功している 18)。この研究は、SWNT によるがん治療への戦略について有益な示唆を与えてくれる重要な研究であった。
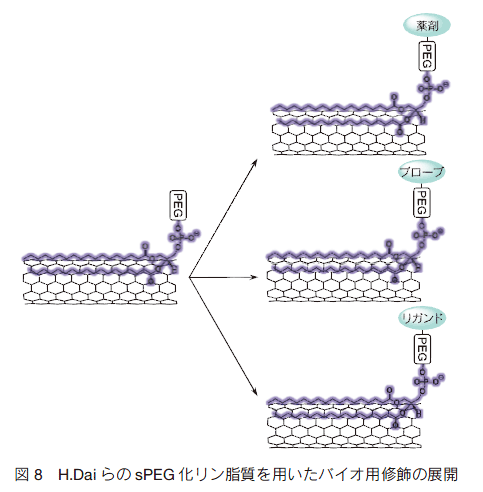
リン脂質誘導体可溶化剤で分散された SWNT では近赤外発光細胞イメージング 19) の他、SWNT の強いラマンシグナルを利用したラマン細胞マッピング 20) も報告されている。 SWNT は 13C を導入することによりラマンピークがシフトすることから、マルチカラーのラマンプローブとして染め分けることも可能である。 SWNT は、遺伝子の導入や光刺激によるがん治療およびプローブ分子としてマルチな機能性を有していると言えよう。
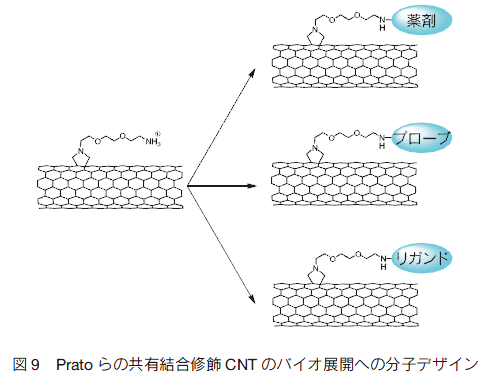
一方で、共有結合による化学修飾 SWNT の in vitro 実験も 2004 年ごろから立ち上がった。 Prato らは、いわゆる Prato 反応と言われるフラーレンへの反応で確立していた付加反応を SWNT 表面の官能基化へ適応し、化学修飾 SWNT をバイオアプリケーションへ展開した 21)。彼らは図 9 で示した官能基化 SWNT を出発物質とし蛍光分子を導入した SWNT の細胞内への導入を顕微鏡観察により確認した。またプラスミド DNA をイオンコンプレックス形成により官能基化 SWNT と複合化し、これを効率よく細胞内に導入することにも成功している。このような化学修飾法では蛍光基や薬剤骨格などを有機合成化学に基づいて自在に修飾できるのが特徴である。ただし化学修飾法では SWNT はドープされることになり、SWNT ならではの強い近赤外領域での吸収や発光等の特長は失われ、SWNT 自身のイメージングや光熱変換を用いた温熱治療の効率は低下するといった短所もある。
2-2.in vivo アプリケーション
培養細胞実験において得られた興味深い知見を踏まえて 2008 年頃から動物体内(in vivo)への CNT の導入実験が報告され始めた。 in vivo 研究において可溶化 SWNT は、i) イメージングのプローブ ii) 腫瘍の温熱治療のための発熱体 iii) 腫瘍部への分子送達キャリアという主に 3 つの用途に展開されている。
イメージングとしては、マウス体内からの SWNT の近赤外発光によるイメージング 22)、ラマン散乱によるイメージングの他 23)、SWNT をパルス光で励起した時に発生する音波をイメージングする光音響イメージングが報告されている 24)。また光熱変換作用を利用した腫瘍の温熱療法はマウス体内においても有効であることが多くの実験から確かめられている。以上 2 つの用途は、光照射で SWNT を励起することが必要であるが、体内への近赤外光の深度(~数 cm)を考えた時、人体内部にも適用可能であるとは言い難い。従って薬剤を腫瘍部に送達する薬物送達システム(ドラッグデリバリーシステム : DDS)としての使い方が最も実際的であろう。
CNT は疎水的な表面を持ち、疎水的分子を効率よく吸着することが知られており、DDS における課題の一つである疎水的薬剤の送達には非常に有利なキャリアである。例えば代表的な疎水性抗がん剤であるドキソルビシン(DOX)の場合 SWNT 1 g につき 4 g もの DOX 担持が可能である。実際に DOX を担持した可溶化 SWNT をマウスに投与したところ、 DOX のみを投与した場合と比べ、優位な延命が見られた 25)。長さが 150 nm 程度の可溶化 SWNT は PEG 化で血中滞留性を高めた場合、受動的ターゲティングによる腫瘍集積性が見られるが、さらに積極的な腫瘍集積を目指して腫瘍ターゲティング機能を付与するアプローチも実証されている。 Bhirde らは化学修飾により SWNT に抗がん剤であるシスプラチンとレセプター認識部位を結合し、マウスの尾静脈投与したところ、認識部位を連結した場合のみ腫瘍の成長抑制効果を確認した。in vivo においてもターゲティング機能が有効に作用することが明らかとなった 26)。今後はより実用化を意識した研究として SWNT の体外への排出機構の確認などが必要になってくるであろう。
2-3.細胞培養基板としての CNT
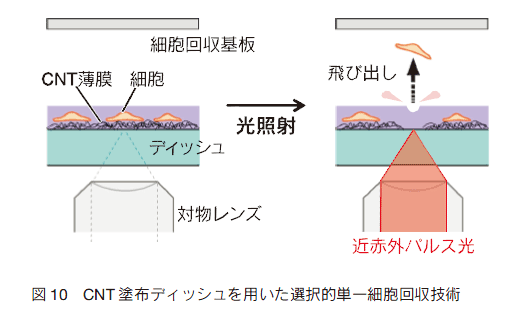
一方、体外で用いる用途にも期待がかかる。最も報告が多いのは、 CNT 薄膜上での細胞培養の研究であろう。 CNT 薄膜は疎水的でファイバーメッシュ状の環境を細胞に与えるため、汎用のガラスディッシュやプラスチックディッシュとは異なる細胞増殖挙動を与えることがある。 CNT 薄膜をコートしたディッシュ( CNT ディッシュ)上で培養した場合、良好な細胞接着および伸展が見られる例が多くの細胞で知られている。このことは、 CNT に接着タンパクが吸着しやすく、細胞に接着環境を与えやすいことを示している。もともと比較的接着の良い HeLa 細胞などではこの効果は明瞭ではないが、接着が比較的難しい細胞には有効であろう。また神経系細胞では特に興味深い挙動が知られており、例えば ES 細胞からの神経系細胞へ分化確率向上や 27)、神経系細胞の活性増加が報告されている 28)。これまで報告されているような高分子ナノファイバー細胞培養基板とは異なる CNT ならではの特性であり興味深い。筆者らは、CNT ディッシュ上で播種した細胞に近赤外パルスレーザー光照射を行い CNT に衝撃波を発生させ、その結果、照射したターゲット細胞が培地外に飛出し、捕獲できることを明らかにした(図 10)。光照射は顕微鏡観察下で行えるために、狙った細胞 1 個を選別して回収できる。さらに回収した 1 個の細胞からの遺伝子情報の読み出しにも成功している 29)。このように細胞培養基板としての CNT の用途はバイオ・メディカル分野において大きな広がりを見せている。
| Copyright(c) 1996-2013 DOJINDO LABORATORIES, ALL Rights Reserved. |