 |
| トップページ > DT Diaphorase 特異的なグルコース定量蛍光色素の開発 |
 |
DT Diaphorase 特異的なグルコース定量蛍光色素の開発株式会社同仁化学研究所 後藤 奈月 蛍光色素は、生物化学の基礎研究、新薬開発、臨床診断といった分野で有力なツールとして注目されてきた。これまで用途に応じた種々の蛍光色素が数多く開発されているが、今回は DT- ジアホラーゼ(以下 DTD)特異的な蛍光色素に着目し、その特徴を紹介する。 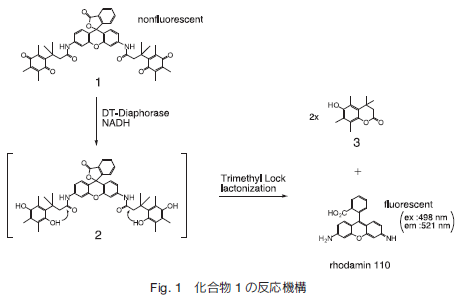 化合物 1 は、ローダミン 110 の 3’と 6’部位にキノンを結合させることにより、ローダミン 110 の蛍光を抑えているため無蛍光である。DTD 、 NADH 存在下では、DTD を触媒として NADH より電子を受け取り、キノン部位に選択的に還元反応が起こる。その際に生成する化合物 2 のフェノール部位は非常に反応性が高いため、速やかに分子内でラクトン化反応を起こし化合物 3 とローダミン 110 を産生する 2)。解離したローダミン 110 は本来高い量子収率を有しており、解離と同時に蛍光が検出される仕組みである。 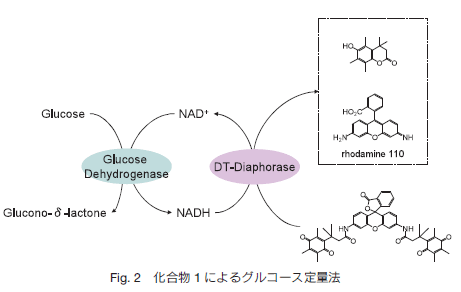
グルコースデヒドロゲナーゼの働きにより、まずグルコースがグルコノラクトンに酸化され、それと同時に系内に存在する NAD+ が還元されて NADH を生じる。 NADH は電子供与体として働き、DTD を触媒として化合物1を還元することによって蛍光物質であるローダミン 110 を産生する。グルコース 1 分子の酸化により生じた電子が結果として 1 分子のローダミン 110 を産出するため、ローダミン 110 の蛍光強度からサンプル中のグルコースを定量することが可能となる。本化合物を用いたグルコース定量法はμM 濃度の測定も可能であり、感度はレサズリンとグルコースオキシダーゼを用いた系 3)に匹敵する。 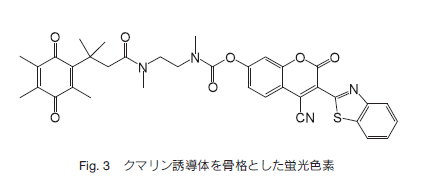 今回紹介したこれらの化合物は、Trimethyl Lock lactonization という反応機構によって DTD 依存的に反応し、蛍光を発するという新規の蛍光色素であり、この色素を用いることによって一般的なグルコース検出法の問題点を克服することが可能である。また、グルコースデヒドロゲナーゼではなく他の酵素を利用することによって、さまざまな検出系への応用が期待できる。 参考文献
2) S. S. Chandran, K. A. Dickson and R. T. Raines, “Latent fluorophore based on the trimethyl lock”, J. Am. Chem. Soc., 2005, 127, 1652. 3) H. Maeda, S. Matsu-ura, Y. Yamauchi and H. Ohmori, “Resazurin as an electron acceptor in glucose oxidase-catalyzed oxidation of glucose”, Chem. Pharm. Bull., 2001, 49(5), 622. 4) S. T. Huang, Y. X. Peng and K. L. Wang, “Synthesis of a new long wavelength latent fluorimetric indicator for analytes determination in the DT-Diaphorase coupling dehydrogenase assay system”, Biosens Bioelectron, 2008, 23(12), 1973.
|
| Copyright(c) 1996-2012 DOJINDO LABORATORIES, ALL Rights Reserved. |