 |
| トップページ > 「蛍光生物学」の最前線2 |
 |
|||||||||||||
「蛍光生物学」の最前線2
1.はじめに生物は様々な、そして多数の生体分子から構成されている。なかでもタンパク質分子は生命現象の主要な担い手である。1990年代に、1個の生体分子を蛍光を用いて可視化する技術(1分子蛍光イメージング法)が開発され、1分子の酵素反応 1, 2)、モータータンパク質の運動 3)、タンパク質間相互作用 4) などがイメージングされて来た。最近では、4種類の異なる蛍光色素で標識したヌクレオチドを用いて1分子のDNAの複製過程をイメージングする1分子DNAシークエンサーが開発され 5)、ゲノム解析の効率が飛躍的に高まるとともにDNAのメチル化などの解析に革新的な成果がもたらされている 6)。また、蛍光標識した分子の位置をナノメートルの精度で計測することが可能であることが示され 7)、蛍光を一つずつ確率的に光らせる技術と組み合わせることにより、光の回折限界を超えた超解像蛍光顕微鏡法が開発された 8)。本稿では、1分子蛍光イメージング法の原理と最新の応用例を解説する。
2.1分子計測の意義従来の生物科学研究では、生体分子の性質を、試験管内の多数分子の平均値として表してきた。例えば、濃度 1μM、体積 1mL の溶液中には、約1015個の分子が含まれている。この場合、個々の分子の平均値からのずれを表す標準偏差と平均値との比は10-7以下になり、測定装置に由来する誤差に比べて無視できるほど小さい。このように、多分子計測では平均値を非常に正確に求めることができるが、分子のダイナミクスを研究することは困難である。生物分子モーターの化学・力学エネルギー変換のように、1分子が担っている2種類の反応のタイミングを明らかにするには、1分子ごとに計測しない限り不可能である 9)。多分子計測のもう一つの欠点は、平均値から1分子の機能を推論するためには、「全ての分子は同様に振る舞う」という仮定を必要とする。しかし、1分子計測によって、生物分子モーターの力発生 9) や、コレステロール酸化酵素などの酵素反応 2)や、受容体のシグナル伝達 10) に履歴作用があることが分かり、この仮定が必ずしも成立しないことが明らかになっている。1分子計測は技術的に難しいが、仮定のない明快な結論を導き出すことができるという長所がある。 3.1分子蛍光イメージングによるタンパク質の機能解析と1分子DNAシークエンサー タンパク質の大きさは光の波長よりもずっと小さいので、これを検出するには特別の工夫が必要である。生体分子に蛍光色素を結合させ、蛍光によって分子の存在が分かるようにしたのが蛍光顕微鏡法である。1980年代になって、DNAやアクチン(筋タンパク質の一種)などの繊維状の巨大分子を、1分子レベルで蛍光顕微鏡観察できるようになったが、これらの観察は、生体分子に数百個の蛍光色素を結合させて、ようやく見えるものだった。1分子の蛍光色素は超高感度カメラならば検出可能な数の光を放出しているが、強い励起光をあてると様々な光学部品より蛍光が発生し背景光となるため、この背景光をいかにして少なくするかが1分子観測の最大の問題点であった。1990年代になって、顕微鏡部品の改良などによって、背景光の問題を解決することにより、1分子の蛍光観察が可能になった。さらに、「エバネッセント場」を利用した局所励起を行うことにより、1分子の生体分子が酵素反応している様子 1, 2) や運動している様子 3) をイメージングすることが可能となった。エバネッセント場を発生させる最も簡単な方法は、全反射を利用する方法である(TIRFM ; total internal reflection fluorescence microscopy) 1) 。高屈折率の媒質(ガラス)から低屈折率の媒質(水溶液)に臨界角以上で光を入射すると全反射が起こり、低屈折率の媒質の界面近傍にエバネッセント場が生成される。エバネッセント場は、界面から深さ方向に指数関数的に減衰する局所場である。このため、波長よりも短い領域を照明することができる。エバネッセント場も伝播光と同様に、物体による散乱を受けたり蛍光色素を励起することが可能である。散乱光や蛍光のみを伝播光として検出できるので、背景光が極めて小さく、1分子の蛍光色素の観察に適している。エバネッセント場は界面のごく近傍しか照明しないので、背景光を抑えられるだけでなく、蛍光標識した生体分子を局所励起できるという利点がある。 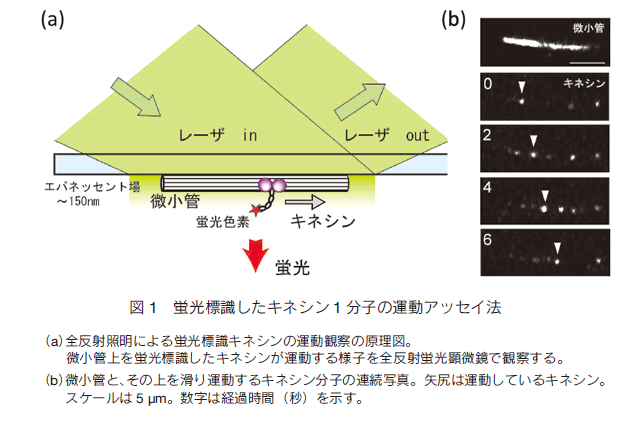
蛍光色素が放出した光子をカメラなどで検出する場合、光の回折により波長の1/2程度に広がってしまう。しかし、単一蛍光分子からの蛍光(10,000光子)の輝度分布を冷却 CCD カメラで撮影して解析すれば、中心位置を0.5秒の時間分解能、1.5 nm の精度で検出することが可能である 7) 。キネシンやミオシンⅤなどの生物分子モーターのモーター部位に結合した蛍光をナノメートル計測することにより、分子モーターが2つのモーター部位を交互に前進させていることが明らかになった。 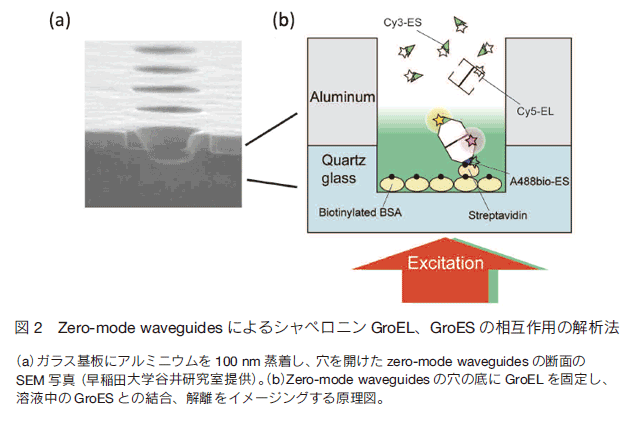 zero-mode waveguides は1分子DNAシークエンスにも応用されている。DNA合成酵素がγリン酸を異なる蛍光色素で標識した4種類のヌクレオチドを取り込みながらDNAを合成するのを利用して、1分子のDNAの塩基配列をリアルタイムに解読することに米国の Pacific Biosciences 社が成功している 5)。同社は、この原理に基づく1分子DNAシークエンサーを開発しており、15分でゲノムのシークエンスを完了する性能に達成することを目指している。 4.超高解像光学顕微鏡への応用光は波動としての性質を持つため、回折により点像は波長の1/2程度に広がってしまう。このような限界があるため、点像の広がりよりも近接する2点を分離してイメージングすることは不可能と思われてきた。しかし、最近、STED (Stimulated Emission Depletion)法、構造化照明法やローカリゼーション法などによる超解像光学顕微鏡法が考案された 8) 。ここでは、ローカリゼーション法による超解像光学顕微鏡法について説明する。光の回折限界よりも接近した2つの蛍光分子が同時に蛍光を発する場合、これらを2つの分子としてイメージングすることはできない。しかし、2つの分子が別々に光る場合は、前章で述べたように分子輝度分布の中心位置をナノメートルの精度で求めることができるので、2つの分子を分離して認識することが出来る。ローカリゼーション法では、蛍光分子の明滅(ON-OFF)を上手く制御して別々に光らせることにより、分子の位置を光の回折限界を超えた精度で決定する。蛍光のON-OFFを制御する方法として、紫外線の照射によって蛍光を発するようになったり、蛍光波長が変化する緑色蛍光タンパク質の変異体を利用する方法がある(PALM; photo-activated localization microscopy) 13) 。また、Cy5 や Alexa647のようなシアニン系の蛍光色素を用いて、検出用の強いレーザー(例えば 647 nm)を照射して全体の蛍光色素をOFF状態にし、微弱な 405 nm のレーザーを照射したり、近傍に短波長の蛍光色素を存在させてこれを励起することにより、わずかな頻度でON状態に戻すことが行われている(STORM; stochastic optical reconstruction microscopy) 14) 。これらの色素は自発的にOFFからON状態に遷移するので、1種類の色素だけでも検出用の強いレーザーを当て続けてON-OFFを観測することが可能である(dSTORM; direct STORM)。ON-OFF が 10,000回以上なるように画像を取得してそれぞれの蛍光分子の輝度分布の中心位置に直径約 20 nm の点をプロットして、スーパーインポーズすることにより全体像を再構成する。このように、点描画のようにして超解像の画像が出来上がる。この場合、焦点面上では約 20 nm、奥行き方向には約 60 nm と、従来の光学顕微鏡の10倍の解像度を得ることができる。ただし、奥行き方向の位置を決めるためにはカメラの前に円筒レンズを置き、1分子の点像の楕円率を計測する必要がある。図3は、化学固定した HeLa 細胞の微小管に Alexa647 標識した抗 α-tubulin 抗体を結合させ、TIRFM と dSTORM で観察した例である。 dSTORM により鮮明で解像度の高い画像が得られている。超高解像光学顕微鏡により、従来の顕微鏡では捉えることの出来なかった微細構造が明らかになったり、複数種の分子の共局在をより厳密に調べることが可能になった。 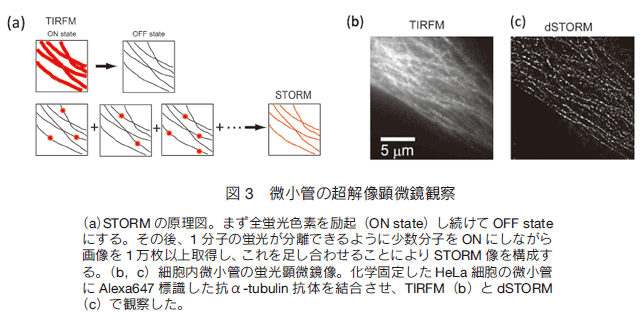
5.おわりに1分子イメージング技術の開発により、さまざまな研究室で、日常のように分子を扱えるようになってきた。本稿では、生物分子モーターを中心に解説したが、ここで紹介した1分子イメージング技術は、あらゆる種類の生体分子の1分子機能アッセイ、例えば、DNAとポリメラーゼやヘリカーゼなどとの相互作用、蛋白質間相互作用、蛋白質とリガンドの相互作用などの解析に応用されつつある。1分子の機能を解析することにより、多分子系では見過ごされていた生体分子機械の動作原理の本質に迫れるであろう。また、次に重要なのは、個々の生体分子が生体というシステムの中でどのように振る舞っているかを解明することである。生体システムの中で物質、エネルギー、情報の流れを分子レベルで追跡することが可能になったので、近い将来、生体システムの構築原理も明らかにされるであろう。
謝辞zero-mode waveguides の製作は、谷井孝志、島本直伸、三宅丈雄、園部弘典、赤堀玲、大泊巌氏(早稲田大学)らよるものである。また、dSTORM による観察は坂本明彦、菅原皓氏(東京大学)によって行われた。記して感謝します。
|
|||||||||||||
| Copyright(c) 1996-2011 DOJINDO LABORATORIES, ALL Rights Reserved. |
