Three-Dimensional Expansion Microscopy Kit (4x 3D-ExM)

膨張顕微鏡法標本作製キット(4x 3D-ExM)
- 細胞を3次元的に約4倍拡大できる
- ゲル作成から膨張までの試薬がオールインワン
- 細胞の微細構造を光学顕微鏡でイメージングできる
-
製品コードT517 Three-Dimensional Expansion Microscopy Kit (4x 3D-ExM)
| 容 量 | メーカー希望 小売価格 |
富士フイルム 和光純薬 |
|---|---|---|
| 10 tests | ¥48,000 | 349-10371 |
【ご注意】
・より詳細な観察をする場合は、水浸レンズの使用を推奨します。よくある質問:観察時の顕微鏡/レンズについて注意点を教えてください をご参照ください。
・細胞の染色試薬類(核染色剤等)はキットに含まれておりません。
| 10 tests | ・Monomer Solution ・Polymerization Initiator ・Polymerization Promoter ・Activation Buffer ・Enzyme Solution ・Crosslinking Solution ・Mold ・Cover Glass |
3 ml×1 30 mg×1 250 µl×1 3 ml×1 100 µl×1 100 µl×1 ×10 ×10 |
|---|
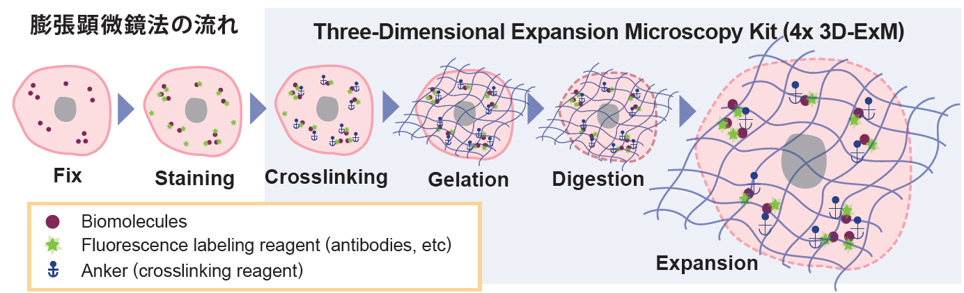
膨張顕微鏡法(Expansion Microscopy:ExM)とは
細胞内には複数のオルガネラが存在し、それぞれのオルガネラの構造を解析することが細胞機能の理解や疾病のメカニズム解明において重要となります。細胞内のオルガネラの構造を高解像度にイメージングするためには、高価な電子顕微鏡や超解像顕微鏡が必要です。一方で蛍光顕微鏡では、アッベの回折限界によりオルガネラの構造を詳細に解析することは困難です。そこで蛍光顕微鏡でオルガネラを観察するための手法の一つとして2015年にExpansion Microscopy法が開発されました。Expansion Microscopy法は吸水性ゲルを利用してサンプル自体を大きくする技術であり、蛍光顕微鏡では困難であった微小な構造のイメージングが可能となります。
本キットは、Expansion Microscopy法を行うためのゲル作成に必要な試薬および枠を同梱したキットであり、細胞を3次元的に約4倍まで膨張することが可能です。
参考文献 : F. Chen, PW. Tillberg, Science., 2015, 347(6221): 543–548.
R. Norman, et.al. Journal of Cell Biology., 2025, 224 (2): e202407116.
This product is covered by U.S. Patent Application No. 17/466,434.
This technology is based on research conducted by Dr. Aussie Suzuki at the University of Wisconsin–Madison.
マニュアル
取扱説明書 操作7 :Cover Glassをゲル作成枠(Mold円内)に移す
取扱説明書 操作16. Moldを取り外し、ゲルを10 cm dishに入れる
取扱説明書 操作.19 ゲルを傷つけないように注意しながら超純水を除去する
技術情報
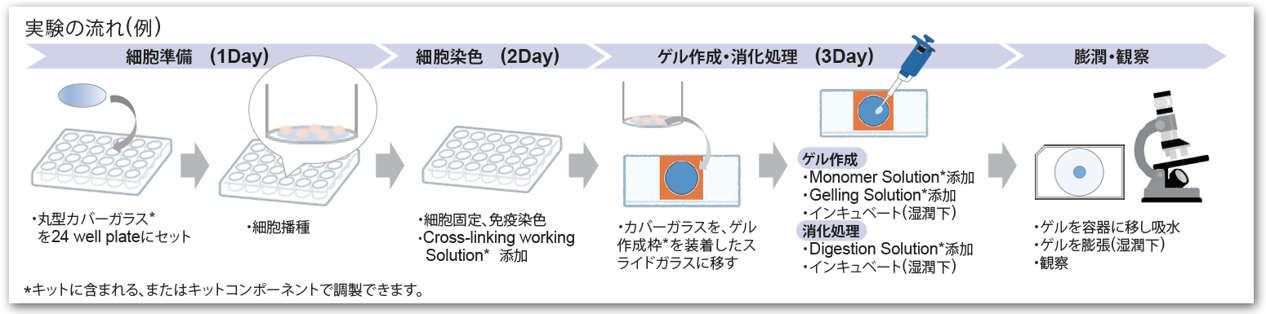
はじめてでもすぐに実験をはじめられる
キットには、実験に必要な試薬が含まれております。細胞の準備からゲルの作成、観察までを詳細に記載したプロトコルを準備しており、はじめてでも安心して実験できます。
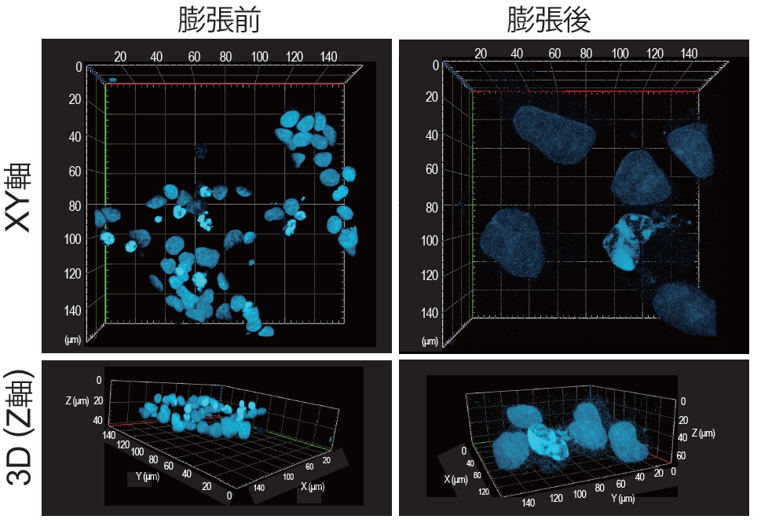
細胞を3次元的に約4倍に拡大
HeLa細胞の核をDAPIで染色し、本キットを用いて膨張顕微鏡法による観察を行いました。
ゲルの大きさと染色した核を膨張の指標として膨張倍率を確認した結果、XYZ軸それぞれに約4倍膨張することを確認しました。
<ゲルの大きさ>

<核染色>
<検出条件>
検出装置: 共焦点レーザー顕微鏡 Lens 40× Water objective
DAPI(青): Ex/Em = 405/420-480 nm
膨張前: Laser 1.0%, Gain 550 V
膨張後: Laser 2.5%, Gain 680 V
膨張前後の細胞の解像度・サイズ変化の評価
RPE1細胞の核をDAPIで染色後、本キットを用いて細胞を膨張させ、20倍水浸レンズを使用した共焦点顕微鏡で観察しました。
同一細胞において、膨張前(Pre-3D-ExM)と膨張後(Post-3D-ExM)を比較した結果、膨張後の細胞は解像度が向上し、さらに長軸・短軸の長さおよび面積が約4倍に増大していることを確認しました。

※青枠(1)上段、赤枠(2)下段は、膨張前後の同一細胞における2つの細胞領域の解像度の変化の例を示しています。
<実験条件>
細胞:RPE1 (hTERT-immortalized retinal pigment epithelial cells)
染色: DAPI 30 min
<観察条件>
顕微鏡システム:スピニングディスクコンフォーカル(Yokogawa CSU + Nikon Ti2 stand+ CMOSカメラ)
Imaging conditions: A 20× water-immersion objective was used for both pre- and post-ExM imaging (the same cell was imaged with identical optical settings).
405 laser: 60% power with 200 msec exposure for ExM
データ提供:Dr. Aussie Suzuki at the University of Wisconsin–Madison
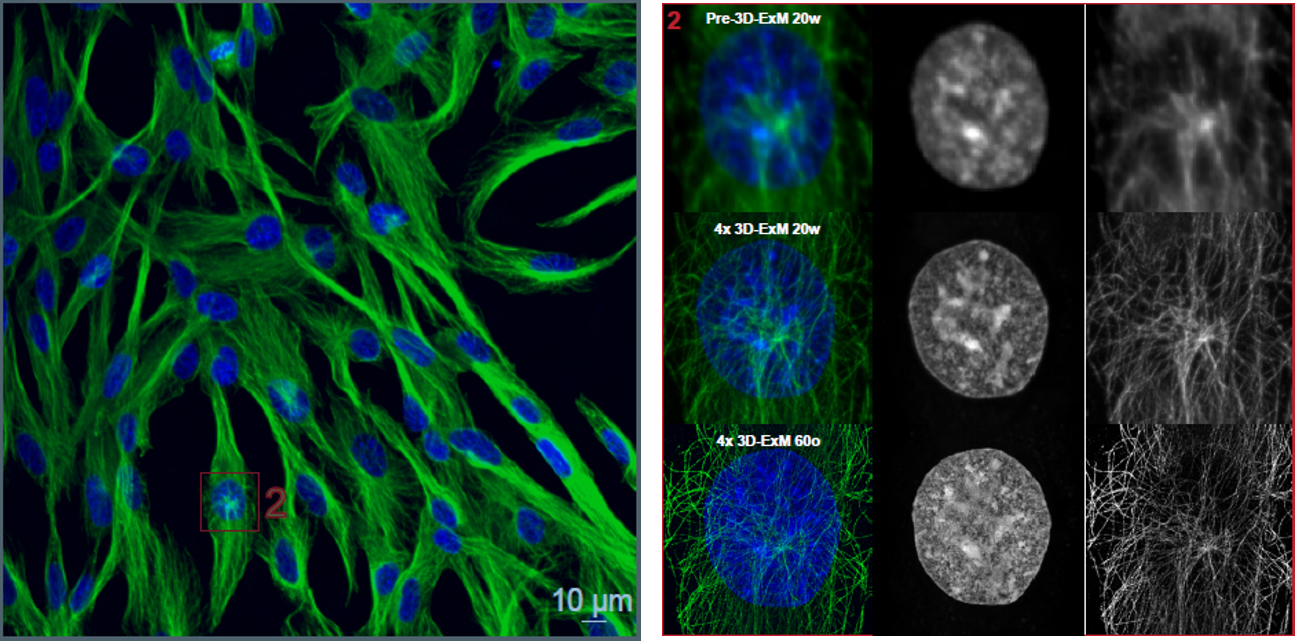
膨張後の核およびチューブリンの観察
RPE1細胞の核およびチューブリンを染色した後、本キットを用いて細胞を膨張させました。その後、20倍水浸レンズを用いて共焦点顕微鏡にて観察し、さらに同一の細胞を60倍油浸レンズでも観察しました。その結果、核および細胞骨格の詳細な形態を確認できました。
<実験条件>
細胞: RPE1 (hTERT-immortalized retinal pigment epithelial cells)
染色:
一次抗体 anti-alpha-Tubulin (DM1A), 1 hour
ニ次抗体 Alexa488 conjugated anti-mouse-IgG, 1 hour
DAPI, 30 min
<観察条件>
顕微鏡システム:スピニングディスクコンフォーカル(Yokogawa CSU + Nikon Ti2 stand+ CMOSカメラ)
Imaging conditions: A 20× water-immersion objective was used for both pre- and post-ExM imaging (the same cell was imaged with identical optical settings). The same cell was also imaged using a 60× oil-immersion objective to obtain higher-resolution images.
405 laser: 60% power with 200 msec exposure for ExM
488 laser: 60% power with 200 msec exposure for ExM
データ提供:Dr. Aussie Suzuki at the University of Wisconsin–Madison
膨張後の核およびチューブリンの3D解析
RPE1 細胞の核およびチューブリンを染色した後、本キットを用いて細胞を膨張させました。膨張後の細胞は、 60倍油浸レンズを使用した共焦点顕微鏡により3D イメージングを行いました。
その結果、核構造および細胞骨格の詳細な形態を高解像度で 3 次元的に観察することができました(Movie 1)。さらに、同一細胞内に存在する 2 種類の異なる形状の核について、それぞれの構造的特徴の違いを 3 次元的に比較・確認することができました(Movie 2)。
|
データ提供:Dr. Aussie Suzuki at the University of Wisconsin–Madison
<実験条件> <観察条件> 405 laser: 60% power with 200 msec exposure for ExM |
実験例:薬剤処理毎のミトコンドリア形態変化の観察
脱分極剤であるCCCP、複合体III阻害剤であるアンチマイシンおよび、ATP合成酵素阻害剤であるオリゴマイシンで処理したHeLa細胞のミトコンドリアの外膜(TOM20)、および内膜(COX IV)を染色し、本キットを用いて膨張顕微鏡法により観察しました。
その結果、膨張前の細胞では、ミトコンドリアの分裂は確認できるものの外膜と内膜の判別が困難でした。一方で、膨張後の細胞では、ミトコンドリア膜電位を脱分極させるCCCPおよびアンチマイシン処理では、外膜がリング状(ミトコンドリア分裂)を示し、内部に内膜タンパク質COX IVが存在しない構造(黄色矢印)が観察されました。さらに膜電位を脱分極させないオリゴマイシン処理では、分裂したミトコンドリア内部にCOX IVが観察されました。本キットを用いることで、ミトコンドリア分裂時の内膜の変化まで観察することができました。
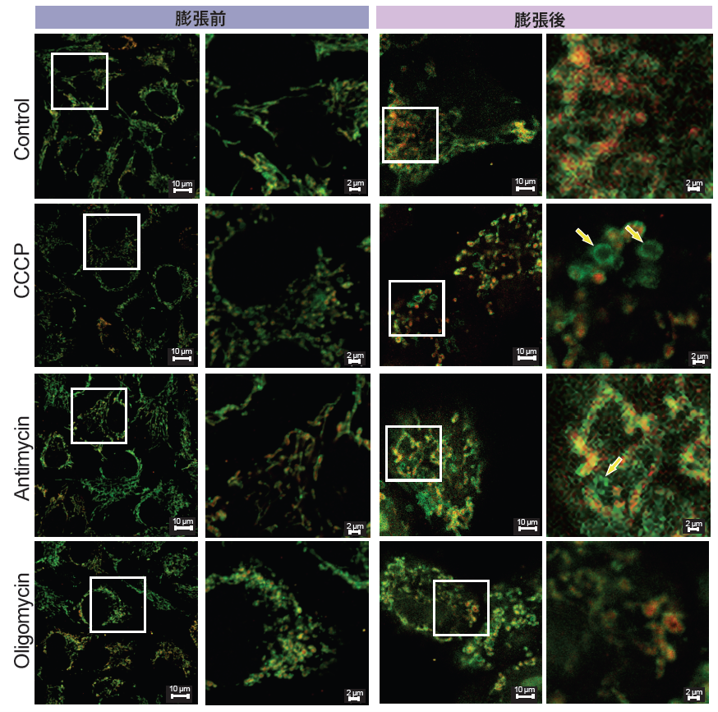
<実験条件>
CCCP : 10 μmol/l 30 min処理
Antimycin: 10 μmol/l 30 min処理
Oligomycin: 10 μmol/l 30 min処理
<検出条件>
検出装置:共焦点レーザー顕微鏡 (Zeiss LSM800)
TOM20 (緑): Ex/Em = 488/500-550 nm
COX IV (赤): Ex/Em = 561/580-620 nm
膨張前
Lens: 63× Oil objective
TOM20: Laser 1.0 %, Gain 650 V
COX IV: Laser 2.0 %, Gain 650 V
膨張後
Lens: 63× Oil objective
TOM20: Laser 70 %, Gain 700 V
COX IV: Laser 70 %, Gain 750 V
よくある質問
-
Q
観察時の顕微鏡/レンズについて注意点を教えてください。
-
A
膨張後の試料は厚みが増すため、深部の観察がしやすい水浸レンズの使用を推奨します。
油浸レンズを使用する場合は、以下の点にご注意ください。
油浸レンズは作動距離(レンズと試料の間の距離)が短いため、ピントが合わない場合(レンズが観察容器に接触する)があります。その際は観察の途中でゲルをスライスして観察してください。詳細は撮像マニュアルをご参照ください。
-
Q
落射型顕微鏡で観察できますか?
-
A
落射型顕微鏡では観察できません。
膨張後の試料は厚みが増すため、落射蛍光顕微鏡では焦点外光が増えバックグラウンドが上昇し細部の観察が困難です。そのため、共焦点顕微鏡での観察を推奨します。よくある質問: 観察時の顕微鏡/レンズについて注意点を教えてください も併せてご参照ください。
-
Q
細胞を染色する際の染色試薬の注意点はありますか?
-
A
・免疫染色で一般的に使用される、赤色〜近赤外領域のシアニン骨格を持つ以下のような色素は、ゲル化反応時に分解を受けるため使用できません。
Alexa Fluor® 647、Alexa Fluor® 660・以下の色素において実績があります。
Alexa fluor® 488 、Alexa fluor® 568 、DAPI
-
Q
膨張後の試料はどのくらい安定ですか?観察まで数日保存しておくことは可能ですか?
-
A
水分を保持した状態であれば、室温で 7 日間保存しても観察できた実績があります。
その際、菌の発生を防ぐため 必ず滅菌水 を使用してください。なお、冷蔵・冷凍保存するとゲルが収縮して観察できなくなるため、ご注意ください。
-
Q
膨張前の細胞を観察したいです。観察のタイミングと観察方法を教えてください。
-
A
細胞を染色した後【取扱説明書 操作3の後(Cross-linking solution添加前)】に観察してください。 Cross-linking solution添加後の観察は、 Cross-linking solution試薬の自家蛍光の影響を受けるため推奨しません。
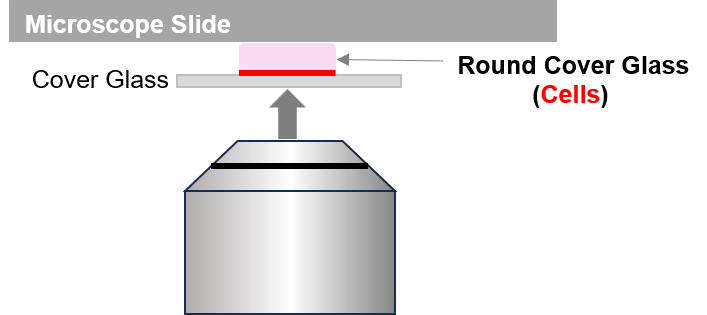
観察時は、細胞を播種した丸形カバーガラスをスライドガラスにのせ、その上から別のカバーガラスをかけたうえで、動かないよう周囲をパラフィン等で固定すると観察しやすくなります。
共焦点顕微鏡では、サンプル(細胞側)が下向きになるようにセットして観察してください。
Preparation of the Slide for Observation and Imaging
-
Q
膨張後に染色できますか?
-
A
膨張後の観察にて蛍光が暗い場合は、追加染色することが可能です。
取扱説明書 [操作24.蛍光観察を行う]項目の補足事項をご参照ください。
-
Q
本キットは組織に使用できますか?
-
A
組織には使用できません。
-
Q
【トラブル:観察】観察対象が見つかりません。
-
A
まずは核を染色した色素の波長で核を探し、その後に目的物に合う波長に切り替えて探してください。 その際は、共焦点顕微鏡のピンホールを広げてZ方向を広範囲で検出してください。
それでも見つからない場合は、レーザー強度またはゲインを上げて観察してください。
詳細は撮像マニュアルをご参照ください。
-
Q
【トラブル:観察】蛍光が弱く観察できません。
-
A
XYZ軸に4倍に膨張しているため、膨張前と比べ蛍光強度が大きく低下します。
1. 通常よりも顕微鏡のレーザーのLaser Power、Gainを上げて観察してください。
【例:油浸レンズ(顕微鏡: Zeiss LSM800)での実績 膨張前:Laser/1-2%,Gain/550-650V 膨張後: Lase20-80%,Gain/700-800 V 】2. 1.でも蛍光が弱い場合は、追加での染色を行ってください。(取扱説明書 [操作24.蛍光観察を行う]項目の補足事項参照)
・核染色の蛍光強度が低い場合:10 µg/ml DAPI水溶液にて室温で30分間染色する。
・免疫染色の蛍光強度が低い場合:追加で二次抗体での染色を行う。
-
Q
【トラブル:観察】ゲルが動いて撮像が出来ません。
-
A
観察容器とゲルとの間に水が残っているとゲルが滑って動きます。そのため、必要に応じてキムワイプなどで水分をふき取ってください。水分量が多い場合はアスピレーターやマイクロピペットを用いて、ゲルの吸い込みや破損に注意*しながら、水分を除いてください。
(*動画: https://www.youtube.com/embed/FCydMTsZAQM)
また、観察容器とゲルの間にキムワイプ等を挟み、動きにくくした状態で観察する方法も有効です。

取扱条件
| 保存条件: 冷蔵 | |
|
危険・有害 シンボルマーク |
    
|
|---|---|











