MATP+
アセチルコリンエステラーゼ用基質
-
製品コードM450 MATP+
-
CAS番号1242026-53-4
-
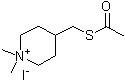
化学名1,1-Dimethyl-4-acetylthiomethylpiperidinium iodide
-
分子式・分子量C10H20INOS=329.24
| 容 量 | メーカー希望 小売価格 |
富士フイルム 和光純薬 |
|---|---|---|
| 10 mg | ¥- | 販売を終了いたしました |
(本製品は特許出願がなされており、小社は試薬用途として、その実施許諾を得て製造・販売しております)
性質
アセチルコリンエステラーゼ(AChE)は、神経伝達物質であるアセチルコリンを分解して神経伝達系をコントロールする重要な酵素の一つであり、脳や血中等に存在することが知られている。この酵素は有機リン系およびカルバメート系の農薬や殺虫剤などによって活性が低下することから、これらの薬物の暴露指標として用いられている。また、アルツハイマー病では神経障害によってアセチルコリン量が減少するため、AChE阻害剤がアルツハイマー病治療薬として注目されている1)。
現在、AChE活性測定には、基質であるアセチルチオコリンと検出試薬であるDTNBを用いたEllman法が一般的に用いられている2), 3)。しかしながら、アセチルチオコリンは、AChE選択性が低く、生体内に存在する非特異的コリンエステラーゼ(ブチリルコリンエステラーゼ;BChE)に対しても反応する。そのため、AChE活性を測定するためにはBChE阻害剤を添加する必要があり、操作が煩雑であった4-6)。
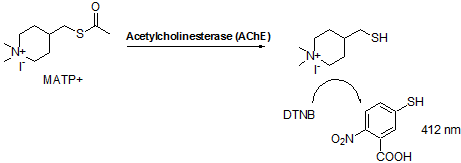
MATP+は、独立行政法人 放射線医学総合研究所(NIRS)によって開発された新規のAChE基質で、アセチルチオコリンに比べて非常に高いAChE選択性を有している(Fig. 1, 2, 3)7)。そのため、BChE阻害剤を添加することなくAChE活性を選択的かつ簡便に測定することができる。また、Ellman法と同様に検出試薬としてDTNBを用いることができるため、同じ装置を用いた測定が可能である。本試薬は全血中のAChE活性測定やKarnovsky/Roots法を用いた神経組織のAChE染色に有用であり、白田らは、本試薬を用いた全血中AChE活性測定の自動分析装置への応用例を報告している。8)
Fig. 1 MATP+を用いたアセチルコリンエステラーゼ活性測定法の原理
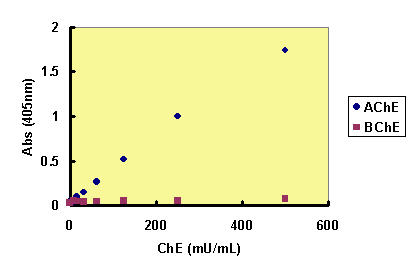
Fig. 2 MATP+のAChE選択性(DTNB発色)
AChEおよびBChEのい濃度依存的な発色を示す。
BChEとはほとんど反応せず、AChEのみ濃度依存的な発色を示すことから
AChE活性を選択的に測定することができる。
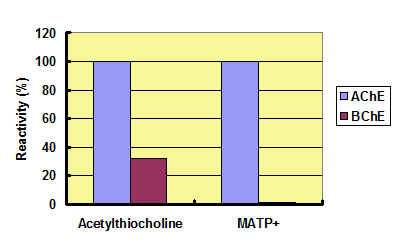
Fig. 3 AChE選択性の比較
注)AChEに対する反応性を100%とした場合の値を示す。
汎用されているアセチルチオコリンは、内在するBChEとも反応し、AChEに対する選択性は低い。
一方、MATP+はBChEとはほとんど反応せずAChEに対する選択性が非常に高いことがわかる。
*AChE(アセチルコリンエステラーゼ)
神経組織、赤血球などに存在する。
コリン作動性神経(副交感神経、運動神経、交感神経の中枢~神経節)の神経伝達物質アセチルコリン(AChE)を酢酸とコリンに分解する。
*BChE(ブチリルチオコリンエステラーゼ)
肝臓、血清などに存在する。AChを含む様々なコリンエステル系を分解する。
健康診断などで検査されるChEは、こちらの方である。
高値の場合は、ネフローゼ症候群、脂肪肝など、低値の場合は、肝硬変、肝炎、
有機リン系薬物中毒(有機リン系の農薬中毒、サリンなどの神経ガス中毒)などが疑われる。
技術情報
注意事項
・本製品を粉末の状態で取り出し使用する場合、性状の性質上、静電気等の要因で容器内に付着し、取り出しにくい場合があります。
・容器内に付着し、取り出せなかった粉末に関しては、使用する溶媒を容器に入れ、溶かし出して使用してください。
操作例
- 操作例 -
使用試薬
・MATP+ (Code: M450); Assay bufferに溶解して使用する。
・DTNB (Code: D029); 100 mmol/l DTNB(DMSO)溶液を調製後、Assay bufferに希釈して使用する。
・Assay buffer (100 mmol/l phosphate、pH7.4)
・Acetylcholinesterase (AChE);必要に応じてAssay bufferに溶解および希釈して使用する。
(1) 組織および細胞中のAChE活性測定
【前処理】
組織
1. 組織 10~100 mgをAssay buffer 0.5~1 ml中でホモジナイズする。
2. 8,000 x gで10分間4℃にて遠心する。
3. 上清を測定試料とする。
*測定試料中のAChE活性はサンプルによって異なるため、必要に応じてAssay buffer で希釈して使用する。
細胞
1. 200 x gで10分間4℃にて遠心し、上清を捨てる。
2. 細胞をPBS 0.5 mlで洗浄し、 再度200 x gで10分間4℃で遠心する。
3. Assay buffer 0.5~1 ml中でホモジナイズする。
4. 8,000 x gで10分間4℃にて遠心する。
5. 上清を測定試料とする。
*測定試料中のAChE活性はサンプルによって異なるため、必要に応じてAssay buffer で希釈して使用する。
プレートアッセイ(組織および細胞)
1. 試料溶液(sample)もしくはAChE標準液(0.025, 0.0125…, 0 units/ml)100 μlを各ウェルに添加する。
注)0 units/mlはblank 1となる。
2. 2 mmol/l DTNB溶液50 μlおよび2 mmol/l MATP+溶液50 μlを各ウェルに添加し、ピペッティングする(sample, AChE standard, blank 1)。 ブランクとして試料(sample)100 μlに対し、2 mmol/l DTNB溶液50 μlおよびAssay buffer 50 μlを添加したウェルを準備する (blank 2)。
3. 37℃で30分間インキュベートする。
4. 405 nmもしくは415 nmのフィルターを用いて、マイクロプレートリーダーで吸光度を測定する。
5. 試料中のAChE活性をAChE標準液の検量線から求める。
注1)検量線はAChE standardの吸光度からblank 1の吸光度を差し引いて求める。
注2)試料中のAChE活性由来の吸光度はsampleからblank 2の吸光度を差し引いて求める。
分光光度計を用いた測定(組織および細胞)
1. Assay buffer 2.5 ml, 10 mmol/l MATP+溶液 0.2 ml, 10 mmol/l DTNB溶液0.2 mlを3 mlキュベットに添加する。
2. 37℃で10分間インキュベートした後、AChE標準液(0.2 units/ml)あるいは測定試料0.1 mlを添加し、37℃で5~10分間412 nm吸光度変化をそれぞれ測定する。
3. AChE標準液の吸光度変化(傾き)から試料中のAChE活性を求める。
(2) 血液中のAChE活性測定
ヘパリン(抗凝固剤)を加えた血液を試料とする。
プレートアッセイ(全血)
1. ヘパリン処理した全血およびAChE標準液 (5, 2.5, …, 0 units/ml) 5 μlを1.5 mlエッペンチューブにとる。
注)0 units/mlはblank 1となる。
2. 2 mmol/l MATP+溶液 250 μlを添加して37℃で30分間インキュベートする。
3. 8,000 x gで1分間遠心した後、上清50 μl各ウェルに添加する。
4. Assay buffer 100 μlおよび2 mmol/l DTNB溶液 50 μlを各ウェルに添加し、ピペッティングする。
5. 405 nmもしくは415 nmのフィルターを用いて、マイクロプレートリーダーで吸光度を測定する。
6. 血中のAChE活性をAChE標準液の検量線から求める。
注)検量線はAChE標準液の吸光度からblank 1の吸光度を差し引いて作成する。
*血中のAChE活性(units/ml) = (O.D.sample - O.D.blank 1)/検量線の傾き
分光光度計を用いた測定(全血)
1. ヘパリン処理した全血10 μlをAssay buffer 90 μlに添加する(10倍希釈液)。
2. Assay buffer 2.5 ml, 10 mmol/l MATP+溶液0.2 ml, 10 mmol/l DTNB溶液0.2 mlを3 ml キュベットに添加する。
3. 37℃で10分間インキュベートした後、AChE標準液 (0.2 units/ml) あるいは測定試料(10倍希釈液)0.1 mlを添加し、37℃ で5~10分間436 nm吸光度変化を測定する。
4. 傾き(Δ436 nm/min)を算出し、血中のAChE活性を求める。
(3) AChE阻害活性の測定
1. サンプル溶液(AChE阻害活性物質を含む)を、Assay bufferで順次倍々希釈することによってサンプル希釈溶液を調製する。
2. 1.で調製したサンプル希釈溶液50 μlを96穴マイクロプレートの各ウェルに添加する。
3. 0.01 units/ml AChE溶液 50 μlを各ウェルに添加し、ピペッティングする。
4. 2 mmol/l DTNB溶液50 μlおよび2 mmol/l MATP+溶液50 μlを各ウェルに添加し、ピペッティングする。
5. 37℃で30分間インキュベートする。
6. 405 nmもしくは415 nmのフィルターを用いて、マイクロプレートリーダーで吸光度を測定する。
参考文献
1) 杉本八郎,日薬理誌, 2004, 124, 163.
2) V. Battissi, M. R. C. Schetinger, L. D. K. Maders, K. F. Santos, M. D. agatini, M. C. Correa, R. M. Spanevello, M. do C. Araujo and V. M. Morsch, Clin. Chim. Acta, 2009, 402, 114.
3) M. S. Garcia-Ayllon, M. X. Silveyra, A. Candela, A. Compan, J. Claria, R. Jover, M. Perez-Mateo, V. Felipo, S. Martinez, J. Galceran and J. Saez-Valero, Hepatology, 2006, 43(3), 444.
4) S. Brimijoin and P. Hammond, J. Neurochemistry, 1988, 51(4), 1227.
5) F. Worek, U. Mast, D. Kiderlen, C. Diepold and P. Eyer, Clin. Chim. Acta, 1999, 288, 73.
6) R. S. Naik, B. P. Doctor and A. Saxena, Chem. Biol. Interact., 2008, 175, 298.
7) T. Kikuchi, T. Okamura, K. Fukushi and T. Irie, Biol. Pharm. Bull., 2010, 33(4), 702.
8)白田亨,医学検査,2013, 62(5) , 528.
取扱条件
| 性状: | 本品は、白色~淡黄白色粉末で水に溶ける。 |
|---|---|
| 純度(HPLC): | 98.0% 以上 |
| 水溶状: | 試験適合 |
| IRスペクトル: | 試験適合 |
| NMRスペクトル: | 試験適合 |
| 保存条件: 冷蔵 , 取扱条件: 吸湿注意 |