-Cellstain®- DAPI
死細胞染色色素
-
製品コードD212 -Cellstain®- DAPI
-
CAS番号28718-90-3
-
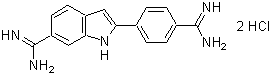
化学名4',6-Diamidino-2-phenylindole, dihydrochloride
-
分子式・分子量C16H17Cl2N5=350.25
| 容 量 | メーカー希望 小売価格 |
富士フイルム 和光純薬 |
|---|---|---|
| 1 mg | ¥6,500 | 342-07431 |
【注意】-Cellstain®- DAPIは、通常、チューブ底面にフィルム状に付着した状態となっております。
稀に、輸送中の振動等により本品がチューブ底面から外れ、チューブ壁面やキャップ裏に付着している場合がございます。内容物を下に落としてから開封をしてご使用ください。
ご不明な点がございましたら、小社カスタマーリレーション部までお問合せください。(Free Dial:0120-489-548)
性質
DAPIは1977年、抗トリパノソ-マ薬の探索のためにDannらによって合成された蛍光性の色素で、蛍光顕微鏡下、酵母のミトコンドリア、葉緑素、ウイルス、マイコプラズマ、染色体中のDNA検出に使用されている1)。460 nmに青色の蛍光を持ち(励起波長360 nm)、DNAのAT配列に特異的なminor groove binderである。DAPIの光耐性は高く、HBO 200水銀ランプ、3 mm厚のBG 12フィルタ-の下でHoechst 33258の約2倍と高い。
本製品はDNAと作用するため変異原性を示す疑いがあることから、使いきりタイプとして製品化した。秤量する時の実験室内への粉末の飛散を防ぎ使いやすくなっている。
なお、-Cellstain®- DAPI solutionは動物細胞の死細胞染色蛍光色素として使用されるが、DAPI自体は細菌の全菌染色色素としても利用することができる5)。全菌染色用としては-Bacstain- DAPI solution(Code:BS04)を別途ご用意しており、こちらをご活用いただきたい。
注意事項
DAPIストック溶液を作成する場合には、水を使用する(PBSには溶解しにくい)。
ただし、水に溶解したものは長期保存には適していない。
長期保存をお考えの際は、溶液の安定性を高めた溶液タイプの製品-Cellstain®- DAPI solution(Code:D523)をご使用いただきたい。
蛍光特性:λex=360 nm, λem=460 nm
参考文献
参考文献
1) W. Schnedl, A. V. Mikelsaar, M. Breitenbach and O. Dann, "DIPI and DAPI: Fluorescence Banding with Only Negligible Fading", Hum. Genet., 1977, 36, 167.
2) I. W. Taylor and B. K. Milthorpe, "An Evaluation of DNA Fluochromes, Staining Techniques, and Analysis for Flow Cytometry. I. Unperturebed Cellpopulations", J. Histochem. Cytochem., 1980, 28(11), 1224.
3) F. Otto and K. G. Tsou, "A Comparative Study of DAPI, DIPI, and Hoechst 33258 and 33342 as Chromosomal DNA Stains", Stain Technol., 1985, 60, 7.
4) N. Poulin, A. Harrison and B. Palcic, "Quantitative Precision of an Automated Image Cytometric System for the Measurement of DNA Content and Distribution in Cells Labeled with Fluorescent Nucleic Acid Stains", Cytometry, 1994, 16, 227.
5)M. Kawai, N. Yamaguchi and M. Nasu,"Rapid Enumeration of Physiologically Active Bacteria in Purified Water Used in the Pharmaceutical Manufacturing Process", J. Appl. Microbiol., 1999, 86 (3), 496.
よくある質問
-
Q
核染色剤に使用される色素の特徴、違いは何でしょうか?
-
A
ここで紹介している色素は核酸との相互作用により蛍光を発するか、蛍光強度が強くなる特徴があります。
蛍光波長以外の違いとしては下記の点がございます。【EB】
塩基特異性は無く、全DNA,RNAに結合します。
生細胞の膜透過性がなく、死細胞を染色します。【PI】
EBと同様に塩基特異性はありません。インターカレーションした時の蛍光強度がEBより高いため、より広く使用される色素です。
生細胞の膜透過性がなく、死細胞を染色します。【DAPI】
2重鎖の副溝(minor groove)と結合します。アデニン-チミジンクラスターに高い結合性を持っています。
生細胞の膜透過性がなく、死細胞を染色します。【AO】
2重鎖にインターカレーションしたときと、単鎖のリン酸に結合した時では蛍光波長が異なることを利用して、2重鎖と単鎖を区別して検出できます。
生細胞の細胞膜を透過します。【Hoechst33342、33258】
DNAのアデニン-チミジン部に特異的に結合します。
生細胞の細胞膜を透過し、生細胞のDNAを染色できる色素です。
-
Q
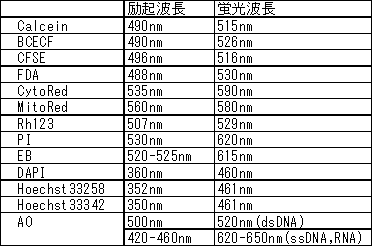
細胞染色色素の励起と蛍光の波長を教えて下さい。
-
A
*AOはフローサイトメトリーなどでは488 nm励起で観察されることもあります
-
Q
DAPIを核染色に用いたいのですが、どのように使用すればよいのでしょうか?
-
A
下記のような使用報告例がございます。 DAPIストック溶液を作成する場合には、水を使用して下さい(PBSには溶解しにくい)。
ただし、水に溶解したものは長期保存には適していません。
長期保存をお考えの際は、溶液の安定性を高めた溶液タイプの製品-Cellstain®- DAPI solution(コード:D523)をご使用下さい。 ご使用の際、ストック溶液を緩衝液もしくは有機溶媒にて目的の濃度に希釈して下さい。【DAPI を用いた細胞染色の例】
固形腫瘍あるいはcluster を含むsample のDAPI 染色の例(参考文献3)
1) 0.02 %トリプシン - EDTA 処理し、37 ℃で30 分間 incubate 後、1,500 rpm で5分間遠心分離を行ない、上清をすてる。
2) -20 ℃の50 % methanol (ethanol でも可)にて固定後、1,500 rpm で5分間遠心分離を行ない、上清をすてる。
3) -20 ℃の30 % methanol にて洗浄後、1,500 rpm で5分間遠心分離を行ない、上清をすてる。
4) 0.2 M リン酸緩衝液(pH 7.2)にて洗浄後、1,500 rpm で5分間遠心分離を行ない、上清をすてる。
5) RNase の0.2 M リン酸緩衝液(pH 7.2)溶液 (1 mg/ml ) を細胞106 個あたり0.2 mL を加え、37 ℃にて30 分間 incubate する。
6) 0.2 M リン酸緩衝液(pH 7.2)にて洗浄後、1,500 rpm で5分間遠心分離を行ない、上清をすてる。
7) 1 μg/ml のDAPI 溶液10 ml 加え、4 ℃にて2時間遮光の上染色する。【DAPI を用いた細胞染色の例】 Vollenweider らはリンフォカイン活性化キラ-(LAK)細胞の細胞増殖アッセイにおいて、
DAPI 染色を行ない、蛍光プレ-トリ-ダ-を用いて測定している(参考文献 2)。
その時の濃度はストック溶液で0.1 mg/mL の水溶液、使用濃度は1 μg/ml のメタノ-ル溶液を用い、
1 well 当たり 100 μl 使用して蛍光染色している。【参考文献】
1) W. Schnedl, A.-V. Mikelsaar, M. Breitenbach, O. Dann, Hum. Genet., 36, 167 - 172 (1977).
2) I. Vollenweider, P. Groscurth, J. Immunol. Methods, 149, 133 (1992)).
3) M. A. Hotz, J. Gong, F. Traganos, Z. Darzynkiwicz, Cytometry, 15, 234 - 244 (1994).
4) N. Poulin, A. Harrison, B. Palcic, Cytometry, 16, 227 - 235 (1994).