-Cellstain®- Calcein-AM
生細胞染色用色素
-
製品コードC326 -Cellstain®- Calcein-AM
-
CAS番号148504-34-1
-
化学名3',6'-Di(O-acetyl)-4',5'-bis[N,N-bis(carboxymethyl)aminomethyl]fluorescein, tetraacetoxymethyl ester
-
分子式・分子量C46H46N2O23=994.86
| 容 量 | メーカー希望 小売価格 |
富士フイルム 和光純薬 |
|---|---|---|
| 1 mg | ¥18,100 | 349-07201 |
性質
Calcein-AM はCalcein の4つのカルボキシル基をアセトキシメチルエステル化(AM 化)することにより細胞膜透過性としたものである。Calcein-AM自体は蛍光をほとんど示さないが、細胞内のエステラ-ゼによる加水分解でCalceinとなる。このCalceinは、膜不透過性の化合物で、強い黄緑色の蛍光を示す(λex=490 nm、λem=515 nm)。Calcein-AMと同じ生細胞染色用色素として同様にfluorescein骨格を持つCarboxy fluorescein diacetate (CFDA) やFluorescein diacetate (FDA) などが知られている。しかし、これらの化合物は発色後細胞膜から漏出しやすく、それが使用上の問題のひとつとなっていた。これらのような色素に比べ、Calcein-AMは発色後の細胞からの漏出が少ない色素として利用が高まってきている。また、リンパ球の増殖や白血球のケモタキシスなどの細胞機能を阻害しないことが知られている。また、Calcein-AM はキラ-T細胞やNK細胞などによる細胞障害活性の測定において、汎用されてきた放射性同位体を用いる51Cr release 法と同様の結果を与えてることから、細胞毒性も少ないことが示唆される。
Calcein-AM は生細胞を染色し、蛍光顕微鏡下の観察やフロ-サイトメトリ-などに利用されているが、死細胞染色色素と共に用いることで生死細胞二重蛍光染色に利用される場合も数多い。Papadopoulusらは、Calcein-AMとEthidium homodimer (EthD-1)を使用して二重染色を行い、2つの色素の蛍光波長の違いを利用しフローサイトメトリーで細胞毒性について検討を行っている。
Calcein-AM は細胞毒性が少なく、また蛍光を発した後の細胞からの漏出が少ないことから、生細胞染色用色素として現在最も有用な色素である。先に示したように、放射性同位元素を使用した計測法も現在行われているが、安全性、簡便性の点からも蛍光性化合物を利用した細胞研究の解析が進んでくるものと期待される。
蛍光特性:λex=490 nm, λem=515 nm
【注意】
本品は、通常、試薬はチューブ底面に無色フィルム状で付着した状態となっております。(下図参照)
稀に、輸送中の振動等により本品がチューブ底面から外れ、チューブ壁面やキャップ裏に付着している場合がございます。
内容物を底面に落としてから開封してご使用ください。
ご不明な点がございましたら、小社カスタマーリレーション部までお問合せください。(Free Dial:0120-489-548)
チューブのみ  |
試薬が入った状態のチューブ  |
| チューブ底面からの写真 | |
参考文献
1) K. McGinnes, G. Chapman, R. Marks and R. Penny, "A Fluorescence NK Assay Using Flow Cytometry", J. Immunol. Methods, 1986, 86, 7.
2) S. J. Morris, "Real-time Multi-wavelength Fluorescence Imaging of Living Cells", BioTechniques, 1990, 8(3), 296.
3) S. A. Weston and C. R. Parish, "New Fluorescent Dyes for Lymphocyte Migration Studies Analysis by Flow Cytometry and Fluorescent Microscopy", J. Immunol. Methods, 1990, 133, 87.
4) D. M. Callewaert, G. Radcliff, R. Waite, J. Lefevre and D. Poulik, "Characterization of Effector-Target Conjugates for Cloned Human Natural Killer and Human Lymphokine Activated Killer Cells by Flow Cytometry", Cytometry, 1991, 12, 666.
5) Han-Qing Xie, R. Huang and V. W. Hu, "Intercellular Communication Through Gap Junctions Is Reduced in Senescent Cell", Biophys. J. , 1992, 62, 45.
6) S. A. Weston and C. R. Parish, "Calcein: a Novel Marker for Lymphocytes Which Enter Lymph Nodes", Cytometry, 1992, 13, 739.
7) X. M. Wang, P. I. Terasaki, G. W. Rankin Jr. , D. Chia, H. P. Zhong and S. Hardy, "A New Microcellular Cytotoxicity Test Based on Calcein AM Release", Hum. Immunol., 1993, 37, 264.
8) N. G. Papadopoulos, G. V. Dedoussis, G. Spanakos, A. D. Gritzapis, C. N. Baxevanis and M. Papamichail, "An Improved Fluorescence Assay for the Determination of Lymphocyte-Mediated Cytotoxicity Using Flow Cytometry", J. Immunol. Methods, 1994, 177, 101.
9) L. S. De Clerck, C. H. Bridts, A. M. Mertens, M. M. Moens and W. J. Stevens, "Use of Fluorescent Dyes in the Determination of Adherence of Human Leucocytes to Endothelial Cells and the Effects of Fluorochromes on Cellular Function", J. Immunol. Methods, 1994, 172, 115.
10) H. Ohata, Y. Ujiki and K. Momose, "Confocal Imaging Analysis of ATP-Induced Ca2+ Response in Individual Endothelial Cells of the Artery in Situ", Am. J. Physiol. , 1997, 272(6), 1980.
よくある質問
-
Q
51Cr-release法との相関はありますか?
-
A
Calcein-AMと51Cr-release法に相関性はあります。
下記文献にその報告があります。
N.G.Papadopoulos, et.al., J.Immunol.Methods, 177,101-111(1994)
-
Q
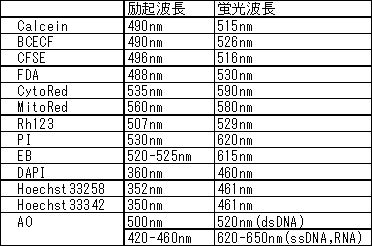
細胞染色色素の励起と蛍光の波長を教えて下さい。
-
A
*AOはフローサイトメトリーなどでは488nm励起で観察されることもあります
-
Q
細胞染色試薬Cellstainの生細胞染色色素の中で細胞内に長く留まるのはどれですか?
-
A
細胞内の保持という意味ではやはり「CFSE」が一番細胞の中に長くとどまることが出来ます。
蛍光強度は落ちますが、8週間細胞の中に蛍光色素があったのが確認されております。
「Calcein-AM」「BCECF-AM」で3日間蛍光が観察されております。
「Calcein-AM」は6時間で90%細胞内に保持されているとの報告もございます。
・S.A.Weston, et.al., J.Immunol.Methods, 133, 87-97(1990)
・H.P.Zhong, et.al., Hum.Immunol., 37, 264-270(1993)
ただ、細胞障害活性ということでは「Calcein-AM」「BCECF-AM」の方が影響を及ぼさない
といわれております。
・L.S.D.Clerck, et.al., J.Immunol.Methods, 172, 115-124(1994)
あと注意点としては、元々の基本骨格がFluoresceinなので、励起光による退光が
起りやすいので長時間の励起による蛍光観察は難しいかもしれません。
(退光防止剤などを使用すれば幾分よいかもしれませんが)
-
Q
Calcein-AMの使用方法を教えてください。
-
A
下記に一例としてHeLa細胞の場合を紹介します。
細胞の種類、観察条件に応じて試薬濃度の検討や固定を行って下さい。【試薬】
A液:Calcein-AM 1mg をDMSO 1mlに溶解する→1 mmol/L溶液
*溶液の保存は劣化を抑えるため、遮光下-20 ℃で行ってください。
B液:A液をPBS(-)で500倍に希釈する(A液10μlをPBS 5 mLで希釈すると2 μmol/Lとなる)
*Calcein-AMは水溶液中で分解するので、B液は用時調製を行ってください。【操作】
1)HeLa細胞をトリプシン-EDTAなどで回収し、細胞の懸濁液を準備する。
2)細胞懸濁液を遠心分離する(1,000 rpm,3 min)
3)上清を除き、PBS(-)を添加する(このとき細胞数が105~106 cells/mLになるように調製する)
4)ピペッティングなどで十分分散させる。
*培養液中の血清などはバックグランドを上昇させる恐れがあるので、2)~4)の操作を
繰り返し行い、十分に洗浄する。
5)1.5mlマイクロチューブに4)で得た細胞懸濁液30μlを添加する。
6)これに[B液]を15 μL添加する。
7)マイクロチューブに蓋をして、37 ℃で15分間インキュベートする。
8)カバーガラス上に7)の液10 μLをのせ、上からカバーガラスを重ね、染色した細胞懸濁液を挟み込む
9)このカバーガラスを蛍光顕微鏡に置き、490 nmのフィルターで励起させ、黄緑色の蛍光を発する生細胞を観察する。
(フィルターについては490±10 nmのものであれば良好に観察することができる)*血清やフェノールレッドはバックグラウンドとなるので除いておくこと。
*バックグランドが高い場合には、洗浄を行ってください。
*スライドガラス上に培養した細胞も同様に染色・観察が可能です。
*PIとの二重染色方法は、プロトコル「生細胞・死細胞を染め分けたい」をご覧下さい。
-
Q
Calcein-AM(粉末)を購入し、溶液にしたいのですがどうすればよいですか?
-
A
DMSOに溶解してください。
分子量がほぼ1000ですので、1 mgを1 mLのDMSOに溶解していただくと1 mMの溶液になります。
DMSOはなるべく乾燥したものをご使用下さい。