BT
比色試薬/金属指示薬
-
製品コードB015 BT
-
CAS番号1787-61-7
-
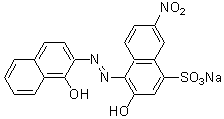
化学名2-Hydroxy-1-(1-hydroxy-2-naphthylazo)-6-nitro-4-naphthalenesulfonic acid, sodium salt
-
分子式・分子量C20H12N3NaO7S=461.38
| 容 量 | メーカー希望 小売価格 |
富士フイルム 和光純薬 |
|---|---|---|
| 25 g | ¥4,700 | 344-00372 |
| 500 g | ¥25,100 | 348-00375 |
性質
一般にEriochrome Black Tと呼ばれる色素で、金属のキレート適定用指示薬や比色定量試薬として使用される。
BTは水、アルコールに溶け易いが、有機溶媒には溶け難い。水溶液は、pH<6で赤色、pH7~11で青色、pH>12で橙色となる。酸解離定数はpKa2=6.3,pKa3=11.5(μ=0.08,20℃)で、多くの金属イオンが共存すると赤色となり、EDTA の添加によって再び青色となる。特に、Ca, Mg, ZnではpH10において、色調変化が起こるため、それらの直接滴定の指示薬として使用される。また、MgやZnによる逆滴定の指示薬として用いることで、多くの金属がキレート滴定できる。
応用可能な金属
キレート滴定指示薬として:
Ca(logK=3.8, pH10), Cd, Hg2+, Mg(logK=5.4, pH10), Mn2+, Pb, Zn, 希土類など
比色試薬として:
Cd, Co, Mg, Zn, 希土類
妨害イオン
Al, Fe3+, Co, Cu, Mn3+など、特にCu, Fe3+は極く微量共存しても指示薬の変色を妨害するので KCN などでマスクする。Al3+, Fe3+, Mn3+にはトリエタノールアミンもマスキング剤として有効である。Mn3+, Fe3+など酸化性のイオンはBTを分解するので、塩酸ヒドロキシルアミンなどの還元剤を添加しておく。
技術情報
表 BTを用いる主な金属の比色定量条件1)
図. BTを指示薬とする滴定の変色例
*注:ご覧になるモニターにより、実際の色合いとは異なる場合がございます。
あくまで目安としてご覧下さい。

参考文献
1) K. Ueno, T. Imamura and K. L. Cheng, "Handbook of Organic Analitical Reagents 2nd Edition", CRC Press, 1992.
2) P. F. Lott, K. L. Cheng and C. H. Kwan, "Spectrophotometric Determination of Thorium with Eriochrome Black T", Anal. Chem., 1960, 32, 1702.
よくある質問
-
Q
BT指示薬を用いたCaの置換滴定の方法を教えて下さい。
-
A
下記方法を参考にして下さい。
【試薬】
0.01~0.001mol/L EDTA標準液
BT指示薬溶液
緩衝液(pH10)
約0.1mol/L Mg-EDTA溶液
【操作】
①試料溶液(Ca濃度1%以下)は必要であればHClまたはNaOHにて中和する。
②溶液100mLにつき緩衝液 2mL,0.1mol/L Mg-EDTA溶液 1mL,指示薬溶液2~4滴を加え、EDTA標準液にて滴定する。
③終点の変色は赤→青。赤味の完全に無くなった点を終点とする。
0.01mol/L EDTA 1mL =0.04008mg Ca
【備考】
・Mg(2+)が全く存在しない場合にはCa(2+)滴定におけるBT指示薬の変色は非常に不明瞭で、Mg(2+)の共存量が増すにしたがって変色は明瞭になる。
Mg-EDTAを添加した場合には MgY(2-) + Ca(2+) →CaY(2-) + Mg(2+)の置換反応は完全に進まず、Ca(2+),Mg(2+)を同時に滴定するような結果になる。
pH10においてMg(2+)3~10%の添加で十分効果が現れる。
・Zn-EDTAをもちいてアンモニアアルカリ性溶液ではCa(2+)と置換反応がおこるので、Mg-EDTAの場合と同様な操作で滴定することが出来る。
・この方法による時はBT指示薬を用いてMg(2+)まるいはZn(2+)を滴定するときと同じく終点の変色は敏感におこるので、0.001mol/L標準液を使用して微量のCaを定量することが出来る。
・BT指示薬の代わりに、カルコンやジンクロームRを指示薬に用いることも出来る。
・Mgその他アルカリ土類金属が共存する場合はその合量が得られる。多量のBa,Srが共存すると終点が不明瞭になる傾向がある。Ca,Mgの混合物の場合にはNN指示薬を用いる方法が便利である。
・Mn,Cr,Fe,Al,Pb,Bi,Sb,Ti,Zr,Th,希土類,Nb,Ta,Ca,Inなどの共存は避けなければならない。
これらのイオンはプラスの誤差を与える。コロイド状のFeが共存すると終点が不明瞭になるのでNa2Sでマスクする。また、Co,Ni,Cu,Zn,Cd,Hg,白金属もチオグリコール酸やアミノエチルメルカプタンなどの添加によってマスクしておく必要がある。
Pb,Bi,Zn,Cd,As,Sb,Sn,Fe,AlなどはBALでマスクする事も出来る。
・多量のPO4(3-)が共存すると妨害が起こるが、CyDTAを滴定指示薬として用いればその妨害を避けることが出来る。
リン酸カルシウムを含む試料溶液に約0.1mol/L Zn-CyDTAを加えpH3~4に調整して良く振り混ぜた後、pH10にしてCyDTA標準液を用いて滴定する。指示薬にはBT指示薬を用い、約60℃に加熱しながら滴定を行なう。
この方法によればモル比で4倍量のPO4(3-)が共存しても妨害を受けず、また同様の方法はMg(2+)滴定の場合にも応用することが出来る。*「キレート滴定」上野景平著(南江堂出版)より
-
Q
Hgの滴定方法を教えてください。
-
A
下記のような方法で行うことができます。また、「XO」を用いた直接滴定もございますので、そちらもご覧下さい。
【試薬】
0.01mol/L EDTA標準液
BT指示薬溶液
緩衝液(pH10)
約0.1mol/L Mg-EDTA溶液【操作】
①試料溶液中のHg2+濃度は100mL中50mg以下にする。
②試料100mLにMg-EDTA溶液5mLを加え、メチルレッド試験紙を用いてNaOH溶液で中和する。
③緩衝液2mL、指示薬数滴を加え、EDTA標準液にて滴定する。
④終点の変色は赤→青。
0.01mol/L EDTA 1mL =2.00059mg Hg【備考】
・Mn2+,Zn2+,Cd2+,In3+,Pb2+などが共存するときにはその合量が求められるので、これらの金属と共存するHgの量を求めるには次の方法が便利である。
上述の滴定を終わった溶液に固形のKI:1~2gを加えると、EDTAと結合していたHg2+はヨード錯塩となるため、Hgと当量のEDTAが遊離する。
そこで0.01M MgまたはZn標準液で指示薬が赤味を生じるまで逆滴定する。
0.01mol/L Mg(またはZn)標準液 1mL = 2.0059mg Hg
・Co2+,Ni2+,Cu2+が共存すると指示薬の変色が妨害されるが、KCNはHg2+もマスクするので、この場合にはマスク剤としてはもちいられない。
・アルカリ土類金属、希土類金属イオンはNH4Fによってマスクされる。
Fe3+はBT指示薬の変色を妨害する。また、I-,CN-および大量のBr-の共存は避けなければならない。
・緩衝液(アンモニア-塩化アンモニウム,pH10)を多量にもちいると、塩化アミド第二水銀の沈殿生成が避けられるので、直接滴定することができる。
ただし、緩衝液の濃度が高いので、終点の変色は多少にぶくなる。
*「キレート滴定」上野景平著(南江堂出版)より
-
Q
Pbの滴定方法を教えてください。
-
A
下記のような方法で行うことができます。
また、「XO」を用いた直接滴定もございますので、そちらもご覧下さい。
【試薬】
0.01mol/L EDTA標準液
BT指示薬溶液
緩衝液(pH10)
約0.1mol/L Mg-EDTA
約0.1mol/L アンモニア水
【操作】
①試料溶液中のPb濃度は100 mL中 30 mg以下にする。
②試料100 mLにMg-EDTA溶液5mlを加え、NaOHにてあらまし中和する。
③必要あればマスク剤を加え、さらに緩衝液2ml、指示薬数滴を加え、EDTA標準液にて滴定する。
④終点の変色は赤→青。
0.01mol/l EDTA 1ml =2.072 mg Pb
【備考】
・Pb2++MgY2-→PbY2-+Mg2+の置換反応は定量的にすすむから、置換したのちpH10にすればPb(OH)2の沈殿を生じることなく滴定することが出来る。
・pH10における滴定であるから、アルカリ金属イオンおよびAg+を除くほとんどすべての金属イオンが妨害し、あるいは一緒に滴定される。したがって共存イオンが多い時はPbSO4として沈殿分離したほうがよい。
・Pb2+と共存するCu2+,Ni2+,Co2+,Zn2+,Cd2+,Hg2+などはKCNでマスクすることができる。
・試料中のPb2+をPbSO4として沈殿分離した場合は、この沈殿を直ちにpH10にてMg-EDTA溶液にとかし滴定することもできる。
・置換滴定によらず試料に過剰のEDTA標準液を加え、MgSO4またはZnSO4標準液で逆滴定することもでき、いずれも正確な結果が得られる。この場合もPbSO4の沈殿は上記に準じて処理することができる。
*「キレート滴定」上野景平著(南江堂出版)より
-
Q
Zn,Cdの滴定方法を教えてください。
-
A
ここでは、BTを指示薬とする直接滴定に関し記載します。
ただし、Cu,Co,Niが溶液中に共存しない場合です。
Cdに関しても同様の方法で滴定することが出来ます。
両者(Zn,Cd)が共存する場合には分別定量が行われます。
滴定の際の液性はアルカリ性になりますので、酸性で行われたい方は「XO」の項目をご覧下さい。
【試薬】
0.01mol/L EDTA標準液
BT指示薬溶液
緩衝液(pH10)【操作】
①試料溶液のZn濃度は100 mL中25 mg以下にする。(Cdは50 mg以下)
②酸性の場合はNaOHで中和する必要があるが、中性付近で加水分解をおこす恐れのある
金属イオンを含む場合はあらかじめ水酸化物として沈殿除去しておく。
③検水100 mLにつき緩衝液2mlおよび指示薬溶液数滴を加え、EDTA溶液で滴定する。
終点は赤→青。赤みが完全に無くなった点を終点とする。
0.01mol/L EDTA 1mL = 0.6539 mg Zn
= 1.1241 mg Cd
【備考】
・BT指示薬をもちいて滴定できるpHは7~10である。pH7以下では遊離色素イオンが赤色を呈し、pH10以上では色素-金属キレートの条件安定度定数が大きくなりすぎるため、いずれも明瞭な終点を認め難い。pH7~10の間でのみ正確な終点がみとめられる。・Cu3+,Co2+,Ni2+が微量でも共存する時はBT指示薬の変色が妨害される。
Fe3+,Ti4+,Al3+,Pb2+などは滴定前に水酸化物として除去することができる。
Al3+および少量のFe3+はトリエタノールアミンで、また少量のTi4+,Al3+はタイロンでマスクすることが出来る。
Uが共存する場合にはH2O2を添加してMg2+標準液で逆滴定すれば、その妨害を防ぐことが出来る。
Mn2+,Zn2+,Cd2+が共存すれば、その合量が得られる。・Znの場合、0.0001mol/L EDTA溶液をもちい1.5 μgのZnを定量、また0.01 mol/L EDTA溶液と超微量ビュレットをもちい0.2 mgのZnを±2 μgの精度で滴定した報告がある。
ミクロ滴定の場合には溶液を30~40℃にあたためた方が終点が明瞭になる。・アルカリ土類金属イオンやMn2+が共存する場合には一緒に滴定されるから酸性領域での滴定が便利である。
・BT指示薬の代わりにジンコンを指示薬としても全く同一条件で滴定することが出来る。
ただし、緩衝液としてはアンモニア-塩化アンモニウム系よりもホウ砂-ホウ酸系のものがよい。
また、ジンコンはCd2+に対して変色しないので、Cd2+滴定の場合にはZn2+標準液を用いて逆滴定しなければならない。アルカリ土類金属イオンが共存すれば一緒に滴定される。*「キレート滴定」上野景平著(南江堂出版)より
-
Q
BT指示薬の調整法を教えてください。
-
A
下記のような調製方法がございます。
ただの水溶液やアルコール溶液では不安定で保存できません。
また、溶液化した[Universal BT]という製品もございますのでご利用ください。①色素純末0.5 g,塩酸ヒドロキシルアミン4.5 gに無水メタノールを加えて100 mLにする。
②色素純末0.2 gをトリエタノールアミン15 mL,無水メタノール5 mLに溶かす。*「キレート滴定」上野景平著(南江堂出版)より
取扱条件
| 性状: | 黒褐色~黒色粉末 |
|---|---|
| 水溶状: | 試験適合 |
| メチルアルコール溶状: | 試験適合 |
| 吸光度(メチルアルコール): | 0.250 以上(520 nm付近) |
| 吸光度(ほう酸緩衝液): | 0.400 以上(620 nm付近) |
| 乾燥減量(105℃): | 7.0% 以下 |
| 鋭敏度: | 試験適合 |
| IRスペクトル: | 試験適合 |











