キット内容
| Monomer Solution | 3 ml × 1 |
| Polymerization Initiator | 30 mg × 1 |
| Polymerization Promoter | 250 µl × 1 |
| Activation Buffer | 3 ml × 1 |
| Enzyme Solution | 100 µl × 1 |
| Crosslinking Solution | 100 µl × 1 |
| Mold | × 10 |
| Cover Glass | × 10 |
保存条件
0-5 °Cで保存して下さい。
必要なもの (キット以外)
- 2–20 µl、20–200 µl、100–1000 µlマイクロピペット
- 0.5 ml、1.5 ml マイクロチューブ
- 18G 注射針
- ピンセット
- スライドガラス
- ゲル作成用湿潤容器 (1 ml マイクロピペットチップ用ケースなど)
- 10 cm dish
- ゲル膨張用湿潤容器 (タッパーなど)
- カミソリまたはメス
- PBS (–)
- DAPI solution (製品コード:D523)
- 24-well plate
- スパーテル
- メスシリンダー
- 氷浴
はじめに
細胞内には複数のオルガネラが存在し、それぞれのオルガネラの構造を解析することが細胞機能の理解や疾病のメカニズム解明において重要となります。細胞内のオルガネラの構造を高解像度にイメージングするためには、高価な電子顕微鏡や超解像顕微鏡が必要です。一方で蛍光顕微鏡では、アッベの回折限界によりオルガネラの構造を解析することは困難です。そこで蛍光顕微鏡でオルガネラを観察するための手法の一つとして2015年にExpansion Microscopy法が開発されました。Expansion Microscopy法は吸水性ゲルを利用してサンプル自体を大きくする技術であり、蛍光顕微鏡では困難であった微小な構造のイメージングが可能となります。
本キットは、Expansion Microscopy法を行うためのゲル作成に必要な試薬および枠を同梱したキットであり、細胞を3次元的に約4倍まで拡張することが可能です。
使用上のご注意
- キットの中の試薬は、室温に戻してからご使用ください。
- ゲルを保管する際は乾燥しないように、水中またはゲル膨張用湿潤容器内で保管してください。
- Cover Glassは割れやすいため、取り扱いにご注意ください。
溶液調製・事前準備
Polymerization initiator solutionの調製
- Polymerization Initiatorに超純水 270 µlをマイクロピペットで加え、溶解する。
- 溶解したPolymerization initiator solutionを25 µlずつ0.5 mlマイクロチューブに小分けし、-20℃で保管する。
- 調製後は直ちに-20℃で保存してください。調製後1ヶ月間安定です。
- 調製後は直ちに-20℃で保存してください。調製後1ヶ月間安定です。
Digestion solutionの調製
1.5 ml マイクロチューブにActivation Buffer 223 µlとEnzyme Solution 7 µlを加え、ピペッティングで混合する。
- Digestion solutionは保存できません。調製したその日のうちに、ご使用ください。
Crosslinking working solutionの調製
1.5 ml マイクロチューブにPBS (–) 223 µl とCrosslinking Solution 7 µlを加え、ボルテックス攪拌を行う。
- Crosslinking working solutionは保存できません。調製したその日のうちに、ご使用ください。
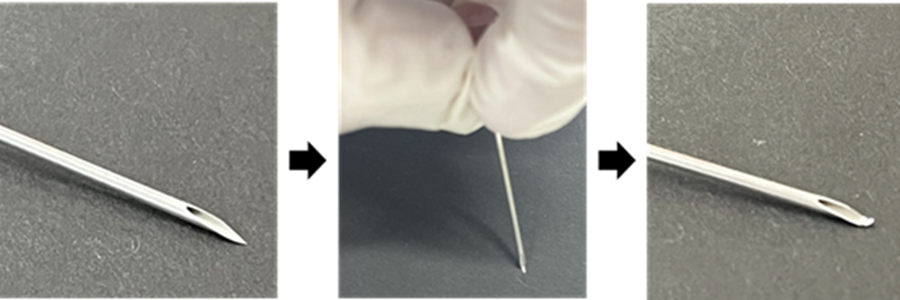
先端を曲げた注射針の準備
※先端に注意しながら、18Gの注射針の先端を平らな机等に押し当て、先を曲げる。
 |
操作
- Cover Glassをピンセットを用いて24-well plateに入れる。
- 細胞培養で使用するため、クリーンベンチ内で行う。
- 細胞をCover Glass上に播種し、インキュベーター(37℃、5%CO2存在下)で一晩培養する。
- 目的の染色および10 µg/ml DAPI水溶液で核染色する。
- 上清を抜き、調製したCross-linking working solution 200 µl を各ウェルに添加し、アルミホイル等で遮光した状態で振とう機上にて一晩室温で攪拌する。
- 上清を抜き、PBS(-) 200 µlで5回洗浄する。洗浄後、PBS(-) 200 µlを各ウェルに加える。
- Mold表面のシールを両面剥がし、スライドガラスに貼る。
- Moldとスライドガラスの間に空気が入っていないことを確認してください。
空気が入っていると溶液が漏れ出る可能性があります。
- Moldとスライドガラスの間に空気が入っていないことを確認してください。
- 先端を曲げた注射針を使用し、操作5.のCover Glassを24-well plateから取り出し、操作6.のMoldの円内に移す。Cover Glassを注射針で持ち上げる際は、ピンセットで取り出しを補助すると操作が簡便になります。

(動画: https://www.youtube.com/embed/LpseTF43aE0) - Monomer Solution 100 µlをCover Glass上に添加し、4℃で30分間インキュベートする。
- Monomer SolutionがMoldの円内全体に浸っても問題ありません。

- 操作8.のインキュベート時間中にゲル作成用の湿潤容器をあらかじめ37℃に温めておく。

- ゲル作成用湿潤容器作成例
1 mlマイクロチップケースの底に水で濡らしたキッチンペーパーを敷いた後、蓋をし、37℃インキュベーター内に入れる。
- ゲル作成用湿潤容器作成例
- 操作8.の上清を吸引除去し、Gelling solution 100 µlをCover Glass上に添加する。
Gelling Solutionの調製は以下に従って調製する。
氷浴上で1.5 mlマイクロチューブにMonomer Solution 190 µl、超純水 2 µlおよびPolymerization Promoter 4 µlを加え、ボルテックス攪拌した後、
Polymerization initiator solution 4 µl を加え、ピペッティングで混合する。

- Polymerization initiator solutionを加えるとゲル化が進行します。操作10の"Gelling solution 100 µl をCover Glass上に添加する"直前にPolymerization initiator solution を加え、調製後は10分以内に使用してください。
- スライドガラスごと操作9.で準備したゲル作成用湿潤容器内に入れ、蓋をし、37℃で1時間インキュベートする。

- ゲル作成用湿潤容器ごとインキュベーターから取り出し、Moldの円内に、調製したDigestion solution 200 µlを添加する。その後、蓋をし、37℃で3時間インキュベートする。

- 操作12.のインキュベート時間中にゲル膨張用湿潤容器をあらかじめ37℃に温める。



➀市販のタッパー ➁濡らしたキッチンペーパーを中に入れる ➂蓋を閉めて37℃インキュベーター内に入れる - 10 cm dishが入る容器を選択すること。
- ゲル膨張用湿潤容器作成例
水で濡らしたキッチンペーパーをゲル膨張用湿潤容器底に敷いた後、蓋をし、37℃インキュベーター内に入れる。
- 10 cm dishに、超純水を約45 ml加える。
- ゲル作成用湿潤容器ごとインキュベーターから取り出し、操作12.のスライドガラスをゲル作成用湿潤容器から取り出す。
- Moldをスライドガラスから取り外した後、ゲルを操作14.の10 cm dishに入れる。
- Moldを外す際にゲルの縁に傷がついても問題ありません。
- この時、Cover Glassが一緒に10 cm dishに入っても問題ありません。

(動画: https://www.youtube.com/embed/bzpiKpsb9LE ) - 10 cm dishを円を描くように揺らし、ゲル全体が超純水で浸るようにする。
- 操作17.の10 cm dishを操作13.で準備したゲル膨張用湿潤容器に入れ、37℃で30分間インキュベートする。

- 10 cm dishの蓋は外した状態でいれること。
- ゲルを傷つけないように注意しながら10 cm dish内の超純水を全て吸引除去する。

- アスピレーターやマイクロピペット、スポイト等を使用する。
(動画: https://www.youtube.com/embed/FCydMTsZAQM )
- アスピレーターやマイクロピペット、スポイト等を使用する。
- 操作19.の10 cm dishに超純水約60 ml入れ、ゲル膨張用湿潤容器の蓋をし、37℃で30分間インキュベートする。

- ゲルを傷つけないように、超純水を加える。
- 操作19.および20.をさらに2回行う。
- 膨張したゲルを下記図のようににカミソリやメス等を使用してカットする。
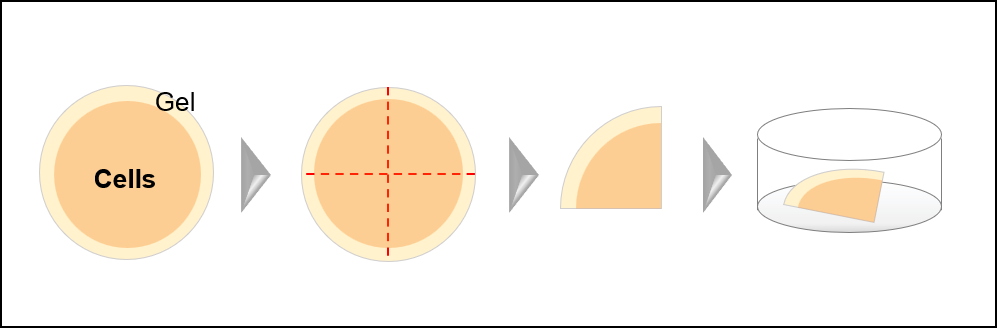
- 観察用35 mm dishに、カットしたゲルをスパーテルを使用して傷つけないように移す。
- 蛍光顕微鏡で観察を行う。
- 観察時には、以下のことを確認して下さい。撮像の操作詳細は"撮像マニュアル"をご参照ください。
撮像マニュアル(https://dojindo.co.jp/products/contents/T517_ImagingManual.html)
- 水浸レンズの使用を推奨します。
- 明視野や位相差で細胞の位置を確認しにくいため、DAPIで核染色した核を目印に焦点を合わせてください。
- 核染色の蛍光強度が低い場合は、10 µg/ml DAPI水溶液3 mlを観察用35 mm dishに加え、室温で30分間染色してください。その後、超純水で洗浄操作を行ってください。
- 観察が困難な場合はゲルが上下逆の可能性がありますので、スパーテルでゲルをひっくり返した後、観察してください。
- 免疫染色の蛍光強度が低い場合は、PBS(–) を加え15~30分間浸し、追加で二次抗体での染色を行ってください。染色後、超純水で3回洗浄し、再膨張させてください。
再膨張時は、操作17から再度行ってください。
- 観察時には、以下のことを確認して下さい。撮像の操作詳細は"撮像マニュアル"をご参照ください。
実験例
HeLa細胞の脱共役剤処理したミトコンドリア外膜と内膜のイメージング
【細胞準備】
- Cover Glassを24 well-plateに入れた後、HeLa細胞(2.0 x 105 cells/ml,500 µl)を播種し、37℃、5% CO2インキュベーター内で一晩培養した。
- 培地を取り除き、HBSS 500 µlで1回洗浄した。
【薬剤処理】 - CCCP (5 µmol/l、10 µmol/l)/血清不含MEM 200 µlを各wellに添加し、37℃で30分間インキュベートした。
【固定化・染色】 - 溶液を取り除き、4 %パラホルムアルデヒド/PBS 200 µlを添加し、室温で15分間インキュベートした。
- 上澄みを取り除き、PBS 200 µlで3回洗浄した。
- 0.1 mol/l NH4Cl/PBS 200 µlを添加した後、室温10分間インキュベートした。
- 上澄みを取り除き、PBS 200 µlで3回洗浄した。
- 0.1% Triton X-100/PBS 200 µlを添加し、室温で10分間インキュベートした。
- 上澄みを取り除き、PBS 200 µlで3回洗浄した。
- 10% Blocking One-P/PBS 200 µlを添加し、室温で1時間インキュベートした。
- 上澄みを取り除き、Can get signal Immunoreaction Enhancer Solution 200 µlで1/200 に希釈したanti-COXⅣ抗体(Rabbit由来)とanti-TOM20抗体(Mouse由来)を添加し、室温で2時間インキュベートした。
- 上澄みを取り除き、PBS 200 µlで3回洗浄した。
- Can get signal Immunoreaction Enhancer Solution 200 µl で1/200 に希釈したAlexa568標識anti-Rabbit IgGとAlexa488標識anti-Mouse IgGを添加し、室温暗所で1時間インキュベートした。
- 上澄みを取り除き、PBS 200 µlで3回洗浄した。
- PBS 200 µlで1/100 に希釈したDAPI solutionを添加し、室温で30分間インキュベートした。
- 上澄みを取り除き、PBS 200 µlで3回洗浄した。
【架橋・ゲル化】 - 調製したCrosslinking working solution 200 µl を添加し、アルミホイルで遮光した状態で振とう機上にて室温で一晩撹拌した。
- 上澄みを取り除き、PBS 200 µlで5回洗浄し、PBS 200 µlを加えた。
- Moldをスライドガラスに貼った。
- 先端を曲げた注射針を使用し、染色操作をしたCover Glassを24-well plateから取り出し、スライドガラスに貼り付けたMoldの円内に移した。
- Monomer Solution 100 µlをCover Glass上に添加し、4℃で30分間インキュベートした。
- 上澄みを取り除き、調製したGelling solution 100 µlをCover Glass上に添加し、事前に37℃に温めておいたゲル作成用の湿潤容器に入れ、37℃で1時間インキュベートした。
【消化・膨張】 - Moldの円内に、調製したDigestion solution 200 µlを添加し、37℃で3時間インキュベートした。
- Moldをスライドガラスから取り外した後、超純水 45 mlを入れた10 cm dishに移し、事前に37℃に温めておいたゲル膨張用湿潤容器に入れ、37℃で30分間インキュベートした。
- ゲルを傷つけないように注意しながら10 cm dish内の超純水を全て取り除き、10 cm dishに超純水 60 mlを入れ、ゲル膨張用湿潤容器に入れた後、37℃で30分間インキュベートした。
- 25.の操作を追加で2回行った。
【観察】 - ゲルを傷つけないように注意しながら10 cm dish内の超純水を全て取り除き、観察用µ-Dish 35 mm, High Glass Bottom(ibidi81158)にゲルを2 x 2 cmにカットしてスパーテルを使用して移した。
- 共焦点レーザー蛍光顕微鏡 (LSM 800, Zeiss) で観察を行った。
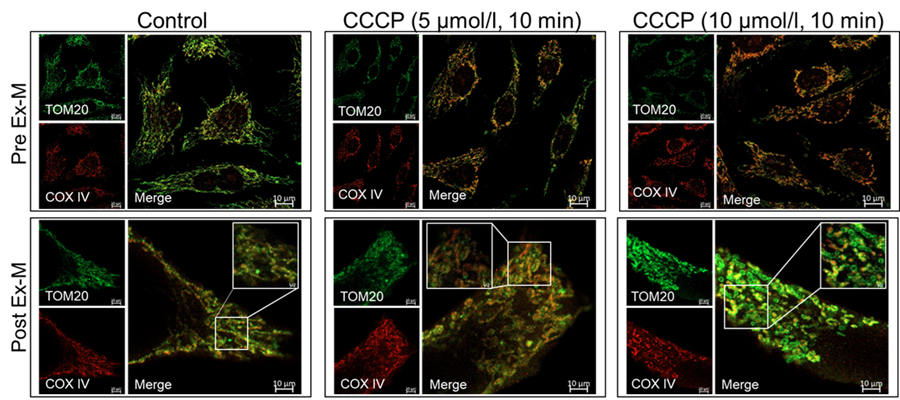
Pre Ex-M
TOM20) Laser Power:1%, Digital Gain:650V Excitation:488 nm Emission:500-550 nm
COXⅣ) Laser Power:2%, Digital Gain:650V Excitation:561 nm Emission:580-620 nmPost Ex-M
TOM20) Laser Power:70%, Digital Gain:700V Excitation:488 nm Emission:500-550 nm
COXⅣ) Laser Power:70%, Digital Gain:750V Excitation:561 nm Emission:580-620 nm図1 膨張処理前後における薬剤処理を行ったミトコンドリアの形態変化
参考文献
1) R. X. Norman et al., ournal of Cell Biology, 2025, 224, e202407116.
This product is covered by U.S. Patent Application No. 17/466,434.
This technology is based on research conducted by Dr. Aussie Suzuki at the University of Wisconsin–Madison.
よくある質問/参考文献
T517: Three-Dimensional Expansion Microscopy Kit (4x 3D-ExM)
Revised Feb., 04, 2026


 を押して省略できます。
を押して省略できます。

