はじめに
バイオフィルムとは、固体液体界面上に形成される菌体外多糖を主要構成成分とした集合体で、水の存在するあらゆる場所に存在しています。医療器具内の細菌汚染やう蝕・歯周病、食中毒、産業分野においても金属の腐食や排水管の汚染などはバイオフィルムが要因とされ、様々な分野でバイオフィルムの関与が指摘されています。そのため、抗バイオフィルム活性を有する素材の探索が注目を集めています。
Biofilm TestPiece Assay Kitはクリスタルバイオレット染色法により素材ごとのバイオフィルム形成量の違いを測定することができます。独自開発した素材を固定することのできる蓋を使用することで、洗浄・染色操作によりバイオフィルムが剝がれることなく、複数サンプルを簡便に測定することが可能です。
キット内容
| 24 tests | |
| TestPiece Holder | x 1 |
| Crystal Violet Solution | 50 ml x 1 |
保存条件
冷暗所にて保存してください。
必要なもの (キット以外)
-
- 試験片(サイズ: 20 × 10 × 1–3 mm (縦 × 横 × 厚さ))
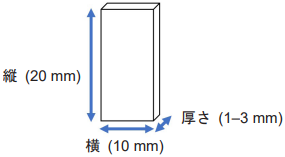
- 試験片(サイズ: 20 × 10 × 1–3 mm (縦 × 横 × 厚さ))
-
- Falcon® 24-wellプレート (同仁化学製品コード: B608, 24-well Plate)
- プレートリーダー(590 nm付近の吸光フィルター)
- インキュベーター
- 1000–5000 μl マイクロピペット
- エタノール
- 生理食塩水
使用上のご注意
- バイオフィルム形成条件(培地・培養時間等)は菌種により異なります(表1参照)。バイオフィルム形成条件を確立後、バイオフィルム形成測定を行ってください。
- 一度使用したTestPiece Holderの再利用は、雑菌等のコンタミネーションの可能性があるため推奨いたしません。また、TestPiece Holderは加熱により変形しますので、再利用のためのオートクレーブ等加熱滅菌はできません。
- 24-wellプレートはメーカーによって仕様が異なり、小社ではFalcon® 24-wellプレートが適合することを確認しております。お持ちでない方は別途ご準備頂くか小社で取扱がございますのでお求めください。
-
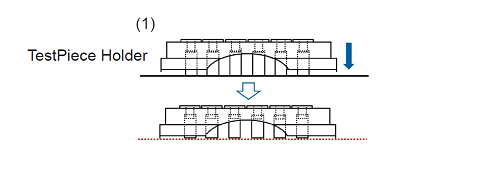
- TestPiece Holderには向きがあります。図1のようにTestPiece Holderの突起と24-wellプレートの"FALCON"の文字が重なるように被せてください。
操作
バイオフィルム形成量測定
-
1. 試験片をTestPiece Holder に固定する。
- 試験片はコンタミネーションに気を付け、傷がつかないようにピンセット等で固定してください。
- TestPiece Holder のクリップ部分に試験片を軽く差し込み、清潔な平面にHolder を押し当てて試験片の高さをそろえてください。
- 弊社Web サイトに固定する際の動画を掲載していますのでご参照ください。
-
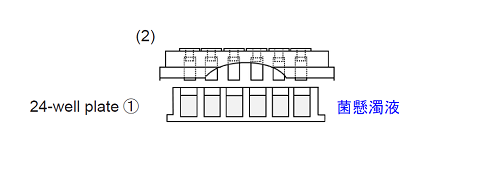
2. 24-well plate ①の各ウェルに菌懸濁液を1.8 ml 入れる。試験片を固定したTestPiece Holder を被せて適温に設定したインキュベーターで培養する ( 試験片上にバイオフィルムが形成される)。
- TestPiece Holder の向きにご注意ください。
- 菌種により、バイオフィルム形成条件が異なります。( 表1)
-
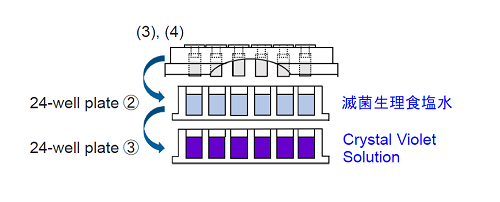
3. 24-well plate ②の各ウェルに滅菌生理食塩水2.0ml を、24-well plate ③の各ウェルにCrystal Violet Solution 2.0 ml を入れる。
4. 24-well plate ②に手順(2) のTestPiece Holder を浸し、30 秒ほど上下左右に軽く揺らして洗浄する。
続けて24-well plate ③にTestPiece Holder を被せて室温で30 分静置する。- 洗浄の際は、TestPiece Holder を緩やかに生理食塩水に浸し、激しい振とうは避けてください。バイオフィルムが剥がれたり、試験片がずれたりする可能性があります。
-
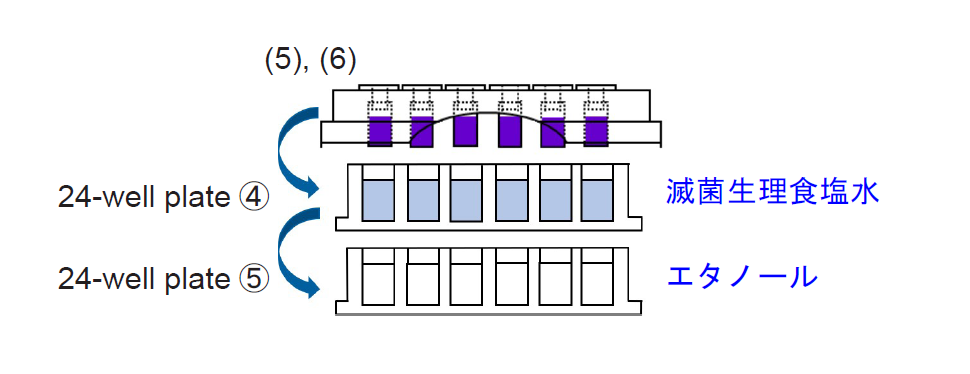
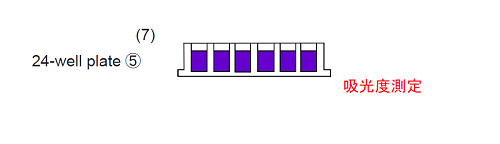
5. 24-well plate ④の各ウェルに滅菌生理食塩水2.0 mlを、24-well plate ⑤の各ウェルにエタノール 2.0 mlを入れる。
6. 24-well plate ④に手順(4) のTestPiece Holder を浸し、30 秒ほど上下左右に軽く揺らして洗浄する。続けて24-well plate ⑤にTestPiece Holder を被せて室温で30 分静置する。
- 洗浄の際は、TestPiece Holder を緩やかに生理食塩水に浸し、激しい振とうは避けてください。バイオフィルムが剥がれたり、試験片がずれたりする可能性があります。
- Crystal Violet の抽出効率はバイオフィルムの形成状態によって異なる場合があります。抽出効率を最適化する場合には、エタノール以外の抽出液をご検討ください。
-
7. 24-well plate ⑤からTestPiece Holder を取り外し、マイクロプレートリーダーで590 nm 付近の吸光度を測定する。
- 吸光度が高く、吸光度計の上限を超える場合は、希釈してから測定して下さい。
実験例1
ポリスチレン(PS) に対するバイオフィルム形成実験例:黄色ブドウ球菌
- 黄色ブドウ球菌のバイオフィルム形成は24 時間のインキュベートを2 回行ったため、24-well プレートを6 枚使用した。
- TestPiece Holder にポリスチレンの試験片 (20 × 10 × 2 mm ( 縦 × 横 × 厚さ)) を固定した。
- 培養した菌懸濁液をMueller-Hinton broth (MHB) 培地で約107 CFU/ml となるように希釈して播種用菌液とし、24-well plate ①の各ウェルに1.8 ml ずつ播種した。
- 24-well plate ①にTestPiece Holder を被せ、37 °C で24 時間インキュベートした。
- 24-well plate ②の各ウェルに菌を含まないMHB 培地を1.8 ml ずつ入れ、手順(3) のTestPiece Holder を被せ、37 °C でさらに24 時間インキュベートした。
- 24-well plate ③の各ウェルに滅菌生理食塩水2.0 ml を入れた。24-well plate ④の各ウェルにCrystal Violet Solution 2.0 ml を入れた。
- 手順 4 のTestPiece Holder を24-well plate ③に浸し、30 秒ほど軽く揺らして洗浄した。続けて24-well plate ④にTestPiece Holder を被せ、室温で30 分静置した。
- 24-well plate ⑤の各ウェルに滅菌生理食塩水2.0 ml を入れた。24-well plate ⑥の各ウェルにエタノール2.0 ml を入れた。
- 手順 6 のTestPiece Holder を24-well plate ⑤に浸し30 秒ほど軽く揺らして洗浄した。続けて24-well plate ⑥にTestPiece Holder を被せ、室温で30 分静置した。
- TestPiece Holder を取り外してエタノールで4 倍希釈し、マイクロプレートリーダーを用い595 nm の吸光度を測定した。
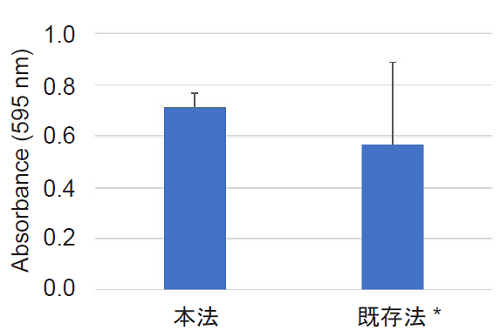
図2 PSに対するS. aureusのバイオフィルム形成
本法で測定した結果のデータは既存法と比較して、バラつきが小さいことが確認できた。
- 既存法: 試験片をシャーレやビーカー等の容器の底に静置してバイオフィルムの形成・評価をする方法
実験例2
素材ごとのバイオフィルム形成実験例: 黄色ブドウ球菌
実験手順は、実験例1と同様。
-
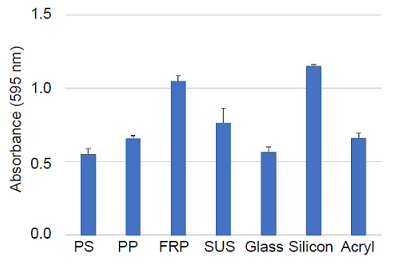
図3 素材ごとのバイオフィルム形成
-

図4 素材ごとのバイオフィルム形成の写真
| 菌種 | 菌希釈培地 | 接種菌濃度 (CFU/ml) |
培養時間 (h) |
| Pseudomonas aeruginosa | Brain Heart Infusion | 107 | 5–6 |
| Staphylococcus aureus | Mueller-Hinston Broth | 107 | 48* |
| Escherichia coli | Brain Heart Infusion | 107 | 72* |
- 24時間ごとに培地交換を行って培養しています。
本キットは福岡県工業技術センター生物食品研究所との共同開発品です。
-------------------------------------------------------------------------------------------------
FalconはCorning Incorporated, Life Sciencesの登録商標です。
Product Number: 353047
Falcon® セルカルチャー24ウェル マルチウェルプレート 平底 フタ付き
-------------------------------------------------------------------------------------------------
よくある質問/参考文献
B606: Biofilm TestPiece Assay Kit
Revised Jun., 01, 2023


 を押して省略できます。
を押して省略できます。