 |
| トップページ > 新規化合物を用いたROSの検出 |
 |
薬の蛍光標識による可視化株式会社同仁化学研究所 岩本 正史 私たちの生活において、画像には訴求力があり、また多くの情報が含まれている。生物学においても同様で、直接眼で見て理解することは重要である。そのため、蛍光標識による可視化は生物学の様々な分野で盛んに取り入れられ、それに伴う近年の生物学の進歩は目覚ましいものがある。今回は抗体やタンパク質などの生体高分子への蛍光標識ではなく、より低分子の薬剤への蛍光標識について紹介する。 Ternatin(1, Fig.1)は、マッシュルームから単離されたN -メチル環状ヘプタペプチドであり、in vitro、in vivoにおいて脂肪蓄積抑制効果があることが確認された。しかし、その生物学的作用機構や標的細胞は未だ解明されていない。そこでShimokawaらは、ternatinを蛍光標識し、可視化することでternatinの脂肪蓄積抑制機構の解明を試みた1)。 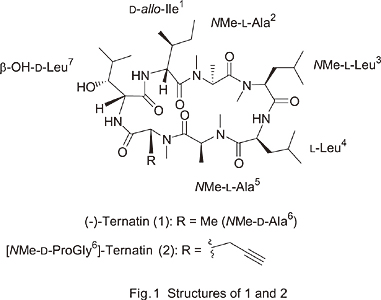
初めに、ternatinの構造活性相関を調べ、Ile1とLeu4のアミノ酸残基が脂肪蓄積抑制作用に重要であることを確認した。その結果を基に、高活性の[N Me-D-ProGly6]-ternatin(2, Fig.1)を設計、合成し、Huisgen反応(Click Chemistry*)によりFITC標識した化合物3(FITC標識ternatin)を合成した。この蛍光標識化合物はternatinよりも活性は低いものの脂肪蓄積抑制作用を有することが確認された。そこで、この化合物3を用いて、ternatinの細胞内動態観察を行った。実験には3T3-L1細胞を用いたが、これはternatinが3T3-L1細胞(マウス前駆脂肪細胞)の分化を初期の段階で抑制していることが最近の研究で示唆されたからである。化合物3で処理した3T3-L1細胞を蛍光顕微鏡で観察すると、細胞内に強い蛍光が見られ、その蛍光は細胞内のある特定の小器官に局在していることが確認された。その詳細については未だ不明であるが、Shimokawaらの合成した蛍光標識ternatinによって、ternatinが3T3-L1細胞の特定器官に作用することが明確になった。本研究はternatinの脂肪蓄積抑制の生物学的作用機構解明の足がかりになるものと考えられる。 ところで、FITCなどの蛍光色素を低分子の生理活性化合物に標識する際には、その本来の性質が失われないような注意が特に必要である。 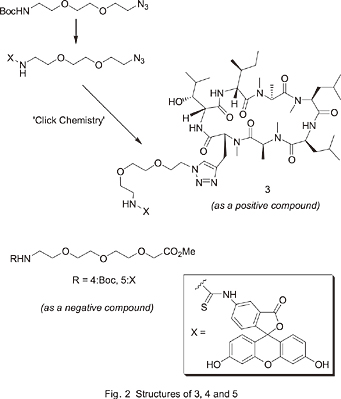
今回Shimokawaらが行ったように、目的化合物の生理活性部位を的確に判断し、生理活性に影響がない部位に蛍光色素を導入しなければならない。また、標識に際しても、抗体やタンパク質と異なり、特定の標識部位(スルフィドやアミノ基)を持たないことも多いため、足場となる官能基を導入しなければならないことなど、低分子の蛍光標識ではより課題が多い。しかし、今回紹介した論文にもあるように、生体内での薬剤の動態観察には、蛍光標識化合物の有用性が高いといえる。どの細胞に作用するのか、さらには細胞のどの部位に作用するのか、その後の代謝はどのように行われるのか、など多くの情報を得られる可能性が秘められている。特に、薬の効用は確認されているがその機構が不明な薬(漢方など)に対しては大いに役立つであろう。今後ますます薬剤の蛍光標識が増えるにしたがい、今まで見えなかったことが見えてくることを期待したい。 参考文献1) K. Shimokawa, O. Ohno, K. Yamada, Y. Oba and D. Uemura, Chem. Lett, 2009, 38 (2), 150-151. *Click Chemistry |
| Copyright(c) 1996-2009 DOJINDO LABORATORIES,ALL Rights Reserved. |