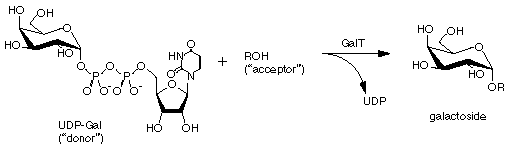
(株)同仁化学研究所 佐々本 一美
糖鎖生物学が非常に注目されており、その機能に着目した薬剤 の開発も盛んに行われている1)。糖鎖の多様性はタンパク質や核酸 と大きく異なっている。タンパク質に対する核酸の様に、構造を 一義的に決定する情報分子が存在しないし、また、一級および二 級水酸基からのみ成る糖自身の構造上の多様性も特異な点である。 このため、糖鎖を自由に合成する技術はタンパク質や核酸と比べ て大きく立ち遅れていたが、最近になって固相合成についての報 告が多くなされており、自動化がいよいよ現実のものとなってき た。とは言え、研究者が望み通りの糖鎖を自由に自動合成できる レベルではなく、依然として主流は酵素を利用する合成である。酵 素法は化学合成と比べ、高い選択性や穏和な反応条件、また、面 倒な保護・脱保護を必要としないなどメリットは大きく、これま で多くの糖鎖合成に利用されてきた。
酵素法の場合、グリコシド結合形成を触媒する酵素は、glycosidase とglycosyltransferaseの2種類であるが、glycosidaseは反応が逆 向きなので収量が低く、普通はglycosyltransferaseが利用される (図1)。この場合の基質は糖ヌクレオチド(酵素が動物由来の場 合、ヌクレオチドは UDP または GDP)であるが、最大の課題は基質が高価なことである(例えば、UDP-galactose は 5 mg で1万円以上)。glycosyltransferase がクローニングによって容易に入手できるようになってきた現在、基質の供給の問題はさらに深刻 になっている(安価に化学合成する方法も Hindsgaul2) らによって報告されているが、生物・医学研究者に恩恵をもたらしてはいな いようだ)。
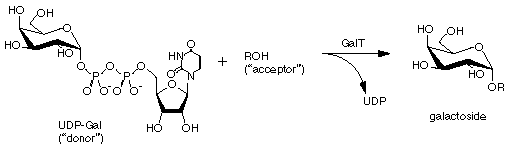
図1:galactosyltransferase(GalT)によるグリコシド形成反応
これらの問題を回避する代表的な二つのアプローチを紹介した い。Wang3)らのグループは、galactoside の生合成経路上の4種類の酵素(GalK, GalPUT, GalU, PK)を大腸菌で発現させ、His-Tag によって樹脂に固定し、糖ヌクレオチドの再生システムを構 築した(図2)。出発原料の acceptor, PEP, galactose(および、触媒量の ATP, UDP,Glc-1-P)を用い、生理的条件下、樹脂およびglycosyltransferse と24 ℃、4日間反応させる。樹脂は再生も可能である。これによって、種々の galactoside を 70 % 以上の収率で得ている。
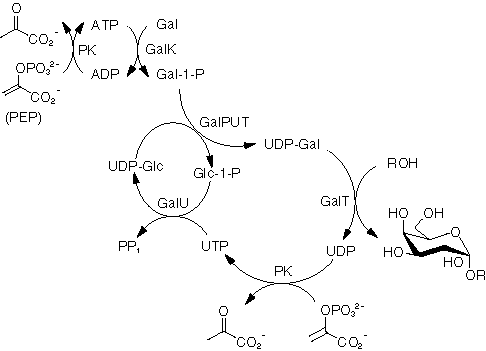
図2: UDP-Gal の生合成経路
一方、Blixt4) および Wang5) らのグループはそれぞれ独立に、基質としてもっと安価な UDP-glucose(数十倍安い)を利用する方法を報告している。 galactosyltransferase と UDP-glucose-4'-epimerase(galactose 再生酵素)との融合タンパク質を大腸菌で発現させることにより、gスケールの経済的な糖鎖合成を実現してい る。これらは、糖のもつ可能性をさらに引き出すためにも重要な アプローチである。
1) 例えば、J. Alper, Science, 291, 2338 (2001).
2) M. Arlt and O. Hindsgaul, J. Org. Chem., 60, 14 (1995).
3) X. Chen, J. Fang, J. Zhang, Z. Liu, J. Shao, P. Kowal, P. Andreana, and P. G. Wang, J. Am. Chem. Soc., 123, 2081 (2001).
4) O. Blixt, J. Brown, M. J. Schur, W. Wakarchuk, and J. C. Paulson, J. Org. Chem., 66, 2442 (2001).
5) J. Fang, X. Chen, W. Zhang, J. Wang, P. R. Andreana, and P. G.Wang, J. Org. Chem., 64, 4089 (1999).