 |
| �@�g�b�v�y�[�W > �����q�`���𗘗p�������_�F���^���q�F���V�X�e���̊J�� |
 |
||||||||||||||||||||||||||
�����q�`���𗘗p�������_�F���^���q�F���V�X�e���̊J��
|
||||||||||||||||||||||||||
 |
�y�� �D�u ��q��w���H�w�� ���ʌ����� |
 |
���� ���m ��q��w�@�w�� ��q��w���H�w�������������H�w�� ���� |
Abstract
�@�@Multipoint recognition is an important strategy which is widely used in biological systems for enhancing binding affinity and selectivity. By mimicking these recognition systems, many researchers have attracted much attention for the design of artificial supramolecular systems over the last several years. In this review, we described the development of supramolecular sensor based on the multipoint molecular recognitions. Several design concepts of molecular recognition systems based on�@�i1�jself-assembly of amphiphilic probes,�@�i2�jmolecular recognition probes/cyclodextrin complexes,�@�i3�jmolecular recognition probes/dendrimer complexes, and�@�i4�jmolecular recognition moieties-modified linear polymer have been reviewed. These bio-inspired molecular recognition systems based on the formation of supramolecular complexes are expected for the development of novel nanomaterials or functional materials.
1�D �͂��߂�
�@�����ɂ����ďd�v�Ȗ�����S���Ă��鐶�̓��̕��q�́A����߂Đ��k�ōI���ɋ@�\���Ă���B���̓��̕��q�͂��̓����������I�ɒ��߂�����i�t�B�[�h�o�b�N���߁j�A���̓��̏����q�����ȑg�D�I�ɕ����̂��`�����ċ@�\�������肷�邱�ƂŁA�����̈ێ����s���Ă���B�Ⴆ�A�^���p�N���͑a�����A�~�m�_�Ɛe�����A�~�m�_����\������Ă���A���e�}���̍����q�ł���B���̍\���䗦�͒ʏ�̐��n���^���p�N���ł͂قړ��ʂł���A���^���p�N���ł͑a�����A�~�m�_�̊����������B�^���p�N���́A�����ɂ����ă|���y�v�`�h���̑a�����c���̂裂̖������ʂ����A���̑a������͂ɂ��a���ʂ���j�Ƃ��ċ���̌`�Ԃ��Ƃ�B���ɂ��A�y�f��R�́A DNA �� RNA �Ȃǂ̑��푽�l�ȕ��q�����̓��Ŏ��ȑg�D�I�ɍ����\�����`�����ĕ��G�ȋ@�\�����Ă��� 1�j �B���̂悤�ɁA�����̒����i���̉ߒ��ɂ����Ēz���������Ă����I���Ȑ��̋@�\�ɕ���āA�l�H�n�̍������q�ɂ���č����\���`���₻�̋@�\���������邾���łȂ��A����𗽉킷�镪�q�̐v��J�����������̌����҂ɂ���Đi�߂��Ă���B
�@�����ɂ����ẮA��������L���錋���ł��鐅�f���������x�ȕ��q�F���̔����ɑ傫���֗^���Ă���B���̓��ł͎��͂����ŕ���ꂽ�e���I�Ȋ����ł���Ȃ���A���q�F���⎩�ȑg�D�����N�������ʂ��a���I�ȏ�ɂ������悤�A�I���ȕ��q�v���Ȃ���Ă���B�^���p�N���̈��ł���y�f�͓���̊�Ɣ�������y�f�������ʂ������A���̊�̕��q�F����ł��銈�����ʂ̑������a����ɑ��݂��Ă���B���̂悤�ɁA���x�ȕ��q�F������������ɂ����ĕ��q�F���ɓK��������`�����邱�Ƃ��d�v�ł���B�l�H�n�ɂ����Ă��A�^�[�Q�b�g�ƂȂ����̃^���p�N����F���ł��鍇�����q�̊J�����i�߂��Ă����B���̑�\�I�ȗႪ���i�ł���A�^�[�Q�b�g�ƂȂ�^���p�N���ɉ����ĕ��q�F�����ʂ��ɕ��q�v���č���Ă��� 2�j �B�������A���ᕪ�q�ʂ̕��q���^�[�Q�b�g�Ƃ������q�F���ɖڂ�������ƁA�]���^�̐l�H�n�̍������q�͗L�@�n�}���ł͍������q�F���\�������̂́A�ɐ��n�}�ł��鐅���ł͕��q�̑��ݍ�p���ł�������邽�߂ɗL���ɋ@�\���Ȃ��ꍇ�������B�Ⴆ�A�N���E���G�[�e���͗L�@�n�}���ɂ����Ă��̊T�C�Y�ɉ����ē���̃A���J�������C�I���ƑI��I�Ɍ������`�����邪�A�����ł͂��̌����萔�͔��ɏ����� 3�j �B�܂��A�����̗L�@���q�͑a�������������̂��������߂ɁA���ւ̗n�𐫂��ۑ�ƂȂ��Ă���B
�@���̈���A��r�I�P���ȍ\���̕��q���m��g�ݍ��킹�������q�^�̕��q�F���v���[�u���ߔN���ڂ��W�߂Ă���B�����q�^�̕��q�F���v���[�u�́A�@��������r�I�e�ՂŒ�R�X�g�ł���A�A���q�F�����ʂ������q���g�ݍ��킹�邱�Ƃő��_�ł̕��q�F�������҂ł���A�O�����ɉ��������q�\���̕ω��ɂ���ĕ��q�F���\�𐧌�ł���A�Ȃǂ̗��_����������B�M�҂�̃O���[�v�ł́A�]���� 1�F1 �^�̑��ݍ�p�Ɋ�Â����q�v�ł͓����Ȃ����l�ȕ��q�F���@�\��L����A�����q�����̌`���𗘗p�������q�F���V�X�e���̊J����i�߂Ă��� 4�j �B�{�e�ł́A�ߔN�̒����q�����̌`���𗘗p�������q�F���n�ɂ��āA�M�҂�̌����𒆐S�ɏЉ��B
�Q�D���ȉ�`���𗘗p�������q�F���V�X�e��

�@�e�������ʂƑa�������ʂq���ɕ��������e�}�����q�́A�ՊE�~�Z���Z�x����ƕ��q���m�����ȉ���A�~�Z���`�����邱�Ƃ��m���Ă���B�ՊE�~�Z���Z�x�͗��e�}�����q�̐e�������ʂƑa�������ʂ̃o�����X�iHydrophile-Lipophile Balance, HLB�j�ɂ���Č��܂�B�M�҂�́AHLB �q�F���Ȃǂ̊O���h���ɂ���ĕω������A���q�F���ɔ����Đ����鎩�ȉ��Ԃ̕ω������w�I���Ō��o���邱�Ƃ̂ł��闼�e�}�����q�̊J�����s�����B�} 1 �ɊJ�������N���E���G�[�e���^���e�}���A�]�v���[�u�i15C5-Azo-Cn�j�̊�{���i�������� 5�j, 6) �B�e�������ʂƂ��Ďl���A�����j�E���A�a�������ʂƂ��Ē�����A���L��������ь����ϊ����ʂł���A�]�x���[���A���[�ɃA���J�������C�I���F�����ʂł���N���E���G�[�e�����i�i�x���]-15-�N���E��-5�j�������B�A�]�x���[���͎��O���Ǝ˂ɂ����π-π * �J�ڂɗR������ 350 nm �t�߂̋z�����傫���������邪�A�A�]�x���[���������ƁA��N�q���ݍ�p�ɂ���āA���q���m���ςݏd�Ȃ�����ԁiH ��j�ł͒Z�g���V�t�g�A����Ĕz�u���ꂽ��ԁiJ ��j�ł͒��g���V�t�g���������Ƃ��m���Ă��� 7�j �B15C5-Azo-Cn �ɁA��X�̃A���J�������C�I����Y�������Ƃ��̃C�I���I�𐫂ɂ��ċz���x��iA370/A420�j���Ƃ��Č��������Ƃ���A15- �N���E��-5 �� 1�F1 ���̂��`�����邱�ƂŒm���� Na�{�C�I�������A�C�I�����a�̑傫�� K�{�C�I����Y�������n�ɂ����āA���傫�ȋz���x�ω�����ђZ�g���V�t�g������ꂽ�B����́AK�{�C�I���ɂ���ăT���h�C�b�`�^�̓�ʑ̌`���ɂ�������i���ꂽ���߂ł���ƍl������B�܂��A���̉�����̓A���L�������Ɉˑ����An = 6 �̏ꍇ�ɍł����� K�{�C�I���I�𐫂�����ꂽ�B�����ɂ����ċ����C�I���̔z�ʌ����ɗU�N���ꂽ����`������ɂ́A��͂����߂邽�߂ɓK���Ȓ����̃A���L�������K�v�ł��邪�A��������ƃA���L�����̑a�������ݍ�p�ɂ���ċ����C�I�����Ȃ������ł����ȉ�������邽�߁A�����C�I���ɑ���F���\�͒ቺ���邱�Ƃ��킩��B�ȏ���A�A���J�������C�I����F�����邱�ƂŃv���[�u���q���P���q�̏�Ԃ����ʑ̂��`�����A�z���X�y�N�g���̕ω��Ƃ��Ċώ@���邱�Ƃ��ł����B���̉�`���ɂ̓A���L�������̒����A�܂�a�������ʂɂ�����a�������ݍ�p�̋����𐧌䂷�邱�Ƃ��d�v�ł��邱�Ƃ𖾂炩�ɂ����B�]���A�����ł̃A���J�������C�I���F���͓���Ƃ���Ă������A�C�I���F���ɔ�����`���̐���ɂ���Ď����ł���_�������[���B
�R�D�V�N���f�L�X�g������p�������q�F���V�X�e��
�@�V�N���f�L�X�g�����icyclodextrin,CyD�j�́A�O���R�[�X���q���m��α-1,4 �O���R�V�h�����Ō������Ă����̃I���S���ł���A���̊��`������O���R�[�X���q���ɉ����āAα-CyD�i6 �j�Aβ-CyD�i7 �j�Aγ-CyD�i8 �j�� 3 ��ނ��m���Ă���B CyD �͊̓������a����ł��邽�߁A�L�@���q��a�������ݍ�p�ɂ���ڂ��A���艻���邱�Ƃ��ł���B���̐����𗘗p���āA����܂łɐH�i�≻�ϕi�A���i����ւ̉��p���i��ł���B�����ŕM�҂�́ACyD �̑a����ɒ��ڂ��A�����Ɏ�X�̕��q�F���v���[�u���ڂ��������q�����̂��`�������邱�Ƃɂ��A�V�����@�\���������邱�Ƃ���Ă���B

�@�O�q�����n�Ɠ��l�ɔF�����ʂɃx���]-15- �N���E��-5 ��p�����u���^�̃v���[�u�i15C5-C3Py�j��v�����i�} 2�j 8�j,9) �B15C5-C3Py �͗L�@�n�}���ł͂��̊T�C�Y�ɑΉ����� 1�F1 �^���̂��`������ Na�{�C�I���ɑI�𐫂��������A�����ł́Aγ-CyD ���݉� K�{ �̓Y���ɂ���ăs�����̃��m�}�[�u�����������A���g�����ŐV���Ƀu���[�h�Ȍu������B����� 15C5-C3Py �� γ-CyD �ɕ�ڂ���� K�{�C�I����F�����ăT���h�C�b�`�^�̓�ʑ̂��`���������ƂŐ������_�C�}�[�u���ł���A������ K�{�C�I���݂̂������x�Ɍ��o�ł��邱�Ƃ𖾂炩�ɂ����B
�@�܂��A�x���]-15- �N���E��-5 ����уW�s�R�����A�~�m��� 2 �̈قȂ镪�q�F���T�C�g�� 1 ���q�̗����[�ɗL����W�g�s�b�N�^�̃A�]�v���[�u�i15C5-Azo-dpa�j��v�����i�}3�j�j 10) �B 15C5-Azo-dpa �́A�����ɂ����� γ-CyD �� 2 ���q��ڂ��ꂽ�i15C5-Azo-dpa�j2/γ-CyD �����̂ƂȂ邱�Ƃ� Job plot �ɂ���ڔ�̎Z�o���m�F���Ă���B�����[�����ƂɁA���̕����̂́AZn2�{�AK�{�ACO32�|�܂��� CH3CO2�| �����݂��Ă��鎞�ɂ̂݁A��ʑ̂˂���\�����Ƃ邱�Ƃ� ICD �X�y�N�g������� NOESY ����ɂ�薾�炩�ɂȂ����B���ɁACO32�| �ˋ��ɂ���đ傫�Ȃ˂���\�����āA�X�v���b�g�^�̌����ȗU�N�~��F���������B���̂悤�ɁA���q�F���v���[�u�� CyD ��g�ݍ��킹�������q�����̂́A���_�ŕ��q��F�����邱�Ƃɂ���āA���q�̋�Ԕz�u�𐧌䂷�邱�Ƃ��ł��A���l�ȕ��q�\�����Ƃ蓾��B���̕�ڍ\���ω��������Ƃ��Ď��o�����ƂŁA���l�ȉ����@�\��L���鉻�w�Z���T�[�̊J�������҂ł���B

�@���ɁA���̌��o��ړI�Ƃ��āA���q�F�����ʂ��N���E���G�[�e������t�F�j���{�����_�ɕς������q�F���v���[�u�iC1-APB�j��v�����i�} 4�j�j 11) �B�t�F�j���{�����_�́A�����q�Ȃǂ̃V�X�W�I�[����L���鉻�����Ɖt�I�Ȋ�G�X�e�����`�����邱�Ƃ��L���m���Ă���B��ʓI�ɁA�t�F�j���{�����_�̓t���N�g�[�X�I�𐫂ł��邪�A���͂̊���ω������邱�ƂŁA���̑I�𐫂𐧌�ł���B�܂����߂ɁAC1-APB �� CyD �Ƃ̒����q�����̌`���ɂ��Č��������Ƃ���AC1-APB �͒P�Ƃł͐����Ŏ��ȉ���ĂقƂ�nju�����Ȃ����Aβ-CyD ��Y������ƁA�����ł��s�����R���̃��m�}�[�u�������������������B C1-APB �� CyD �̕�ڋ����ɂ��Č��U�N�d�q�ړ��iPET�j�̊ɘa���Ԃׂ��Ƃ���AC1-APB �P�Ƃ� α-CyD �������ɔ�ׂ� β-CyD �������ł̂݁A�ɘa���Ԃ� 2�`3 �{�����Ȃ��� 12�j �B����́AC1-APB �̃s�������ʂ� β-CyD �ɕ�ڂ���Ē����q�����̂��`�����Ă��邱�Ƃ������Ă���B C1-APB �� β-CyD �Ƃ̒����q�����̌`���ɂ���� C1-APB �̐����ł̎��ȉ���}�����ꂽ���Ƃɉ����āA�s�������͂̊����a����ɂ�����Đ��ɂ��������}����ꂽ���ƂŁA���m�}�[�u�����������邱�Ƃ����炩�ɂȂ����B���� C1-APB/β-CyD �����̂̓����������ɂ��ĕ]������ƁA�t���N�g�[�X���݉��ł� pKa �̒l�� 7.95 ���� 6.06 �ւƃV�t�g�����B���� pKa �̒ቺ�ɂ��A�����������ɂ����ē��̓Y���ɂ��u�����x�̑����������A�����������ł̓��̌��o���\�ƂȂ����B���� C1-APB/β-CyD �����̂ł́A�s�����u���c���d�q���^�́A�t�F�j���{�����_���d�q��e�̂ƂȂ��Ă���BC1-APB/β-CyD �����̂͒����������A�������݂��Ȃ���Ԃł̓s�����u���c����_�^�i�����^�j�̃t�F�j���{�����_��e�̂ւ� PET �ɂ��������Ă��邪�A���ƃt�F�j���{�����_�̃G�X�e���`���ɂ���ēd�q��e�����������APET �Ɋ�Â��������j�Q���ꂽ���ƂŁA�u�������鉞���@�\�ɂȂ��Ă���B
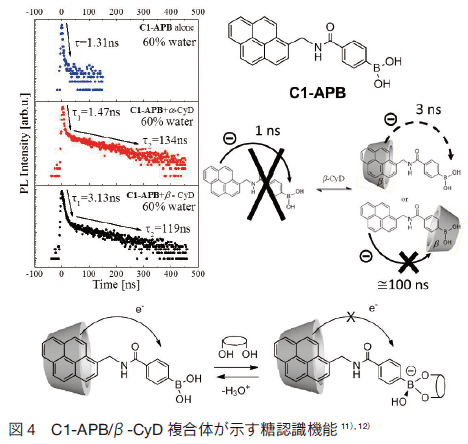
�@����ɁAC1-APB �� γ-CyD �̓��_��� 3 �ʂ��A�~�m������ 3-NH2-γ-CyD ��p���Ă��̓��F���@�\�ɂ��ĕ]�������Ƃ���A�����[�����Ƃ� C1-APB/3-NH2-γ-CyD �����̂̓O���R�[�X�ɍ����I�𐫂��������Ƃ𖾂炩�ɂ����i�}5�j 13) �BC1-APB/3-NH2-γ-CyD �����̂̃O���R�[�X�F���@�\���𖾂��邽�߂ɁAγ-CyD �̈ꋉ���_��� 6 �ʂ��A�~�m������ 6-NH2-γ-CyD �ɂ��ē��l�ɓ��F���@�\��]�������Ƃ���A�A�~�m�����Ă��Ȃ� γ-CyD �Ɖ������قڈ�v�����B�����̌��ʂ��AC1-APB �̓��F�����ʂł���t�F�j���{�����_���ʂ� β-CyD �̎��Ɠ��l�� 6 �ʂ̈ꋉ���_��ł͂Ȃ��A3 �ʂ̓��_��ɂ��邱�Ƃ��킩��B���̂��Ƃ���A�t�F�j���{�����_�Ɠ��̌����`���ɉ����ē��� 3-NH2-γ-CyD �̃A�~�m��Ƃ̊ԂɐÓd���ݍ�p�������A���_�ő��ݍ�p���邱�Ƃɂ���ăO���R�[�X��F�����Ă���ƍl������B

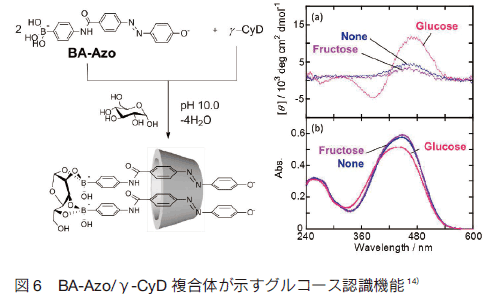
�@����A�} 6 �̂悤�� BA-Azo �� γ-CyD �ɕ�ڂ����� BA-Azo/γ-CyD �����q�����̂̓����������ɂ��Ē��ׂ��Ƃ���A�O���R�[�X���݉��� ICD �X�y�N�g���ɕ�ڍ\���ω��ɂ�� π-π * �J�ڗR���̃X�v���b�g�^�R�b�g�����ʂ��ϑ�����A���O���z���X�y�N�g���ɂ����Ă��A�O���R�[�X���݉��ŋɑ�g���̒Z�g���V�t�g���ϑ����ꂽ�j 14) �BBA-Azo �� γ-CyD �ւ̕�ڋ����ׂ��Ƃ���ABA-Azo �� γ-CyD �� 2 ���q��ڂ���ABA-Azo ���m�����s�z�u�Ń_�C�}�[�`�������ۂ̃A�]���\��Ԃ̗�N�q���ݍ�p�ɋN�����钴���q�����������Ă��邱�Ƃ����炩�ɂȂ����B���̂��Ƃ���Aγ-CyD �ɕ�ڂ��ꂽ 2 ���q�� BA-Azo �ŃO���R�[�X��F�����Ă��邱�Ƃ����������B�ȏ�̂悤�ɁA���q�F���v���[�u���q CyD �����̂Ƃ��đ��_�F�������邱�Ƃɂ���āA�������̑I�𐫂�e�Ղɐ���ł���B
�S�D�f���h���}�[��p�������q�F���V�X�e��
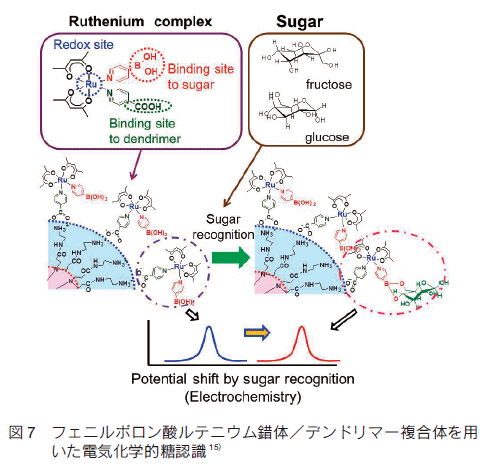
�@�f���h���}�[�͋K���I�ɕ�����J��Ԃ����؏�̍����q�ł���B ���̂悤�ȓ����I�ȍ\����L���邱�Ƃ���A�f���h���}�[�͎��Ɏ����悤�ȑ��̍����q�ɂ͌����Ȃ���X�̓��������B�@�����q�ɂ�������炸�A���q�ʕ��z�����ɋ����A�ψ�ȕ��q�ʂ������q�ł���B�A���[�ɔ������̊��\��𑽐��L���Ă��邱�Ƃ���A�f���h���}�[���[���C�����邱�Ƃő��_�F���@�\�����������w�Z���T�[�̐v�����҂ł���B�����ŁA�f���h���}�[���[�ɃA�~�m���L����|���A�~�h�A�~���ipolyamidoamine, PAMAM�j�f���h���}�[�\�ʂɁA�������ʂƂ��ăJ���{���_��A���q�F�����ʂƂ��ăt�F�j���{�����_��L����Ҍ��������e�j�E������ �mRuII (acac) 2�i4-Bpy�j�i4-Cpy�j�n�iHacac: acetylacetone, 4-Bpy: 4- boronic pyridine, 4-Cpy: 4-carboxylic pyridine�j��Ód���ݍ�p�ɂ��W�ς����A���̓d�C���w�I���o���s�����i�} 7�j 15�j �B���F���@�\�̕]���ɂ́A�����d�����x�Ɠd�ʌ��o�\��L��������p���X�{���^�����g���[�iDPV�j�@��p���Ă���B�t���N�g�[�X�� �mRuII (acac)2�i4-Bpy�j�i4-Cpy�j�n/PAMAM-G2 �n�t�ɓY���������A���́mRuII (acac�j2�i4-Bpy�j�i4-Cpy�j�n/PAMAM-G2 �̔g�̕��d�ʑ��ɐV���ȃs�[�N��������B�O���R�[�X��K���N�g�[�X��Y���������ɂ͓d�ʃV�t�g�͏������A�d�ʃV�t�g�����邱�Ƃɂ���đI��I�Ƀt���N�g�[�X�����o�ł���B�܂��APAMAM �f���h���}�[�̐����ς��ē��l�̑�����s�����Ƃ���A����̒Ⴂ�������ɑ��鉞���\�������Ȃ����B����͗p�������̂��V�X�^�ŁA���̔F�����ʂł���t�F�j���{�����_�� PAMAM �f���h���}�[�̓����Ɍ����Ă��邽�߁A�^�[�Q�b�g�ł��铜���q���{�����_���ʂɋߐڂł����x�̊Ԍ����K�v�ł��邱�Ƃ������Ă���B
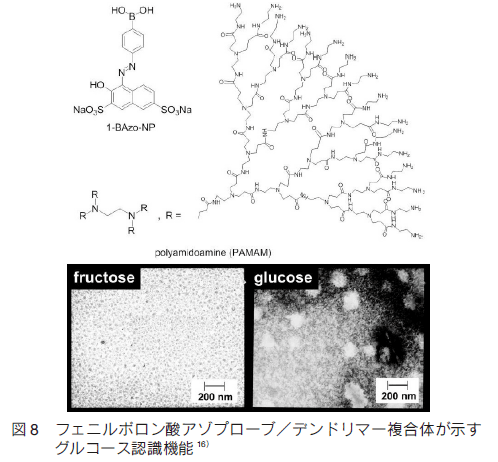
�@�܂��A�M�҂�̓f���h���}�[�\�ʏ�փA�j�I�����̃t�F�j���{�����_���W�ς��������w�Z���T�[�̊J�����s���Ă��� 16�j �B���q�F�����ʂɃt�F�j���{�����_������A�]�v���[�u�i1-BAzo-NP�j���������A�����������ɂ����� PAMAM �f���h���}�[�̕\�ʂɐÓd�I�Ɏ��ȏW�ς����������q�����̂ł���i�} 8�j�B 1-BAzo-NP �̓����_�o�b�t�@�[���A�����������ɂ����ăt���N�g�[�X�A�O���R�[�X��K���N�g�[�X�ɂ͖w�lj����������Ȃ��B�������A���̗n�t���� PAMAM �f���h���}�[�� 4 ����iPAMAM-G4 �j��Y������ƁAPAMAM �f���h���}�[�\�ʂ� 1-BAzo-NP ���W�ς��A���قȓ������@�\�������B�Ⴆ�A 1-BAzo-NP/PAMAM-G4 �����̂́A�O���R�[�X�ɉ������ċÏW�̂��`�������B���̋ÏW�̌`���͒��g�����̋z���x�ω��i���x�j�̑���ŕ]���ł���B 1-BAzo-NP �� PAMAM-G4 �f���h���}�[�̕\�ʏ�ɍŖ��Ɏ��ȏW�ς��������ɁA���̑��x���ł������Ȃ邱�Ƃ����炩�ɂȂ����B�����āAPAMAM �f���h���}�[�̐����� 3 ���ォ��� 5 ����܂ŕω������ē��l�̑�����s�����Ƃ���A��������P���̎�ނ� PAMAM �f���h���}�[�̐��㐔�ɉ����ĕω������B�����[�����ƂɁA 1-BAzo-NP/PAMAM-G5 �ł́A�K���N�g�[�X�I��I�ȉ������N����B�����̌��ʂ́APAMAM �f���h���}�[�\�ʂɂ����� 1-BAzo-NP �̏W�ϖ��x�𐧌䂷�邱�Ƃɂ���āA���F���I�𐫂�����ł��邱�Ƃ������Ă���B
�@����ɕM�҂�́A�J���{���_���[��L����t�F�j���{�����_�^�A�]�v���[�u�iB-Azo-Cb�j�� PAMAM �f���h���}�[���[�̃A�~�m������w�����ɂ���Č��������� B-Azo-Cb/PAMAM �����̂��v�����i�} 9�j 17�j �B���� B-Azo-Cb/PAMAM �����̂������|�_�Z�����[�X�������쐻���A��X�̓��̗A���\�ׂ��Ƃ���AB-Azo-Cb/PAMAM �����̂�|�_�Z�����[�X�����ɕ�������̓��̗A���\�́A�n�t���ł� B-Azo-Cb/PAMAM �����̂̓��I�𐫂ƈ�v�����B����́A�t�F�j���{�����_������Œ薌�^�̓��A�����N�����Ă��邱�Ƃ������Ă���B�܂��A�t�F�j���{�����_�^�A�]�v���[�u��Ód�I�� PAMAM �f���h���}�[�\�ʂɎ��ȏW�ς������ۂ̌��ʂƓ��l�ɁA�p���� PAMAM �f���h���}�[�̐���ɂ���ē��̗A���\�ɈႢ������邱�Ƃ����炩�ɂ��Ă���B�����̌��ʂ́A�t�F�j���{�����_�^�v���[�u/PAMAM �����̂�p���āA���̃f���h���}�[�̐��㐔��t�F�j���{�����_�^�v���[�u�̏C�����x����ɂ���āA���̑I��I�Ȍ��o�╪���ւ̉��p�̉\�������������̂ł���B
�T�D������|���}�[��p�����}�N���ȕ��q�F���V�X�e��
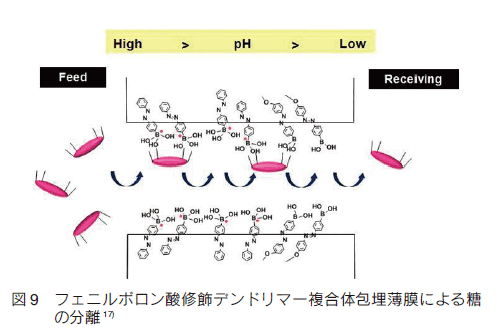
�@�@���_���ݍ�p�͓V�R�̌n�ɂ����Č����̐e�a����I�𐫂����߂邽�߂ɂ悭�p�����Ă���헪�ł���B���̂悤�Ȑ����̌n�ɕ�����A�l�H�n�ɂ����đ��_�̎ア���ݍ�p��g�ݍ��킹���o�C�I�C���X�p�C�A�[�h�V�X�e���̊J�����i��ł���B���_�ɂďq�ׂ��悤�ȃ^���p�N���̍����\���`���ɕ���ĕ��q�v����Ă�����̂ɢ�i�m�Q���������B�i�m�Q���͑����Ȃǂ̒�����̐e���������q�ɑa�����@�\�����\��𑤍��ɏ��������������q����Ȃ�A���̑������ˋ��_�ɂ��Ď��ȑg�D�I�Ƀl�b�g���[�N�����邱�ƂŁA���a���\ nm �̃i�m���q���`������B�M�҂�́A�����̑����Ƀr�^�~�� B6 ���킸���ɏC�������r�^�~�� B6 �u��������v�����i�} 10�j 18�j,19) �B���̃r�^�~�� B6 �u��������p���A�����������ɂ����ăr�^�~�� B6 �̃A���f�q�h��ƃ^���p�N�����̃A�~�m��Ƃ� Schiff ����`�������邱�Ƃɂ���āA�^���p�N�����ˋ��_�Ƃ����^���p�N���ˋ��i�m�Q�����J�������B�r�^�~�� B6 �Ɉ����C�I����z�ʂ����ASchiff ����`���𑣐i���邱�ƂŃJ�`�I�����^�A�j�I�����^���p�N���̂�����Ƃ��i�m�Q�����`�����邱�Ƃ��ł���B�܂��A�����[�����ƂɁA���̃^���p�N���ˋ��i�m�Q���͌��̃^���p�N���̍����\����ێ����Ă���A�i�m�Q���ւ̊��\��C���ɂ���čזE���������������サ���邱�Ƃ���A�^���p�N���f���o���[�L�����A�Ƃ��Ẳ��p�W�J�����҂���Ă���B

�U�D������
�@�{�e�ł́A�����q�����̌`���𗘗p�������_���q�F���V�X�e���ɂ��āA�M�҂�̌����𒆐S�ɂ܂Ƃ߂��B���݁A�����q�����̌`���ɂ�镪�q�F���𗘗p���āA�����C�I����̕��q�̑I��I�Ȍ��o������V�X�e���̊J����A�a�����ۂ̂悤�ȃ}�N���Ȍn�̊Ȉե�v���Ȍ��o�@�̊J����i�߂Ă���B���߂ɏq�ׂ��悤�ɁA���镪�q�����̕��q�� 1 : 1 �ŔF�����ĉ��������r�I�P���Ȍn�Ɋ�Â��z�X�g�\�Q�X�g���w�╪�q�F�����w����A�������i���̉ߒ��őn��o�����A���x���k���ȑ��_�F���^�̕��q�F���n��l�H�I�Ȍn�ō\�z���A����𗽉킷��@�\��n�����邱�Ƃ����ꂩ��̉ۑ�ł���ƍl������B���̂悤�Ȑ����̂����݂ɕ�����o�C�I�C���X�p�C�A�[�h�V�X�e���A���Ȃ킿���_�F���^�̕��q�F���V�X�e���J����i�߂Ă������Ƃ��A������̃i�m�}�e���A����@�\���ޗ��̊J�����s���Ă�����ʼnv�X�d�v�ɂȂ�Ǝv����B
| ���҃v���t�B�[�� | |
| ���� | �y�� �D�u�iYuji Tsuchido�j |
|---|---|
| ���� | ��q��w���H�w���@���ʌ����� |
| �A���� | ��102-8554 �����s���c��I���䒬 7-1 TEL�F03-3238-3371�AFAX�F03-3238-3361 E-mail�Fy-tsuchido@sophia.ac.jp |
| �o�g�w�Z | ������Ȏ��ȑ�w��w�@�������Ȋw���畔���������Ȋw��U |
| �w�� | ���m�i���w�j |
| ��� | ���q�F���A�i�m�o�C�I�}�e���A���A�����q���w |
| ���� | ���� ���m�iTakashi Hayashita�j |
|---|---|
| ���� | ��q��w���H�w�������������H�w�� ���� ��q��w �w�� |
| �A���� | ��102-8554 �����s���c��I���䒬 7-1 TEL�F03-3238-3372�AFAX�F03-3238-3361 E-mail�Fta-hayas@sophia.ac.jp |
| �o�g�w�Z | ��B��w��w�@�H�w�����ȍ������w��U |
| �w�� | �H�w���m |
| ��� | ���q�F���A�����q���w�A���͉��w |
| Copyright(c) 1996-2015 DOJINDO LABORATORIES,�@ALL Rights Reserved. |