光線力学的治療への応用を目指した新規光感受性物質の開発
株式会社 同仁化学研究所 平島 義紀
1. はじめに
日本における悪性腫瘍(癌)の死亡率・罹患率は増加の一途を
たどり、2006年に癌で死亡した人は329,314例、2002年に新たに
診断された癌(罹患全国推計値)は589,293例にのぼっている(国
立がんセンター がん対策情報センター調べ)。これまでの癌の治
療法は、外科手術による切除が約7割を占め、それには痛みが伴
い、臓器の温存ができない。また、抗癌剤治療や放射線治療は副
作用を起こすという欠点があり、患者は大きな負担を余儀なくさ
れてきた。そこで、患者の負担を軽減する新しい治療法として注
目されているのが光診断・治療である。
本稿では、光化学反応を利用して癌細胞を消滅させる治療法の
ひとつである、光線力学的治療(Photodynamic therapy: PDT)に
焦点を当て、PDTの概略、ならびに問題点を述べるとともに、PDT
における癌治療の向上を目指した新しい試みについて紹介する。
2. 光線力学的治療
PDTは、腫瘍親和性光感受性物質が有する腫瘍組織、新生血管
への特異的な集積性と光の励起によって発生する一重項酸素(活
性酸素の一種)の強い細胞破壊効果を利用した治療法である。本
法は、1979年にDoughertyらが、乳癌の皮膚転移に対して、ヘマ
トポルフィリン誘導体(Hematoporphyrin derivatives)を用いて
PDTを初めて以来、数多くの研究がなされている1, 2)。
PDTは、正常組織に大きな障害を与えることがなく、低エネル
ギーで病変部を治療することができ、レーザー光照射によって
様々な病変に対して治療可能である。そのため、近年、妊孕(に
んよう)性の温存療法(治療後も子供を産める)を希望する若年
患者の増加傾向がある中、そうしたニーズに答える治療法とし
て、その有用性が注目されている。PDTは従来の方法と異なり、
子宮頸部をほぼ原形のまま残し、治癒率も高く、術後の妊娠分娩
に支障がない。
腫瘍親和性光感受性物質が光線に暴露されると、光エネルギー
を吸収して励起状態(一重項状態)に遷移する。これが基底状態
に戻る際のエネルギー転換により生じる活性酸素が細胞を変性、
壊死に陥らせると考えられている(実際には、腫瘍親和性光感受
性物質は静脈投与後、腫瘍組織に集積し、赤色光線によって励起
される)。
このように、光感受性物質はPDTで代表されるように、活性酸
素種による酸化ストレスを負うことで、腫瘍細胞等の特定の細胞
を殺傷する目的で用いられる。しかし現在、臨床で使用される薬
剤には光線過敏症(投与した薬剤が太陽光のエネルギーを吸収し
て光増感反応を起し、発生した活性酸素種により紅斑、水疱、色
素沈着等皮膚の異常反応を引き起こす)という合併症を生じる
ケースがある。
最近では、第2世代光感受性物質として、レザフィリン
(Laserphyrin , 明治製菓)(Fig.1)が早期肺癌に対して、ビスダ
イン(Visudyne , 明治製菓)(Fig.1)が早期肺癌に対して、ビスダ
イン(Visudyne , NOVARTIS)(Fig.2)が加齢性黄斑変性症に
よる脈絡膜新生血管に対して、新たに厚生労働省より認可を受
け、急速に普及し、光感受性物質の副作用として問題だった光線
過敏症は、軽度で済むようになってきている。 , NOVARTIS)(Fig.2)が加齢性黄斑変性症に
よる脈絡膜新生血管に対して、新たに厚生労働省より認可を受
け、急速に普及し、光感受性物質の副作用として問題だった光線
過敏症は、軽度で済むようになってきている。
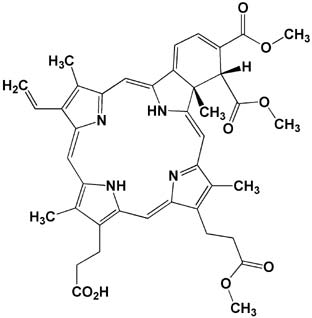
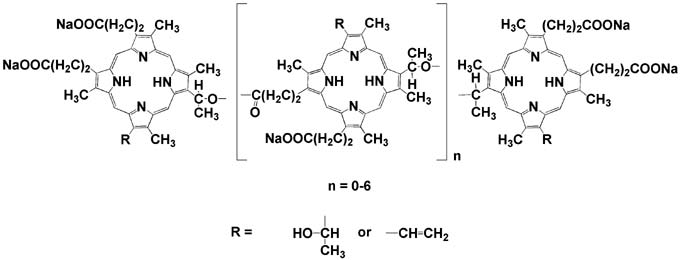
これらは、第1世代光感受性物質であるフォトフリン(Porfimer
sodium, Photofrin , 日本ワイスレダリー)(Fig.3)よりも吸収帯
の波長が長波長側に存在し、励起効率が高く、また正常組織から
早く排泄される特性をもつため、光線過敏症等の副作用が少ない
とされる。フォトフリンは組織透過性の比較的高い630 nmの赤
色光線で励起され光線力学反応が発生するが、ここで問題になる
のは光感受性物質の吸収効率である。最も生体由来組織の影響が
少ない励起波長は650 ~ 700 nm近辺とされており、より深部病
巣の治療を目指す場合、長波長領域での吸収帯を有するレザフィ
リン(波長:664 nm)やビスダイン(波長:689 nm)が有力となっ
てくる。 , 日本ワイスレダリー)(Fig.3)よりも吸収帯
の波長が長波長側に存在し、励起効率が高く、また正常組織から
早く排泄される特性をもつため、光線過敏症等の副作用が少ない
とされる。フォトフリンは組織透過性の比較的高い630 nmの赤
色光線で励起され光線力学反応が発生するが、ここで問題になる
のは光感受性物質の吸収効率である。最も生体由来組織の影響が
少ない励起波長は650 ~ 700 nm近辺とされており、より深部病
巣の治療を目指す場合、長波長領域での吸収帯を有するレザフィ
リン(波長:664 nm)やビスダイン(波長:689 nm)が有力となっ
てくる。
しかしながら、腫瘍への選択性が不十分である等の問題は未解
決であり、脈絡膜新生血管は網膜にも存在することが示されてい
るため、光活性化後に網膜色素上皮や網膜外顆粒層を含む網膜構
造にも付帯的に損傷が起こる可能性がある3)。
そこで、光感受性物質に “スイッチ” を持たせ、腫瘍が存在す
る部位でのみ光増感機能を発揮することが可能になれば腫瘍以外
の損傷が防止できると考えられる。また、薬剤投与後の直射日光
を避ける必要が解消され、合併症として懸念される光線過敏症を
回避することができ、PDT における癌治療の向上が期待される。
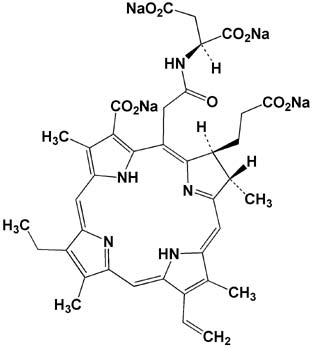
Fig.1 Laserphyrin
Fig.2 Visudyne
Fig.3 Photofrin
3.Thiazole orangeの特性を利用した新規光感受性物質の開発
3-1. Thiazole orange( TO) の有用性
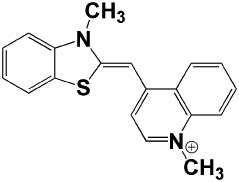
Thiazole orange (TO) (Fig. 4) は2種類の芳香環が結合して共
役系を構成する非対称のシアニンである。この色素の水溶液中で
の蛍光強度は無視できる程度であるが、核酸と結合した時には極
めて強い蛍光を出す。芳香環間の化学結合周りの回転が停止して
の基底状態への無輻射遷移が排除されるため、蛍光強度の増加が
起こると考えられている。その結果、TOの核酸へのインターカ
レーションが起こると量子収率が増大し、DNAやRNAを高感度
に検出することが可能となる。このTOの特性を用いて、血液中
の網状赤血球測定を行ない、赤血球内変形体を検出するなど、多
くのアプリケーションがある。
Fig.4 Thiazole orange
3-2.新規光感受性物質“PhoTO-Gal”の開発
そこで、小出らはTOに高水溶性のかさ高い構造を付加させる
ことで、細胞中における生体分子への結合性を下げ、この構造が
生体内の反応により切り出されると、その結合性が回復し、光増
感能が増大するという手法を考え、光感受性機能の“オン”と“オ
フ”を制御できる光感受性物質の開発を試みた4)。
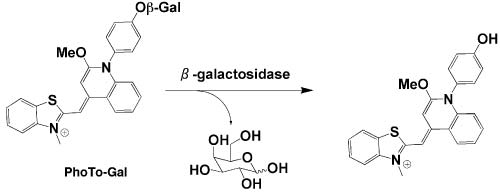
まず、TO誘導体に代表的なレポーター酵素であるβ-galactosidaseに
よって切り出されるβ-galactosyl基を付加させ
た化合物“PhoTO-Gal”を合成した。
そして、生細胞中での機能を評価するため、lacZ 遺伝子が
導入されたHEK293 lacZ (+) 細胞と導入されていないHEK293
lacZ( -) 細胞を用いて、1 μml/l のPhoTO-Gal を添加した細胞に
おける光照射時の細胞殺傷能の検討を行なった。その結果、β
-galactosidase を発現するHEK293 lacZ( +) 細胞において 光を
照射した部位での細胞死が確認された。このことより、“PhoTOGal”は、光感受性機能の“オン”と“オフ”をβ-galactosidaseによって制御した光増感剤であることが確認され、光増感剤の新
たな有効性が示された(Scheme 1)。
Schemel. Design of PhoTO-Gal
今後、本手法はプロドラッグとして、癌細胞で還元酵素を産生
するようにデザインされた遺伝子と共に、薬剤を投与する治療法
(gene-directed enzyme prodrug therapy) もしくは、癌細胞と特
異的に結合する抗体に還元酵素を結合させた複合体と共に薬剤を
投与する治療法 (antibody-directed enzyme prodrug therapy) に
も適用可能であると考えられる。また、標的部位の細胞におけるpH変化や
他の酵素反応等を更に識別することで、特定条件下にある細胞種のみを
より高い選択性で殺傷することができる系の確立も望まれる。
▲ページのトップへ
参考文献
1) T. J. Dougherty, G. Lawrence, J. H. Kaufman, D. Boyle, K. R. Weishaupt, A.
Goldfarb, J. Natl. Cancer Inst., 1979, 62(2), 231-237.
2) 加藤治文 監修, (2002) PDTハンドブック -光線力学的治療のアドバンストテ
クニック-, 医学書院.
3) U. Schmidt-Erfurth, T. Hasan, K. Schomacker, T. Flotte, R. Birngruber, Lasers
Surg. Med., 1995, 17(2), 178-188.
4) Y. Koide, Y. Urano, A. Yatsushige, K. Hanaoka, T. Terai, T. Nagano, J. Am.
Chem. Soc., 2009, 131(17), 6058-6059.
▲ページのトップへ
|



 , 明治製菓)(Fig.1)が早期肺癌に対して、ビスダ
イン(Visudyne
, 明治製菓)(Fig.1)が早期肺癌に対して、ビスダ
イン(Visudyne